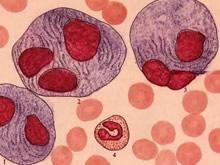
簡介
 戈謝病
戈謝病戈謝病(Daucher disease發音“go-shay” 舊稱高雪病)是一種由基因突變引起的遺傳疾病。基因在正常情況下負責葡糖腦苷脂酶的作用,這種酶幫助人體分解成名為葡糖腦苷脂的脂肪。有戈謝病的患者,不能產生這種酶,因而也不能分解脂肪,這樣就把脂肪累積在肝臟、脾和骨髓中。戈謝病能導致疼痛、疲勞、黃疸、骨損傷、貧血甚至死亡。
雖然戈謝疾病可能影響任何種族的人員,但對來自東歐(Ashkenazi)的猶太人影響更為普遍。在Ashkenazi猶太人口中,戈謝病是最普遍的遺傳疾病,大約1/450人的機率。在總體人口中,影響的機率是1/10萬,按照美國國家戈謝疾病基金的統計,有2500位美國人患戈謝病。
在1991年,酶取代治療變成對戈謝病第一有效治療方法,治療由根據研究提供的改性型葡糖腦苷脂酶組成。治療只要在門診部進行。每隔兩周治療一次,每次花1—2小時。酶取代療法能停止和經常逆轉戈謝病的症狀,讓患者享受更好的生活質量。
病因
GD為常染色體隱性遺傳性疾病。是由於β-葡糖苷酶-葡糖腦苷酯酶缺乏致葡糖腦苷脂在肝、脾、骨骼和中樞神經系統的單核巨噬細胞內蓄積。此病的根本缺陷在於缺乏葡萄糖腦苷脂酶的活性,此酶能把葡萄糖腦苷脂分解成葡萄糖和神經醯胺。常在兒童期發病,但亦有許多在嬰兒期和成年期發病,典型的病理學特徵是廣泛的網狀細胞增生,細胞充滿葡萄糖腦苷脂和纖維細胞漿,細胞變形,有一個或幾個細胞核偏離細胞中心,這些細胞可在肝,脾,淋巴結及骨髓中被發現。
臨床表現
 戈謝病
戈謝病任何年齡自出生至80歲均可發病,但以少年兒童多發,7歲以下更多。可分為三型:
1、成人型(Ⅰ型) 為本病最常見類型,也是脂質貯積病中常見者。猶太人中多見,但各民族中均有。在美國估計每年兒童患者不到5000例。任何年齡均可起病,常以脾臟大就醫。進展可快可慢,進展慢者,脾臟大尤甚,有時有脾梗死或脾破裂而發生急腹症症狀。肝臟呈進行性腫大,但不如脾臟腫大明顯。病程久者,皮膚及黏膜呈茶黃色,常誤診為黃疸,暴露部位如頸、手及小腿最明顯,呈棕黃色。眼球結膜上常有楔形瞼裂斑,底在角膜邊緣,尖指向內、外眥,初呈黃白色,後變為棕黃色。肺累及時可影響氣體交換而出現症狀。晚期患者四肢可有骨痛,甚而病理性骨折,以股骨下端最常見,也可累及股骨頸及脊柱骨。有脾功能亢進時可因血小板減少而有出血傾向。小兒患者身高及體重常受影響。
2、嬰兒型(Ⅱ型) 患兒自生後即可有肝大、脾大,3~6個月時已很明顯,有吸吮、吞咽困難,生長發育落後表現。神經系統症狀突出,頸強直、頭後仰、肌張力增高、角弓反張、踺反射亢進,最後變為軟癱,無反應。腦神經受累時可有內斜,面癱等症狀。易並發感染。由於病程短暫,多於嬰兒期死亡,因此肝、脾臟腫大不如成人型明顯,無皮膚色素沉著,骨骼改變不顯著。
3、幼年型(Ⅲ型) 常於2歲至青少年期發病,脾大常於體檢時發現,一般呈中度腫大。病情進展緩慢,逐漸出現中樞神經系統症狀,如:肌陣攣性抽搐、動作不協調、精神錯亂,最後臥床不起。肝臟常輕微腫大,但也可進行性腫大而出現肝功能嚴重損害。
檢查
1.血常規
多為輕至中度,正細胞正色素性貧血,血小板可輕度減少,淋巴細胞比值相對增多。
2.組織病理學檢查
骨髓細胞塗片的尾部找到戈謝細胞。戈謝細胞體積大,直徑約20~80μm,多呈卵圓形,含有一或數個偏心胞核,核染色質粗糙,胞漿量多,呈淡藍色,充滿交織成網狀或洋蔥皮樣的條紋結構。細胞做糖原和酸性磷酸酶染色呈陽性。電鏡檢查可見細胞胞漿中有特異性的管狀的腦苷脂包涵體。在肝、脾及淋巴結中也可找到戈謝細胞。
3.β-葡糖腦苷脂酶活性測定
測定白細胞或培養的皮膚成纖維細胞中β-葡糖腦苷脂酶活性。Ⅰ型酶活性相當於正常人12%~45%;Ⅱ型酶活性極低,幾乎測不出;Ⅲ型酶相當於正常人13%~20%。酶活性測定最好同時與患兒的雙親一起檢測更有意義。
4.X線檢查
典型的X線徵象:長骨骨髓腔增寬,普遍有骨質疏鬆,股骨遠端膨大,猶如燒瓶樣。常有股骨頸骨折或脊柱壓縮性骨折,肺部可見浸潤性病變。
5.基因分析
通過基因突變型的分析可助診斷。
6.生化檢查
血清酸性磷酸酶增高。
診斷
根據肝大、脾大或有中樞神經系統症狀骨髓檢查見有典型戈謝細胞、血清酸性磷酸酶增高可做出初步診斷進一步確診應做白細胞或皮膚成纖維細胞GC活性測定。值得注意的是有 時在骨髓中看到一種與戈謝細胞很相似的假戈謝細胞(pseudogaucher’scell)它可出現在慢性粒細胞白血病地中海貧血、多發性骨髓瘤、霍奇金淋巴瘤漿細胞樣淋巴瘤(plasmocytoidlymphoma)及慢性髓性白血病它與戈謝細胞的不同點是胞質中無典型的管樣結構。鑑別診斷時可做GC酶活性測定。
腦電圖檢查可早發現神經系統浸潤在神經系統症狀出現前即有廣泛異常波型。Ⅲ型患者在未出現神經系統症狀前很難與I型鑑別。通過腦電圖檢查可預言患者將來是否有可能出現神經系統症狀。
產前診斷:患者的母親再次妊娠時可取絨毛或羊水細胞經酶活性測定做產前診斷,若患者的基因型已確定也可做產前基因診斷。
典型的細胞可以在骨髓,脾穿刺或肝活檢的標本中發現。細胞培養無腦苷酯酶的活性則可明確診斷,戈謝病可以通過羊膜穿刺術或絨毛取樣而進行產前診斷、DNA技術可以診斷特定的戈謝病等位基因,編碼葡萄糖苷酸的基因定位於人類染色體的Iq21位。
預後
戈謝病Ⅰ型進展緩慢,脾切除後可長期存活,智力正常,但生長發育落後。對葡糖腦苷脂酶製劑替代治療反應顯著,預後最好。
戈謝病Ⅱ型多於發病後1年內死於繼發性感染,少數患者可存活2年以上。
戈謝病Ⅲ型多由於神經系統症狀較重,死於併發症。
產前診斷:患者的母親再次妊娠時可取絨毛或羊水細胞經葡糖腦苷脂酶活性測定做產前診斷。若患者的基因型已確定,也可做產前基因診斷。
鑑別診斷
1、尼曼-皮克病(鞘磷脂貯積症) 見於嬰兒,且肝、脾也腫大,但此病肝大比脾大明顯;中樞神經系統症狀不如戈謝病顯著。主要鑑別點為此病黃斑部有櫻桃紅色斑點,骨髓中所見特殊細胞與戈謝病顯著不同,且酸性磷酸酶反應為陰性,結合其他組織化學染色可資鑑別。
2、某些代謝性疾病 如脂質貯積病中的GM1神經節苷脂貯積症,岩藻糖苷貯積症及黏多糖貯積症IH型,均有肝大、脾大及神經系統表現,但GM1神經節苷脂貯積症50%,有黃斑部櫻桃紅色斑,骨髓中有泡沫細胞,三者均有醜陋面容、舌大、心臟肥大,X射線片均有多發性骨發育不良改變,岩藻糖苷貯積症尚有皮膚增厚及呼吸困難等。
3、具有肝脾腫大的疾病 如血液病中的白血病、霍奇金病、漢-許-克病、重型珠蛋白生成障礙性貧血,鑑別一般不困難。漢-許-克病除肝大、脾大外,尚有骨骼缺損及(或)突眼及(或)尿崩症。另外,尚應與黑熱病及血吸蟲病鑑別。
4、具有戈謝細胞的疾病 戈謝細胞可見於慢性粒細胞白血病、重型珠蛋白生成障礙性貧血、慢性淋巴細胞白血病,此類患者中β-葡糖腦苷脂酶正常,但由於白細胞太多,如慢性粒細胞白血病中神經鞘脂的日轉換率為正常的5~10倍;重型珠蛋白生成障礙性貧血時,紅細胞的神經鞘脂轉換率也增加,超越組織巨噬系統的分解代謝能力,而出現葡糖腦苷脂的沉積,形成戈謝細胞。愛滋病及分枝桿菌屬感染及霍奇金病時也可有戈謝細胞。鑑別有賴於臨床、輔助檢查及β-葡糖腦苷脂酶的測定。
5、脾臟淋巴瘤/白血病:鏡下脾臟內為瀰漫一致的淋巴瘤細胞/白血病細胞浸潤,免疫表型可見異型瘤細胞克隆性生長。對無法解釋的肝脾腫大和輕度貧血或伴有進行性發育遲鈍、智力減退、病理性骨折者應想到該病的可能,骨髓穿刺塗片、切除標本病理切片查到Gaucher細胞,有助於該病診斷,確診依賴血白細胞及皮膚纖維母細胞培養,以同位素標記的葡萄糖苷脂作底物,行β-葡萄糖苷脂酶活力測定,葡萄糖苷酶活力<20%(攜帶者為60%以下),而血清酸性磷酸酶活力高。
治療方法
1、一般療法注意營養,預防繼發感染。
2、對症治療 貧血或出血多者可予成分輸血、巨脾或脾功能亢進症狀明顯者 可考慮切脾,但全脾切除後雖可減輕腹部負擔,減輕貧血和出血傾向,改善發育狀態,偶可自行緩解而痊癒,但有加速肝大及骨骼破壞的可能。故應儘量延遲手術,必要時,可考慮部分脾切除術。骨痛可用腎上腺皮質激素。
3、酶療法 國外近年來採用β-葡糖腦苷脂酶治療本病,取得一定療效。成人型治療1年後一般情況好轉,肝脾明顯縮小,生長發育加快,血紅蛋白升高,血小板亦緩慢上升,肺部受累者,肺功能亦可得到改善。骨病變如舊,但發現治療初期有不伴尿鈣增加的低血鈣情況,推測骨病變好轉可能需較長時間。嬰兒型套用後,肝、脾可縮小,但腦症狀多不能好轉。目前對套用劑量及方法尚不統一,初步套用結果認為2、3U/kg,每周3次,靜脈滴注,療效與60U/kg,每2周1次療效相似。此提示2周1次的大劑量方法非常不經濟,前種方法可降低極為昂貴的藥費。嬰兒型的劑量一般認為應較大,每月70~120U/kg,每周2或3次。此酶的來源有2種:一為來自胎盤名阿糖腦苷酶或β-葡萄腦苷酯酶,另一為重組品,名imiglucerase或cerezyme,各15例雙盲法比較,療效相仿。
靜脈輸入從胎盤中提煉的葡萄糖腦酯酶可以改善Ⅰ型病人的臨床症狀,現較通用的方法是每次靜脈輸入超過1~2小時,每2周1次(劑量因人而異,最初的劑量為每次60u/kg)、治療計畫(劑量,輸入頻率及輸入速率)還需進一步研究,劑量比FDA提倡的每2周60u/kg略少是較為合適的、
4、骨髓移植 異基因骨髓移植治療能使酶活力上升,肝、脾縮小,戈謝細胞減少,但手術危險性與療效必須慎重衡量考慮。
5、基因治療 已試用β-葡糖腦苷脂酶的正常基因插入到自身幹細胞中並進行自身移植,尚需進行繼續研究。
併發症
1、主要併發症為脾梗死或脾破裂而危及生命。脾臟正常結構遭破壞和纖維化;肝臟有不同程度的纖維化。
2、合併病理性骨折,常見於股骨下端骨折,也可見股骨頸及脊柱骨折。
3、腦內的顱神經核、基底節、丘腦、小腦和錐體束等處的神經元退行性變等。
其它
對有本病家族史的孕婦,可測定培養羊水細胞或絨毛細胞中的β-葡糖腦苷脂酶活性、進行產前診斷。近來,亦已開始藉助PCR方法進行DNA分析,更為容易。如已有一孩為本病患者,則以後的胎兒中有50%可能患有本病,故應對胎兒進行產前酶活力檢測,必要時進行人工流產。