定義
亞歷山大病是一種少見的非家族性白質腦病,典型病例表現為以額葉為主的白質異常和巨腦。腦記憶體在Rosenthal纖維是確診亞歷山大病的組織學前提。臨床特點
部分生理、心理及行為的發展出現遲緩,可能有大頭症(Macrocephaly,亦作“巨頭症”,一種頭部逐步脹大的病變)、腦癇、痙攣,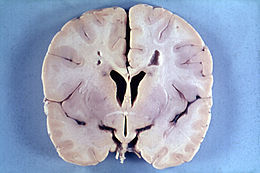 .
.嬰兒型
目前為最常見類型。症狀通常在出生後1~2年發病,病程多數在2~3年,罕見病例可以存活到十幾歲。典型症狀為發育遲緩、巨腦畸形和癲癇,接下來出現精神運動性遲滯、痙攣和四肢癱。嬰兒通常沒有反應,不會學笑,頭圍漸進性增大,出生後6~18個月頭圍通常超過正常的98%,頭失去控制,偶爾患兒出生時就有巨腦畸形,但也有罕見病例因為顱縫已閉合不出現巨頭。此外部分患兒合併梗阻性腦積水,原因可能為室管膜下出現羅森塔纖維(Rosenthalfibers,RF)導致腦室系統狹窄、閉塞影響腦脊液流通所致。
少年型
比嬰兒型少見。發病年齡6至十幾歲,可存活10年或更長。不同之處在於主要為腦幹受累的症狀,如假性球麻痹(吞咽困難、飲水嗆咳和構音不清)、眼瞼下垂、眼球震顫和面癱,也可出現全身痙攣、無力,不出現巨頭,智慧型可以不受損或表現為緩慢進行性下降。
成年型
罕見,其臨床表現類似多發性硬化或少年型亞歷山大病,但發病年齡較晚,以剛成年的患者居多。
亞歷山大病多為散發,沒有家族史,但罕見。Wohlwill(1959)和Klein(1988)等報導嬰兒型亞歷山大病同胞兄弟姐妹中有患病者,推測可能為常染色體隱性遺傳所致;Howard等(1993)報導1例家族成年型亞歷山大病,可能為常染色體顯性遺傳。
診斷標準
(1)以額葉為主的廣泛腦白質異常。(2)腦室周緣在T1加權像呈高信號而在T2加權像呈低信號。
(3)基底節和丘腦異常。
(4)腦幹異常,特別累及了中腦和延髓。
(5)一個或多個結構(包括腦室周緣,額葉白質、視交叉、穹隆、基底節、丘腦、齒狀核和腦幹)的對比強化。
5條標準中符合4條即可確認為亞歷山大病)。
病理學
亞歷山大病是一種遺傳性疾病,影響中樞神經系統(中腦和小腦)。它是一種與膠質纖維酸性蛋白(GFAP)相對應的染色體17q21段的基因突變。這種病是一種隱性遺傳代謝性疾病,所以若孩子的父母帶有這個基因突變,他們的子女會有一半機會遺傳有這種病。亞歷山大症屬於腦白質失養症(Leukodystrophy)的一種類型:“腦白質失養症”又名“腦白質營養不良”,但這病症跟營養不良無關,而是指一組白質脫髓鞘性病變,會影響髓鞘發育或生長。亞歷山大症患者會由於脂肪酸代謝障礙,令極長鏈脂肪酸在腦白質異常積累,使腦白質被破壞,並形成一種纖維狀的嗜酸性粒細胞沉積,稱為羅森塔爾纖維(Rosenthalfiber)。這一種羅森塔爾纖維並不存在於健全人士,只會在某些特定的病症,例如一些癌症的患者身上出現,分別只在於羅森塔爾纖維在亞歷山大症患者身上出現的位置與其他病變患者並不相同。
根據亞歷山大症患者的計算機斷層掃描(CT)顯示:
患者的腦白質密度較低;
腦額葉占主導性;
+/-側腦室擴張
病因與發病機制
亞歷山大病的病因仍不十分清楚,但有關RF的研究很多。1990年Bettica等在超微免疫定位研究中已經證實RF對膠質纖維酸性蛋白有免疫反應,而膠質纖維酸性蛋白是星形細胞中間絲的主要成分。RF含有兩種小的應激蛋白(aB-晶體蛋白、熱休克蛋白27),其中aB-晶體蛋白已經能從RF中分離、純化出來,可能是RF的一種主要成分。1993年1waki發現缺氧能導致這種aB-晶體蛋白升高,在破碎紅纖維中這種蛋白也升高,因此認為本病與線粒體功能有關。1982年Horoupian發現將鎳絲植入鼠腦可制出RF的實驗模型,但他對RF的形成機制未搞清楚。目前對本病作了更深入的研究,1996年把人類神經膠質纖維酸性蛋白的基因插入到鼠模型中,導致了神經膠質蛋白的過度表達,鼠的中樞神經系統出現了廣泛分布的RF,鼠出生後第10天死亡,這種轉基因鼠提供了RF的形成,成為亞歷山大病的模型,有關本病明確的病因與發病機制還有待於進一步的深入研究。
治療
亞歷山大症目前還沒有根治的方法,或標準治療過程。同種異體骨髓移植曾在一名七個月大的患病女嬰身上嘗試,但對她的病情未有改善。預後
預後一般較差。對於發病時間較早的病例,病人通常在病徵出現之後10年內死亡。通常情況下,發病時間越晚,病者的病發時期亦越慢。參看
髓鞘計畫(TheMyelinProject)斯坦尼斯基金會
膠質纖維酸性蛋白

