簡介
 帕金森病性痴呆
帕金森病性痴呆帕金森綜合徵(Parkinsonism)不同於帕金森病,臨床表現可部分甚至全部類似帕金森病不同之處在於帕金森綜合徵的病因明確即任何直接或間接破壞多巴胺均能引發帕金森綜合徵。常見的帕金森綜合徵有以下幾種:藥物性:臨床上最常見,這些藥物包括氟哌啶醇、氯丙嗪、甲氧氯普胺、利舍平、甲基多巴等,都可能引起帕金森綜合徵;血管性:腦梗死或腦出血等可直接或間接影響多巴胺系統功能;中毒:包括重金屬、煤氣等中毒;代謝性疾病:肝豆狀核變性尿毒症的末期;外傷和腫瘤或遺傳變性疾病。
病因
 帕金森病性痴呆
帕金森病性痴呆1、遺傳因素部分病例(10%~15%)為常染色體顯性遺傳模式。但儘管基因研究已有所發現,學術界仍存在較多爭議,可能與多基因遺傳有關目前尚難定論勱有待進一步研究
2、自由基損傷和氧化磷酸化缺失目前實驗證明人組自由基較對照組明顯升高且線粒體複合體1氧化磷酸化缺陷,這些均與造成線粒體DNA以及其他大分子的損傷有關
3、環境的危險因素臨床和實驗研究證明一種叫1-甲基-4-苯基-1.2.3.6四氫吡啶(簡稱MPTP)的物質中毒與發病有關,目前已用NPTP製作模型進行實驗研究
總之,關於發病機制的研究雖然目前以黑質多巴胺神經元中65%~70%的變性減少脫失,造成紋狀體的多巴胺遞質減少,使紋狀體的多巴胺和乙醯膽鹼(ACh)平衡失調而發病為主,但亦有研究證實腦內其他神經遞質如去甲腎上腺素(NE)5-羥色胺(5-HT),γ-氨基丁酸(GABA)等也參與了發病過程。
機理
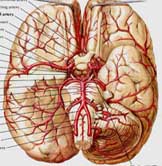
痴呆與腦部器質性疾病有關,病變的部位不同,其臨床表現也有差異,但以額葉、顳葉、邊緣系統以及第三腦室等聯合纖維集聚的部位損害時容易發生智慧型減退。腦變性病可造成大腦萎縮,神經細胞減少、缺失、變性、壞死,有些神經細胞皺縮,星形膠質細胞特殊肥大,增殖與變性,有些神經細胞內神經原纖維纏結和顆粒空泡變性,其改變多以海馬、杏仁區、紋狀體部位較顯著,這些部位與記憶、情緒等有直接關係。某些軀體疾病可使電解質紊亂,酸鹼平衡失調,中間代謝產物大量蓄積,腦血流障礙,還可使腦組織長期處於缺氧狀態,造成腦細胞變性、軟化、壞死或呈點狀出血,導致腦機能障礙。某些微生物毒素浸及腦細胞也可引起腦機能改變。維生素缺乏可引起腦細胞碳水化合物代謝障礙,腦外傷可使腦結構發生改變,腦部腫瘤可直接對腦組織刺激與破壞,腦外傷可使腦結構發生改變,腦部腫瘤可直接對腦組織刺激與破壞,還可對鄰近與遠處腦組織造成機能性壓迫與移位,也可引起腦血液與腦脊液循環障礙,使腦細胞變性、壞死等。某些中毒性疾病可使大腦皮質下灰質蒼白球等處產生軟化、壞死,導致大腦機能障礙,引起智慧型減退。某些疾病除引起上述改變外,尚可引起一些神經遞質的改變,造成兒茶酚胺、乙醯膽鹼、γ-氨基丁酸及腦肽的減少,這些物質與記憶、情緒、思維、行為等均有直接關係,這些物質的減少,可出現情緒、思維、行為、記憶等方面的障礙,而出現痴呆。發病機制
 帕金森病性痴呆
帕金森病性痴呆近年來研究證實多巴胺在胞質內蓄積可導致神經元死亡,囊泡單胺轉運蛋白對多巴胺神經元具有保護作用。研究人員利用大鼠動物模型和細胞培養蛋白電泳技術進行實驗研究結果證實神經毒性物質MPP 與突觸前膜內的囊泡單胺轉運體有較強的親和力,它影響多巴胺在突觸囊泡的貯存,造成突觸體胞質的多巴胺增多,多巴胺通過自身氧化產生大量的自由基和醌類物質勱導致多巴胺能神經元的退行性改變甚至死亡。然而,如果多巴胺與囊泡單胺轉運蛋白結合後進入酸性的分泌囊泡可以避免多巴胺的自身氧化。這個過程在神經保護機制上起了重要作用。研究人員又給大鼠腹腔內注射一定劑量的利舍平後可使其出現類的症狀,如骨骼肌僵硬強直、運動遲緩這是由於利舍平抑制了囊泡單胺轉運蛋白的活動和功能。由此可推論囊泡單胺轉運蛋白的活動和功能受到抑制與發病相關為進一步證實上述研究結果將其實驗室克隆勱的囊泡單胺轉運蛋白基因轉錄進成纖維細胞CHO內,結果發現,表達囊泡單胺轉運蛋白的成纖維細胞CHO能抵抗神經毒性物質MPP 的毒性給神經介質多巴胺後表達囊泡單胺轉運蛋白的成纖維細胞CHO胞質內多巴胺很少蓄積,細胞死亡率明顯低於未轉錄囊泡單胺轉運蛋白基因的成纖維細胞CHO這些實驗研究結果進一步證實了多巴胺勱在胞質內的蓄積多少與神經元死亡率呈正相關多巴胺在胞質內的蓄積可導致神經元死亡可能與的發病有關勱而囊泡單胺轉運蛋白的功能與多巴胺在神經元的蓄積相關它對多巴胺神經元具有保護作用此研究為的治療提供了新的理論依據並對傳統的左鏇多巴治療提出了質疑。
併發症
本病屬於慢性進展性疾病,因運動功能及精神障礙使患者生活質量下降,如發展到痴呆則更為嚴重。如不及時治療,患者生存期明顯縮短,晚期因長期臥床極易罹患各種慢性軀體疾病及繼發各系統感染或衰竭。如出現肺炎、尿路感染等併發症。約有1/4的帕金森病人因過分擔心疾病而伴有抑鬱症狀。抑鬱狀態女性患者可有自殺企圖。臨床表現
 帕金森病性痴呆
帕金森病性痴呆1、神經系統症狀和體徵
(1)運動緩慢(bradykinesia)和運動不能(akinesia)是PD常見症狀之一。起病緩慢多從單肢或一側肢體開始,表現為動作減少和動作緩慢,患肢笨拙不靈活,精細動作困難協同動作減少,影響日常生活如吃飯用筷不能;書寫時可出現書寫緩慢字越寫越小(稱“小寫症”);久坐後起立困難臥床翻身困難。行走起步困難,上肢協同擺動減少且越走越快,呈慌張步態。行進中停步呈前沖步態轉彎不靈活或轉彎動作分解。早期多無語言障礙吞咽活動多不受影響,隨病程進展逐漸出現口齒不清、流涎病情加重出現說話不清構音吞咽障礙
(2)肌強直僵硬(rigidity)姿勢異常和姿勢反射障礙是常見症狀與錐體束病變的痙攣性肌張力增高不同,PD是錐體外肌張力增強,屈肌和伸肌均受侵犯。PD的肌強直呈僵直狀態,這是由於伸肌頑固對抗使伸肌和屈肌張力均增高使肌肉僵直不能鬆弛。臨床表現動作減少運動緩慢由於伸屈肌張力不平衡和不協調,檢查發現肢體被動活動時肌張力增高,呈“齒輪樣”阻抗感被動肢體呈現“鉛管樣”強直面頰肌強直導致面部表情減少、呆板,呈特有的“面具臉”全身肌肉強直導致姿勢異常和姿勢反射障礙嚴重肌強直使頭稍向前傾軀幹俯屈前臂內收肘關節屈曲,使身體失去正常直立姿勢呈彎曲前傾姿勢,成為PD特有的姿勢行走時可見步態慌張體位不穩,嚴重時發生動作僵住。
(3)震顫(tremor)也是PD三主征之一,最為常見。約有1/3病人以此為首發症狀。約有70%~80%的病人有此症狀。震顫是主動肌群與拮抗肌群收縮不協調導致交替收縮使肢體呈4~6次/s的節律性震顫該症狀在臨床上多緩慢發生,從單肢或一側肢體開始,以上肢遠端、特別是手的震顫最具特徵性它與共濟失調的意向性震顫相反多在安靜時出現稱為靜止性震顫。手指震顫明顯呈“搓丸樣”或“捻珠樣”在主動的隨意動作如拿取物品時則震顫減輕或消失睡眠時震顫消失,情緒激動時震顫加重在一般情況下起病由一側上肢手震顫開始,隨病情發展擴展至下肢和對側肢體病情加重時亦可累及下頜、口唇、舌及頭部等震顫。
(4)其他症狀和體徵:PD病人多無主觀感覺異常但隨病情進展有些病人可出現強直肌群疼痛如肩背部呈脹痛刺痛等不適。PD少數病人可見到下肢尤其小腿肌肉疼痛不適,多在安靜或睡眠時出現小腿肌肉蠕動樣疼痛伴有不規則的小腿活動,呈不安腿綜合徵表現,影響睡眠和休息。
PD病人腱反射多不受累。偶有腱反射活躍和亢進者。當肌強直嚴重時腱反射引出困難,但無病理反射。一旦引出病理征時則應考慮帕金森疊加綜合徵,如多系統萎縮或考慮為繼發性帕金森綜合徵。多發性腔隙性腦梗死可見到錐體束征和錐體外束征同時存在應注意鑑別
自主神經功能障礙也是PD病人常見症狀臨床表現多汗面部潮紅、流涎、肢體皮溫過低、頑固性便秘和膀胱排空勱不全,也有些病人面部皮脂溢出過多或脂溢性皮炎等
2、精神心理症狀注意力不集中是PD病人中相當常見的症狀。
同時可伴有動作減少、言語緩慢情緒低沉等有些病人注意力渙散,出現生理錯覺乃至視空間感知障礙索。
少數病人主動活動減少,出現人格改變表現欣快、行為幼稚、性格孤僻膽怯、萎靡猶豫、多疑、易激惹、以自我為中心等不願參加社會活動甚少探親訪友抑鬱焦慮等多為患病後心理障礙所致的患者可發展成抑鬱焦慮症。
幻聽被害妄想和疑病妄想、聯想障礙少見索,有些索是繼發於意識障礙的譫妄狀態。
抑鬱狀態女性患者多見勱表現為反應遲緩、情緒低落、焦慮,嚴重者可有自殺企圖抑鬱程度與神經病變相關,表現反應遲鈍、情緒低落焦慮自殺企圖常是來精神科治療的主要原因。抑鬱也可以是本病的首發症狀,以女性多見。
PD病人認知功能障礙注意力不集中記憶力障礙也是與動作緩慢情緒低落抑鬱等心理障礙有關對這些病人檢查如給予足夠的時間勱其記憶力、計算力和定向力等仍屬正常但PD病人約有15%~20%發展成全面認知障礙,智慧型衰退。臨床表現記憶力喪失計算力、定向力和判斷力喪失發展成痴呆隨病程進展,智力亦逐漸降低,呈現皮質下痴呆特點。
本病呈緩慢進展逐年加重影響整個社會功能最後導致痴呆死亡多由軀體疾病或並發感染所致。
併發症:本病屬於慢性進展性疾病,因運動功能及精神障礙使患者生活質量下降,如發展到痴呆則更為嚴重如勱不及時治療,患者生存期明顯縮短晚期因長期臥床極易罹患各種慢性軀體疾病及繼發各系統感染或衰竭如出現肺炎、尿路感染等併發症約有1/4的人因過分擔心疾病而伴有抑鬱症狀抑鬱狀態女性患者可有自殺企圖。診斷
 帕金森病性痴呆
帕金森病性痴呆2、精神症狀出現在神經系統症狀之後。
3、神經系統具有典型三大主征——運動減少且緩慢,肌強直靜止性震顫神經檢查無錐體束征排除各種原因的繼發性帕金森綜合徵即可診斷。
4、嚴重者出現痴呆勱。
鑑別診斷1、腦炎後帕金森綜合徵發生於任何年齡主要先有腦炎病史後出現運動不能——強直綜合徵。運動笨拙肌強直、震顫,但靜止性震顫少見早在1920年歐洲發生“昏睡性腦炎”以後世界各地均有發病該病病因未明僅從臨床流行病學和病理所見認為病毒性腦炎。主要病變以腦幹中腦黑質損害為主神經細胞壞死、膠質細胞增生膠質結節。臨床表現為帕金森綜合徵伴有陣發性眼動危象即發作性眼球固定任何方向,每次發作幾分鐘乃至幾十分鐘對症治療可用金剛烷胺和苯海索等。多巴胺製劑療效不佳。
2、關島帕金森——痴呆綜合徵本病是20世紀40年代後,發生在西太平洋關島的一種疾病多在中年人緩慢發病。一般先出現帕金森綜合徵伴有痴呆,繼之出現肌萎縮側索硬化。少數亦可先出現肌萎縮側索硬化後出現帕金森綜合徵和痴呆。病理所見普遍性腦萎縮,黑質和藍斑色澤變淺勱神經原纖維纏結見於黑質海馬杏仁核和新皮質神經元。未見到老年斑和路易小體。流行病學研究提示外源性環境因素致病,可能與食用蘇鐵樹果實有關。近年提出與地區水土化學元素有關,尚未定論勱
3、藥物誘發帕金森綜合徵主要見於抗精神病藥物,如酚噻嗪類的奮乃靜、氟奮乃靜。丁醯苯類氟哌啶醇以及降壓藥利血平和鈣離子拮抗劑桂利嗪、氟桂利嗪等;長期服用具有阻滯多巴胺D2受體作用者亦可誘發本病臨床表現為遲發性運動障礙,多以運動減少、緩慢、肌強直為主要症狀靜止狀震顫少見病因明確停藥後多數能自行緩解和恢復
4、血管性帕金森綜合徵多見於中老年人患有高血壓動脈硬化和糖尿病等腦血管病危險因素者。主要病理特點是基底節紋狀體區、內囊丘腦半卵圓中心和腦橋等腔隙性梗死或小梗死病灶。臨床表現多數病人有短暫性腦缺血發作(TIA)或小卒中發作病史,錐體束和錐體外束症狀相併發生或先後發生肢體乏力、運動減少緩慢肌強直或僵直多以下肢為重呈“小步步態”靜止性震顫少見。同時多伴有下肢無力出現雙側或單側錐體束征,病理反射陽性。有些病例有假性延髓性麻痹,吞咽障礙最終出現性格改變,強哭強笑,認知障礙,痴呆等。病程呈階梯式進展。頭顱C
 帕金森病性痴呆病人
帕金森病性痴呆病人5、進行性核上性麻痹(PSP)也是中老年中樞神經系統變性病發病年齡50~77(64)歲病變主要在黑質和藍斑,中腦神經核、齒狀核和蒼白球等。起病緩慢早期出現錐體外束症狀運動減少、緩慢,靜止性震顫少見肌僵直明顯,姿勢平衡障礙為臨床所見之一即頸背肌軀幹肌強直呈直立後伸位易向後傾倒。與身體前傾、屈曲前沖姿勢相反。另一臨床特徵即核上性眼肌麻痹即眼球向上、下注視不能。病情緩慢進展相繼出現認知障礙和視空間技能損害晚期發展為痴呆病程3~12(6或7)年多死於肺部感染早期左鏇多巴製劑有一定療效久用無效且易發生體位性低血壓近年提出清除自由基抗氧化劑治療,效果有待觀察。
6、多系統萎縮(MSA)MSA是發生在40~60歲中老年人的一組中樞神經系統變性病起病隱襲緩慢最早由Adams(1961)提出包括紋狀體黑質變性,Shy-Drager綜合徵,橄欖體-腦橋-小腦萎縮(OPCA)和肌萎縮側索硬化(ALS)等近年病理研究發現上述病變部位雖不同,但是病理改變卻相當一致的,即泛素蛋白染色陽性膠質細胞包涵體、神經細胞包涵體和神經絲等 。
症狀
 帕金森病性痴呆症狀分析會診
帕金森病性痴呆症狀分析會診(2)體位性低血壓伴有脊髓、自主神經功能障礙:陽痿、膀胱障礙等(Shy-Drager綜合徵)。
(3)橄欖體-腦橋-小腦萎縮(OPCA):臨床特點是錐體外束征錐體束征和小腦共濟失調。
(4)帕金森綜合徵症狀並發脊髓前角病變,手部肌肉萎縮肌萎縮側索硬化症狀等。
由於起病緩慢病程長上述4條症狀並不同時出現往往是先後出現。臨床具有兩條即可診斷。有時只有一組綜合徵亦可單獨做出症狀診斷如OPCA或Shy-Drager綜合徵等
實驗室輔助檢查有助臨床診斷:①立臥位血壓差40mmHg即可診斷體位性低血壓;②在紋狀體黑質變性,頭顱MRI可見側裂增寬殼核萎縮和側腦室擴大等腦萎縮;③OPCAMRI特別矢狀位可清楚顯示橋池增寬,腦橋和橄欖體以及小腦萎縮;④肌電圖可證實帕金森綜合徵並發肌萎縮側索硬化。
7、與功能性精神病鑑別早期以精神症狀為主者易誤診詳細的軀體檢查可發現證據,精神症狀常帶器質性損害色彩,如意識人格記憶、智慧型障礙還應注意功能性精神病在抗精神病藥治療中出現假性症狀。
8、其他腦變性疾病從病史神經系統病變和體徵(三聯征)結合“面具臉”、慌張步態“搓泥丸”動作進行鑑別
檢查
 帕金森病性痴呆檢查室
帕金森病性痴呆檢查室2、腦脊液雖然有報告多巴胺代謝產物高香草酸和5-羥色胺產物5-羥吲哚醋酸含量減少,但實用性不強
其它輔助檢查
1、腦電圖檢查雖然偶有慢波改變但均無特徵性改變
2、影像學頭顱CTMRI勱在少數例晚期可見普遍性腦萎縮勱,但無局灶性改變MRI對綜合徵在鑑別診斷方面十分重要,例如血管病性帕金森綜合徵可在基底節區有多發腔隙性梗死和梗死軟化灶。單光子核素掃描(SPECT)未見特徵所見。正電子發射斷層掃描(PET)18氟多巴(18F-dopa)可見紋狀體區攝取降低。
治療
 帕金森病性痴呆治療
帕金森病性痴呆治療2、多巴胺替代療法多巴胺替代治療在改善生活質量和延緩病程方面取得進展。但長期服用出現多種運動異常表現如“開-關現象”、“劑末現象”和“晨僵”等。因此替代療法對症狀較輕者不宜過早套用從小劑量開始達到最小有效劑量維持,用藥不宜過多加量,出現異動現象隨時調整用藥。
(1)左鏇多巴(L-Dopa):250mg2~3次/d,口服現多用複方多巴製劑效果較好。①左鏇多巴/苄絲肼(美多巴)(含量:左鏇多巴0.2g勱苄絲肼0.05g)0.125~0.25g,2~3次/d,口服;②帕金寧或息寧(Sinemet)是左鏇多巴/卡比多巴混合劑含量:左鏇多巴200mg,卡比多巴50mg套用劑量1片,2~3次/d,口服
(2)多巴胺受體激動劑:多巴胺受體激動劑主要作用與激活D2受體有關①溴隱亭(bromocriptineparlodel)多與左鏇多巴合用勱開始0.625mg逐漸加量維持量10~30mg,1次/d。②培高利特(Pergolidamedytate)開始用量0.05mg1次/d在2~7周內逐漸增加至0.25mg,2~3次/d,每天維持量應小於0.75~5mg以下。
3、哌啶烷基類衍生物步地品(叔二苯哌啶)10~50mg/d,常用30mg/d影響多巴胺的釋放或吸收同時具有抗膽鹼能作用和可靠的5-HT系統刺激效應。
4、奧芬那君(orphenadrine)100~150mg/d,具有抗膽鹼能及較弱的抗組胺作用,對本病肌僵直有效。
5、精神藥物當病人出現明顯的抑鬱興奮幻覺或妄想症狀時勱可選用適當的抗抑鬱藥或抗精神病藥治療,但應注意精神藥物的副作用,劑量宜低。
6、其他用藥根據發病機制與自由基和興奮性胺基酸毒性作用有關配合套用抗氧化劑和谷氨酸拮抗劑等治療,如維生素E、維生素C等以及其他對症治療藥如肌強直可用肌肉鬆弛劑等
7、外科治療腦立體定向手術有一定療效,但不作為首選治療。外科手術治療經歷較長歷史。20世紀60年代以後的立體定向一側丘腦腹外側核豆狀核襻丘腦底核毀損術和80年代以來的自身腎上腺皮質和異體胎兒中腦黑質細胞移植於一側尾狀核殼核等雖近期有一定療效但均未得到承認而中斷近年微電極引導CTMRI立體定向內側蒼白球腹後部毀損術獲得成功,取得較好療效,宜應選好適應證配合藥物治療並有待積累經驗總結療效。
預後
帕金森病是中樞神經系統變性病主要是黑質變性致使紋狀體多巴胺(DA)不足,使DA與興奮性乙醯膽鹼(ACH)失去平衡由於目前病因和發病機制尚未十分清楚,因此尚沒有有效的預防和根治措施該病起病緩慢,病程長平均病程可達13年,最長可達20或30年勱特別套用左鏇多巴製劑延緩病程取得進展。合理套用多巴胺製劑配合康復以及綜合藥物治療對改善生活質量和延緩病程仍有實際意義。
預防
 帕金森病性痴呆預防中心
帕金森病性痴呆預防中心雖然目前尚不完全清楚的致病原因,但許多研究表明它可能與環境毒素有關。一些研究結果顯示,“跟從來沒在家裡或院子裡用過殺蟲劑或除草劑的人比較起來,一生當中使用這兩種藥劑時間加起來低於30天的人,患的幾率增加40%;如果一生當中使用這兩種藥劑時間加起來超過160天以上患的幾率便增加到70%。”尤其是對家族中有患者的人要更加注意如果某人的直系親屬中有患者,那么他患的幾率要大一些所以要特別注意避免接觸一些環境中危險因素如殺蟲劑、農藥、重金屬錳,親屬中有患者的人要避免從事電焊工種等。
飲食原則及要求:①限制全天蛋白質攝入量,以每公斤體重0.8g為宜。人的症狀睡眠後減輕全天蛋白質分配應白天少,晚餐適量增多②適量增加碳水化合物的比例60%~65%是有益處的③供給充足水,以補充水分消耗,也減少藥物副作用④適宜增加蔬菜、水果和蜂蜜⑤避免刺激性調味品和食物,禁菸酒。⑥營養治療僅有輔助作用此外患者選擇飲食時,應考慮到老年病人常伴有動脈粥樣硬化、心腦血管病、糖尿病等應結合本病及老年人的特點給予適當的總熱量。正常成人24h基礎代謝約需熱量5857.6~7531.2kJ(1400~1800kcal)臥床病人一般需供給熱量6276~8368kJ(1500~2000kcal),下床活動的病人一般需供給熱量8368~9623.2kJ(2000~2300kcal),仍在從事體力勞動的輕症患者,需供給熱量10041~12552kJ(2400~3000kcal)。以上數據,在為具體病人選擇飲食時可作參考。
出現手足顫動為特徵的是因為人腦內傳達信息的物質多巴胺減少研究發現通過食物攝取的鈣可促進腦內合成多巴胺。所以平時應多吃含鈣豐富的食物如:蝦米、海帶、紫菜、豆漿、豆製品、牛奶雞蛋等對預防有良好作用總之愉悅的進餐和多樣的膳食組合對預防有良好的作用。因此,一天的飲食中食物應多種多樣,包括穀類、蔬菜、水果類、豆類、肉類等。據測定,每天吃300~500g穀類食物,可以攝取充足的碳水化合物、蛋白質膳食纖維和維生素B等營養素;每天大約吃400g蔬菜,1~2箇中等大小的水果,從中可獲得維生素A、B、CE及多種礦物質和膳食纖維。國外研究已經證明,多食用這些富含維生素的抗氧化劑食物可以降低的風險。適當喝茶咖啡等含有咖啡因的飲品對預防也有一定作用。國外研究發現每天喝咖啡1~2杯的人可以使的發生率減少50%;若每天喝3~4杯咖啡得的機會只有正常人的1/5咖啡因飲品中含的咖啡因可以讓腦中的神經傳遞物質的敏感度增加,所以不論在行為或動作上都不易出現的肌肉僵硬症狀。