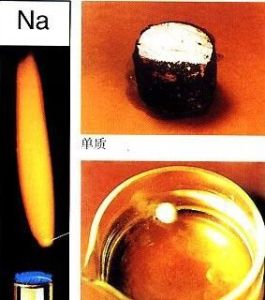
發現簡史
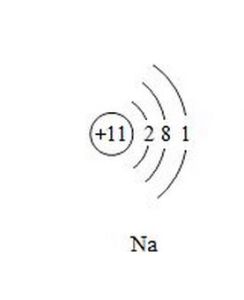 鈉
鈉戴維將鉀和鈉分別命名為Potassium和sodium ,因為鉀是從氫氧化鉀(Potash),鈉是從碳酸鈉(Soda)中得到的,它們至今保留在英文中。鉀和鈉的化學符號K,Na分別來自它們的拉丁文名稱Kalium和Natrium。
簡介
鈉(Sodium)是一種化學元素,它的化學符號是Na,它的原子序數是11。鈉單質不會在地球自然界中存在,因為鈉在空氣中會迅速氧化,並與水產生劇烈反應,所以只能存在於化合物中。
性狀
 鈉
鈉銀白色立方體結構金屬。新切面有銀白色光澤,在空氣中氧化轉變為暗灰色。質軟而輕,密度比水小,在-20℃時變硬,遇水劇烈反應,生成氫氧化鈉和氫氣並產生大量熱量而自燃或爆炸。在空氣中,燃燒時發亮黃色火焰。
遇乙醇也會反應,跟乙醇的羥基反應,生成氫氣和乙醇鈉,同時放出熱量。能與鹵素和磷直接化合。能還原許多氧化物成元素狀態,也能還原金屬氯化物。溶於液氨時成藍色溶液。在氨中加熱生成氨基鈉。溶於汞生成鈉汞齊。相對密度(H₂O)0.968。熔點97.82℃。沸點881.4℃。有腐蝕性。CAS號:7440-23-5
化學反應
與氧氣的反應
在常溫時:4Na+O₂==2Na₂O (氧化鈉,由於衍射顯得有點灰色)
在點燃時:2Na+O₂=點燃=Na2O2 (淡黃色粉末) 並發生:Na+O₂=點燃=NaO₂(超氧化鈉)
鈉在空氣中點燃時,迅速熔化為一個閃亮的小球,發出黃色火焰,生成過氧化鈉(Na₂O₂)和少量超氧化鈉(NaO₂)淡黃色的煙。過氧化鈉比氧化鈉穩定,氧化鈉可以和氧氣加熱時化合成為過氧化鈉,化學方程式為:2Na2O+O2=△=2Na2O₂
與非金屬的反應
2.鈉能跟鹵素、硫、磷、氫等非金屬直接發生反應,生成相應的化合物(以下反應常溫下均反應),如
2Na+Cl2==2NaCl (放出大量熱,生成大量白煙)
2Na+S==Na2S(硫化鈉)(鈉與硫研磨會發生爆炸)
2Na+Br2==2NaBr(溴化鈉)(溴化鈉可以用作鎮靜劑)
與水的反應
在燒杯中加一些水,滴入幾滴酚酞溶液,然後把一小塊鈉放入水中。為了安全應在燒杯上加蓋玻璃片。
觀察到的現象及由現象得出的結論有:
1、鈉浮在水面上(鈉的密度比水小)
2.鈉熔成一個閃亮的小球(鈉與水反應放出熱量,鈉的熔點低)
3.鈉在水面上四處遊動(有氣體生成)
 鈉
鈉4.發出嘶嘶的響聲(生成了氣體,反應劇烈)
5.事先滴有酚酞試液的水變紅(有鹼生成)
反應方程式
2Na+2H2O=2NaOH+H2↑
鈉由於能跟水劇烈反應,能引起氫氣燃燒甚至爆炸,所以鈉失火決不能用水或泡沫滅火器撲救,必須用乾燥沙土來滅火。鈉具有很強的還原性,可以從一些熔融的金屬鹵化物中把金屬置換出來。由於鈉極易與水反應,所以不能用鈉把居於金屬活動性順序鈉之後的金屬從其鹽的水溶液中置換出來,而是先和水反應生成氫氧化鈉,再由氫氧化鈉與鹽反應。但在高溫下,利用反應平衡原理,可以用金屬鈉來制鉀、銣、銫
與酸溶液反應
鈉與水反應本質是和水中氫離子的反應,所以鈉與鹽酸反應,不是先和水反應,
鈉與酸溶液的反應涉及到鈉的量,如果鈉少量,只能與酸反應,如鈉與鹽酸的反應:
2Na+2HCl=2NaCl+H2↑
如果鈉過量,則優先與酸反應,然後再與酸溶液中的水反應。
注意:鈉和酸反應十分劇烈,極易產生爆炸,在試驗中應注意鈉的量和酸的濃度。
與鹽反應
(1)與鹽的水溶液反應
將鈉投入鹽的水溶液中,鈉先會和溶液中的水反應,生成的氫氧化鈉如果能與鹽反應則繼續反應。
如將鈉投入硫酸銅溶液中:
2Na+2H2O=2NaOH+H2↑
2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
(2)高溫下的置換反應反應
這類反應多數為置換反應,常見於金屬冶煉工業中,如
4Na+TiCl4==熔融==4NaCl+Ti(條件為高溫且需要氬氣做保護氣)
Na+KCl=高溫=K(g)+NaCl
★鈉與熔融鹽反應不能證明金屬活動性的強弱
與有機物反應
鈉還能與某些有機物反應,如鈉與乙醇反應:
2Na + 2C2H5OH = 2C2H5ONa + H2↑(生成物為氫氣和乙醇鈉)
製備方法
戴維法
戴維是通過電解法首先製得的金屬鈉,隨後幾十年內,工業上採用鐵粉和高溫氫氧化鈉反應的方法製備金屬鈉,同時得到四氧化三鐵和氫氣。電解氫氧化鈉也得到金屬鈉,但是此方法使用較少。當前工業上普遍採用氯化鈉-氯化鈣熔鹽電解法制金屬鈉。
當斯法
在食鹽(即氯化鈉)融熔液中加入氯化鈣,油浴加熱並電解,溫度為500℃,電壓6V,通過電解在陰極生成金屬鈉,在陽極生成氯氣。然後經過提純成型,用液體石蠟進行包裝。
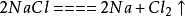 鈉
鈉化學方程式:
卡斯納法
以氫氧化鈉為原料,放入鐵質容器,熔化溫度320~330℃,以鎳為陽極,鐵為陰極,在電極之間設定鎳網隔膜,電解電壓4~4.5V,陰極析出金屬鈉,並放出氧氣。再將製得的金屬鈉精製,用液體石蠟包裝。
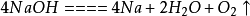 鈉
鈉化學方程式:
(在此實驗中由於熔融狀態的鈉的密度約為:0.968g/cm³,而熔融狀態下的氫氧化鈉的密度約為:2.130 g/cm³,所以最終產生的熔融狀態的鈉單質會浮在熔融的氫氧化鈉上,與空氣中的氧氣快速化合發生危險,所以要在稀有氣體的保護下進行此實驗,否則會發生危險!)
生理作用
鈉是人體中一種重要無機元素,一般情況下,成人體內鈉含量大約為3200(女)~4170(男)mmol,約占體重的0.15%,體內鈉主要在細胞外液,占總體鈉的44%~50%,骨骼中含量占40%~47%,細胞內液含量較低,僅占9%~10%。
1、鈉是細胞外液中帶正電的主要離子,參與水的代謝,保證體內水的平衡,調節體內水分與滲透壓。
2、維持體內酸和鹼的平衡。
3、是胰液、膽汁、汗和淚水的組成成分。
4、鈉對ATP(腺嘌呤核苷三磷酸)的生產和利用、肌肉運動、心血管功能、能量代謝都有關係,此外,糖代謝、氧的利用也需有鈉的參與。
5、維持血壓正常。
6、增強神經肌肉興奮性。
人體鈉的主要來源為食物。鈉在小腸上部吸收,吸收率極高,幾乎可全部被吸收,故糞便中含鈉量很少。鈉在空腸的吸收大多是被動性的,在迴腸則大部分是主動的吸收。鈉與鈣在腎小管內的重吸收過程發生競爭,故鈉攝入量高時,會相應減少鈣的重吸收,而增加尿鈣排泄。因尿鈣丟失約為鈣瀦留的50%,故高鈉膳食對鈣丟失有很大影響。
高溫、重體力勞動、經常出汗的人需要注意補充鈉(飲用淡鹽水等)。鈉普遍存在於各種食物中,一般動物性食物高於植物性食物,但人體鈉來源主要為食鹽、以及加工、製備食物過程中加入的鈉或含鈉的複合物(如谷氨酸、小蘇打等),以及醬油、鹽漬或醃製肉或煙燻食品、醬鹹菜類、發酵豆製品、鹹味休閒食品等。
人體內鈉在一般情況下不易缺乏、但在某些情況下,如禁食、少食,膳食鈉限制過嚴而攝入非常低時,或在高溫、重體力勞動、過量出汗、腸胃疾病、反覆嘔吐、腹瀉使鈉過量排出而丟失時,或某些疾病,如艾迪生病引起腎不能有效保留鈉時,胃腸外營養缺鈉或低鈉時,利尿劑的使用而抑制腎小管重吸收鈉時均可引起鈉缺乏。鈉的缺乏在早期症狀不明顯,倦怠、淡漠、無神、甚至起立時昏倒。失鈉達0.5g/kg體重以上時,可出現噁心、嘔吐、血壓下降、痛性吉爾痙攣,尿中無氯化物檢出。
正常情況下,鈉攝入過多並不蓄積,但某些特殊情況下,如誤將食鹽當食糖加入嬰兒奶粉中餵養,則可引起中毒甚至死亡。急性中毒,可出現水腫、血壓上升、血漿膽固醇升高、脂肪清除率降低、胃黏膜上皮細胞受損等。鈉的適宜攝入量(AI)成人為2200mg/d。
儲存方法
浸放於液體石蠟、礦物油和苯系物中密封保存,大量通常儲存在鐵桶中充氬氣密封保存。金屬鈉不能保存在煤油中是因為與煤油中的有機酸等物質反應成有機酸鈉等物質(呈黃色)附著在鈉表面。當保存在石蠟油中時,空氣中的氧氣也會進入石蠟油,使金屬鈉的表面變灰,形成氧化物膜。
在純度要求不高的少量保存時可用煤油浸泡,如實驗室保存。
貯於陰涼乾燥處,遠離火種、熱源。少量一般保存在液體石蠟中。
與氧化劑、酸類、鹵素分儲分運。
主要用途
工業用途
純淨的金屬鈉在工業上並沒有多大用處,然而鈉的化合物可以套用在醫藥、農業和攝影器材中。氯化鈉就是餐桌上的食鹽。液態的鈉有時用於冷卻核反應堆鈉鉀合金在室溫下呈液態,是核反應堆的導熱劑,起把反應堆產生的熱量傳導給蒸氣輪機的作用。熔融的金屬鈉在增值反應堆中可做熱交換劑。 ) 以往金屬鈉主要用於製造車用汽油的抗暴劑,但由於會污染環境,已經日趨減少。金屬鈉還用來製取鈦,鉀,及生產氫氧化鈉、氨基鈉、氰化鈉等。
實驗用途
在國中教學中,常將金屬鈉與水的反套用作演示實驗向學生展示鹼金屬的活潑性和製造氫氣;在高中化學實驗中會讓學生自己動手操作,並且增多了鈉與乙醇的反應,用以比較水與乙醇的酸性或極性。在科研實驗中,金屬鈉可用來對有機試劑進行深度除水,例如GPC(凝膠液相色譜)對流動液的除水要求特別高,用作流動液或溶劑的四氫呋喃須經過初步除水(用沸石分子篩或無水硫酸鎂等乾燥劑過夜乾燥)、深度除水及蒸餾才能使用。深度除水就可以用金屬鈉與四氫呋喃在70度左右進行回流,加入少量二苯甲酮作為指示劑,當液體變為深紫色時,水就已經除乾淨,直接將回流冷凝管改為直形冷凝管,把溫度稍微再提高,就可以蒸出已經深度除水的四氫呋喃。
生命元素
最危害健康的十種食品添加劑
化學元素周期表
| 族→ | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 電子層 | 0族電子數 | |
| 周期↓ | I A | 0 | |||||||||||||||||||
| 1 | 1 H 氫 | 2 He 氦 | K | 2 | |||||||||||||||||
| II A | III A | IV A | V A | VI A | VII A | ||||||||||||||||
| 2 | 3 Li 鋰 | 4 Be 鈹 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 | L K | 8 2 | |||||||||||
| 3 | 11 Na 鈉 | 12 Mg 鎂 | 13 Al 鋁 | 14 Si 矽 | 15 P 磷 | 16 S 硫 | 17 Cl 氯 | 18 Ar 氬 | M L K | 8 8 2 | |||||||||||
| III B | IV B | V B | VI B | VII B | VIII | I B | II B | ||||||||||||||
| 4 | 19 K 鉀 | 20 Ca 鈣 | 21 Sc 鈧 | 22 Ti 鈦 | 23 V 釩 | 24 Cr 鉻 | 25 Mn 錳 | 26 Fe 鐵 | 27 Co 鈷 | 28 Ni 鎳 | 29 Cu 銅 | 30 Zn 鋅 | 31 Ga 鎵 | 32 Ge 鍺 | 33 As 砷 | 34 Se 硒 | 35 Br 溴 | 36 Kr 氪 | N M L K | 8 18 8 2 | |
| 5 | 37 Rb 銣 | 38 Sr 鍶 | 39 Y 釔 | 40 Zr 鋯 | 41 Nb 鈮 | 42 Mo 鉬 | 43 Tc 鎝 | 44 Ru 釕 | 45 Rh 銠 | 46 Pd 鈀 | 47 Ag 銀 | 48 Cd 鎘 | 49 In 銦 | 50 Sn 錫 | 51 Sb 銻 | 52 Te 碲 | 53 I 碘 | 54 Xe 氙 | O N M L K | 8 18 18 8 2 | |
| 6 | 55 Cs 銫 | 56 Ba 鋇 | 57- 71 鑭系 | 72 Hf 鉿 | 73 Ta 鉭 | 74 W 鎢 | 75 Re 錸 | 76 Os 鋨 | 77 Ir 銥 | 78 Pt 鉑 | 79 Au 金 | 80 Hg 汞 | 81 Tl 鉈 | 82 Pb 鉛 | 83 Bi 鉍 | 84 Po 釙 | 85 At 砹 | 86 Rn 氡 | P O N M L K | 8 18 32 18 8 2 | |
| 7 | 87 Fr 鍅 | 88 Ra 鐳 | 89- 103 錒 | 104 Rf 鑪 | 105 Db | 106 Sg | 107 Bh | 108 Hs | 109 Mt | 110 Ds 鐽 | 111 Rg 錀 | 112 Uub | 113 Uut | 114 Uuq | 115 Uup | 116 Uuh | 117 Uus | 118 Uuo | |||
| 鑭系元 素 | 57 La 鑭 | 58 Ce 鈰 | 59 Pr 鐠 | 60 Nd 釹 | 61 Pm 鉕 | 62 Sm 釤 | 63 Eu 銪 | 64 Gd 釓 | 65 Tb 鋱 | 66 Dy 鏑 | 67 Ho 鈥 | 68 Er 鉺 | 69 Tm 銩 | 70 Yb 鐿 | 71 Lu 鑥 | ||||||
| 錒系元 素 | 89 Ac 錒 | 90 Th 釷 | 91 Pa 鏷 | 92 U 鈾 | 93 Np 鎿 | 94 Pu 鈽 | 95 Am 鎇 | 96 Cm 鋦 | 97 Bk 錇 | 98 Cf 鐦 | 99 Es 鑀 | 100 Fm 鐨 | 101 Md 鍆 | 102 No 鍩 | 103 Lr 鐒 | ||||||