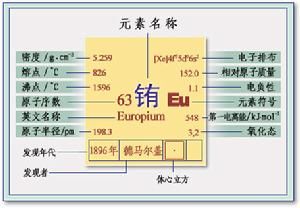
概述
發現人:德馬爾賽發現時間和地點:1901法國
發現過程:1896年,德馬凱(E.Demarcay)發現,1904年,烏爾班(G.Urpain)製得了純的銪的化合物。
元素來源:很少量地存在於獨居石中,常用真空蒸餾氧化銪和金屬鑭的混合物還原來製取。
元素用途:用作彩色電視機的螢光粉,在雷射材料及原子能工業中有重要的套用。
元素描述:第一電離能為5.67電子伏特。能燃燒成氧化物;氧化物近似白色。
簡介
1901年,德馬凱(Eugene-AntoleDemarcay)從“釤”中發現了新元素,取名為銪(Europium)。這大概是根據歐洲(Europe)一詞命名的。銪為鐵灰色金屬,熔點822°C,沸點1597°C,密度5.2434克/厘米³;鈰稀土元素中密度最小、最軟和最易揮發的元素。銪為稀土元素中最活潑的金屬:室溫下,銪在空氣中立即失去金屬光澤,很快被氧化成粉末;與冷水劇烈反應生成氫氣;銪能與硼、碳、硫、磷、氫、氮等反應。銪廣泛用於製造反應堆控制材料和中子防護材料。發現
稀土元素的發現從18世紀末到20世紀初,經歷了100多年,發現了數十個,但只肯定了其中的十幾個。銪被認為是20世紀初被發現的一個稀土元素。1892年布瓦博德朗利用光譜分析,鑑定釤中存在兩種新元素,分別命名為Zε和Zζ。後來在1906年,德馬凱經過研究,確定新元素命名為這兩種元素其實是同一個元素,並命名為europium,元素符號Eu。銪和另一個稀土元素鑥的發現就完成了自然界中存在的所有稀土元素的發現。它們倆的發現可以認為是打開了稀土元素髮現的第四座大門,完成了稀土元素髮現的第四階段。 銪
銪 銪是稀土金屬中的一種。稀土是歷史遺留的名稱,從18世紀末葉開始被陸續發現。當時人們慣於把不溶於水的固體氧化物稱作土,例如把氧化鋁叫做陶土,氧化鎂叫苦土。稀土是以氧化物狀態分離出來,很稀少,因而得名稀土,稀土元素的原子序數是21(Sc)、39(Y)、57(La)至71(Lu)。它們的化學性質很相似,這是由於核外電子結構特點所決定的。它們一般均生成三價化合物。鈧的化學性質與其它稀土差別明顯,一般稀土礦物中不含鈧。鉕是從鈾反應堆裂變產物中獲得,放射性元素147Pm半衰期2.7年。過去認為鉕在自然界中不存在,直到1965年,荷蘭的一個磷酸鹽工廠在處理磷灰石中,才發現了鉕的痕量成分。因此,中國1968年將鉕劃入64種有色金屬之外。1787年瑞典人阿累尼斯(C.A.Arrhenius)在斯德哥爾摩(Stockholm)附近的伊特比(Ytterby)小鎮上尋得了一塊不尋常的黑色礦石,1794年芬蘭化學家加多林(J.Gadolin)研究了這種礦石,從其中分離出一種新物質,三年後(1797年),瑞典人愛克伯格(A.G.Ekeberg)證實了這一發現,並以發現地名給新的物質命名為Ytteia(釔土)。後來為了紀念加多林,稱這種礦石為Gadolinite(加多林礦,即矽鈹釔礦)。
1803年德國化學家克拉普羅茲(M.H.Klaproth)和瑞典化學家柏齊力阿斯(J.J.Berzelius)及希生格爾(W.Hisinger)同時分別從另一礦石(鈰矽礦)中發現了另一種新的物質---鈰土(Ceria)。1839年瑞典人莫桑得爾(C.G.Mosander)發現了鑭和鐠釹混合物(didymium)。1885年奧地利人威斯巴克(A.V.Welsbach)從莫桑得爾認為是“新元素”的鐠釹混合物中發現了鐠和釹。1879年法國人布瓦普德朗(L.D.Boisbauder)發現了釤。1901年法國人德馬爾賽(E.A.Demarcay)發現了銪。1880年瑞士馬利納克(J.C.G.DeMarignac)發現了釓。1843年莫桑得爾發現了鋱和鉺。1886年布瓦普德朗發現了鏑。1879年瑞典人克利夫(P.T.Cleve)發現了鈥和銩。1974年美國人馬瑞斯克(J.A.Marisky)等從鈾裂產物中得到鉕。1879年瑞典人尼爾松(L.F.Nilson)發現了鈧。從1794年加多林分離出釔土至1947年製得鉕,歷時150多年。
性質
元素中文名稱:銪
元素英文名稱:Europium
元素符號:Eu
元素類型:金屬
原子序數:63
相對原子質量:151.96
核內質子數:63
核外電子數:63
核電核數:63
原子體積:(立方厘米/摩爾):28.9
元素在太陽中的含量:(ppm):0.0005
元素在海水中的含量:(ppm)太平洋表面0.0000001
地殼中含量:(ppm):2.1
常見化合價:+2,+3
電負性:1.2
外圍電子排布:4f76s2
核外電子排布:2,8,18,25,8,2
同位素及放射線:Eu-147[24.4d]Eu-148[54.5d]Eu-149[93.1d]Eu-150[36y]Eu-151Eu-152[13.5y]*Eu-153Eu-154[8.6y]Eu-155[7.4y]Eu-156[15.2d]
 |
| 銪 |
第一電離能:546.5KJ•mol-1
第二電離能:1085KJ•mol-1
第三電離能:0KJ•mol-1
單質密度:5.259g/cm3
單質熔點:822.0℃
單質沸點:1597.0℃
原子半徑:2.56埃
離子半徑:1.07(+3)埃
共價半徑:1.85埃
常見化合物:無
氧化態:MainEu+3
OtherEu+2
質子質量:1.05399E-25
質子相對質量:63.441
所屬周期:6
所屬族數:IIIB
摩爾質量:152
最高價氧化物:
密度:5.259
熔點:822.0
沸點:1597.0
外圍電子排布:4f76s2
核外電子排布:2,8,18,25,8,2
晶胞參數:
a=458.1pm
b=458.1pm
c=458.1pm
α=90°
β=90°
γ=90°
維氏硬度:167MPa
晶體結構:晶胞為體心立方晶胞,每個晶胞含有2個金屬原子。
顏色和狀態:銀白色金屬
主要用途
 用作彩色電視機的螢光粉
用作彩色電視機的螢光粉2、近年氧化銪還用於新型X射線醫療診斷系統的受激發射螢光粉。
3、氧化銪還可用於製造有色鏡片和光學濾光片,用於磁泡貯存器件,在原子反應堆的控制材料、禁止材料和結構材料中也能一展身手。因它的原子比任何其他元素都能吸收更多的中子,所以常用於原子反應堆中作吸收中子的材料。
類別
釩酸釔:銪
 摻銪的釩酸釔
摻銪的釩酸釔三氧化二銪
 氧化銪
氧化銪 【英文名稱】ethylenediamine; 1,2-diaminoethane
【相對分子量或原子量】60.11
【密度】0.8994
【熔點(℃)】8.5
【沸點(℃)】117.1
【閃點(℃)】33.9
【蒸氣壓(Pa)】1200(20℃)
【粘度 mPa•s(20℃)】1.54(25℃)
【折射率】1.4540(26℃)
【性狀】:氨氣味的無色透明粘稠液體。
【溶解情況】:溶於水和乙醇,不溶於乙醚和苯。
【用途】:用於制染料、橡膠硫化促進劑、藥物、農藥殺菌劑、氨基樹脂、乙二胺脲醛樹脂、金屬螯合劑EDTA等。液用作清蛋白、纖維蛋白等的溶劑。
【製備或來源】:由氨與乙醇胺或二氯乙烷或二溴乙烷作用而得。
【其他】:能與蒸汽一同揮發,在空氣中灰發煙。有鹼性。有毒。對眼睛、呼吸道、皮膚有刺激性。能吸收空氣中的二氧化碳並能與無機酸生成溶於水的鹽類。
分布
銪在地殼中的含量為0.000106%,是最稀有的稀土元素,主要存在於獨居石和氟碳鈰礦中,自然界有兩種銪的同位素:銪151和銪153。很少量地存在於獨居石中。製造方法
 真空蒸餾氧化銪
真空蒸餾氧化銪富銪鹽酸稀土製備超細高純氧化銪的方法。
一種富銪鹽酸稀土製備超細高純氧化銪的方法,是以富銪鹽酸稀土為原料,其特徵在於所述方法步驟如下:
(1)配料混合:將富銪鹽酸稀土、鹽酸、水進行混合配料;
(2)固-液分離:經過固-液分離,除去不溶性雜質,得到富銪鹽酸稀土溶液料液,料液中稀土的濃度為0.1-1.2mol/L;
(3)電化學還原:將上一步得到的富銪鹽酸稀土溶液在電化學反應器的陰極將三價銪Eu3+還原為二價銪Eu2+,得到EuCl2溶液;
(4)超聲分餾萃取:在超聲萃取設備中,加入EuCl2溶液、萃取液、洗液,三種物料配料的體積比為1∶0.5-5.0∶0.1-2.0,操作條件為超聲頻率19-80kHz,超聲作用強度0.2-20.0W/cm2,操作溫度為5-60℃,進行超聲分餾萃取,中間出口液為EuCl2精製液,進入下一步;
(5)電化學氧化:將上一步得到EuCl2精製液進入電化學反應器中,在電化學反應器的陽極,將二價銪Eu2+氧化為三價銪Eu3+,生成EuCl3精製液;
(6)吸附除雜:在上一步得到的EuCl3精製液中,加入吸附除雜劑,進行進一步深度吸附除雜,經固-液分離,除去雜質,製得純淨的EuCl3精製液,進入下一步;
(7)超聲結晶沉澱:在超聲結晶設備中,加入純淨的鹽酸銪精製液、結晶沉澱劑碳酸氫銨或碳酸銨,鹽酸銪精製液與結晶沉澱劑配料的摩爾比為1∶1.1-1.6,操作條件為超聲頻率19-80kHz,超聲作用強度為0.2-20.0W/cm2,操作溫度為5-60℃,進行超聲結晶沉澱,生成碳酸銪Eu2(CO3)3結晶沉澱物,進入下一步;
(8)固-液分離:經固-液分離,得到固相為碳酸銪Eu2(CO3)3結晶沉澱物,進入下一步;
(9)乾燥、灼燒:在25-800℃乾燥,獲得碳酸銪Eu2(CO3)3;在800-900℃下灼燒,獲得Eu2O3含量≥99.99%,顆粒粒徑為0.01-10.0μm的超細高純氧化銪產品。
化學元素周期表
| 族→ | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 電子層 | 0族電子數 | |
| 周期↓ | I A | 0 | |||||||||||||||||||
| 1 | 1 H 氫 | 2 He 氦 | K | 2 | |||||||||||||||||
| II A | III A | IV A | V A | VI A | VII A | ||||||||||||||||
| 2 | 3 Li 鋰 | 4 Be 鈹 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 | L K | 8 2 | |||||||||||
| 3 | 11 Na 鈉 | 12 Mg 鎂 | 13 Al 鋁 | 14 Si 矽 | 15 P 磷 | 16 S 硫 | 17 Cl 氯 | 18 Ar 氬 | M L K | 8 8 2 | |||||||||||
| III B | IV B | V B | VI B | VII B | VIII | I B | II B | ||||||||||||||
| 4 | 19 K 鉀 | 20 Ca 鈣 | 21 Sc 鈧 | 22 Ti 鈦 | 23 V 釩 | 24 Cr 鉻 | 25 Mn 錳 | 26 Fe 鐵 | 27 Co 鈷 | 28 Ni 鎳 | 29 Cu 銅 | 30 Zn 鋅 | 31 Ga 鎵 | 32 Ge 鍺 | 33 As 砷 | 34 Se 硒 | 35 Br 溴 | 36 Kr 氪 | N M L K | 8 18 8 2 | |
| 5 | 37 Rb 銣 | 38 Sr 鍶 | 39 Y 釔 | 40 Zr 鋯 | 41 Nb 鈮 | 42 Mo 鉬 | 43 Tc 鎝 | 44 Ru 釕 | 45 Rh 銠 | 46 Pd 鈀 | 47 Ag 銀 | 48 Cd 鎘 | 49 In 銦 | 50 Sn 錫 | 51 Sb 銻 | 52 Te 碲 | 53 I 碘 | 54 Xe 氙 | O N M L K | 8 18 18 8 2 | |
| 6 | 55 Cs 銫 | 56 Ba 鋇 | 57- 71 鑭系 | 72 Hf 鉿 | 73 Ta 鉭 | 74 W 鎢 | 75 Re 錸 | 76 Os 鋨 | 77 Ir 銥 | 78 Pt 鉑 | 79 Au 金 | 80 Hg 汞 | 81 Tl 鉈 | 82 Pb 鉛 | 83 Bi 鉍 | 84 Po 釙 | 85 At 砹 | 86 Rn 氡 | P O N M L K | 8 18 32 18 8 2 | |
| 7 | 87 Fr 鍅 | 88 Ra 鐳 | 89- 103 錒 | 104 Rf 鑪 | 105 Db | 106 Sg | 107 Bh | 108 Hs | 109 Mt | 110 Ds 鐽 | 111 Rg 錀 | 112 Uub | 113 Uut | 114 Uuq | 115 Uup | 116 Uuh | 117 Uus | 118 Uuo | |||
| 鑭系元 素 | 57 La 鑭 | 58 Ce 鈰 | 59 Pr 鐠 | 60 Nd 釹 | 61 Pm 鉕 | 62 Sm 釤 | 63 Eu 銪 | 64 Gd 釓 | 65 Tb 鋱 | 66 Dy 鏑 | 67 Ho 鈥 | 68 Er 鉺 | 69 Tm 銩 | 70 Yb 鐿 | 71 Lu 鑥 | ||||||
| 錒系元 素 | 89 Ac 錒 | 90 Th 釷 | 91 Pa 鏷 | 92 U 鈾 | 93 Np 鎿 | 94 Pu 鈽 | 95 Am 鎇 | 96 Cm 鋦 | 97 Bk 錇 | 98 Cf 鐦 | 99 Es 鑀 | 100 Fm 鐨 | 101 Md 鍆 | 102 No 鍩 | 103 Lr 鐒 | ||||||

