概述
鐠是一種銀白色的,中等柔軟的金屬元素,是鑭系元素,在空氣中抗腐蝕能力比鑭、鈰、釹和銪都要強,但暴露在空氣中會產生一層易碎的綠色氧化物,所以純鐠必須在礦物油或密封塑膠中保存。
鐠為淡黃色金屬,質地較軟,有延展性;熔點931°C,沸點3512°C,密度6.773克/厘米³。鐠在空氣中緩慢形成綠色易碎氧化物層;鐠通常以三價氧化態存在。三氧化二鐠可用於製造優良的高溫陶瓷材料,也用於製造綠色的鐠玻璃;鐠在石油化工方面可用作催化劑。
性質
物理性質
自然界中鐠只有一種穩定同位素,141-Pr。但有38种放射性同位素,其中比較穩定的有143-Pr,半衰期為13.57天;142-Pr,半衰期為19.12小
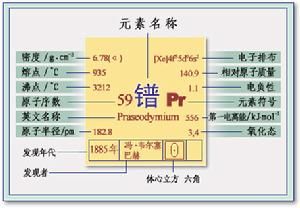
| 熔點 | 931℃ |
| 沸點 | 3.520℃ |
| 密度 | 6.773克/厘米 |
| a | = 367.25 pm |
| b | = 367.25 pm |
| c | = 1183.54 pmα = 90° |
| c | = 1183.54 pmα = 90° |
| β | = 90° |
| γ | = 120°維氏硬度:400 MPa |
| 聲音在其中的傳播速率 | (m/S) 2280 |
| 電離能(kJ /mol) | M - M+ 523.1 |
| 電離能 (kJ /mol) | M+ - M2+ 1018 |
| 電離能 (kJ /mol) | M2+ - M3+ 2086 |
| 電離能 (kJ /mol) | M3+ - M4+ 3761 |
| 電離能 (kJ /mol) | M4+ - M5+ 5543 |
| 元素在太陽中的含量(ppm) | 0.001 |
| 元素在海水中的含量(ppm)太平洋表面 | 0.00000044 |
| 地殼中含量(ppm) | 9.5 |
化學性質
元素符號Pr,屬周期系ⅢB族,稀土元素,鑭系元素。[2]在空氣中抗腐蝕能力比鑭、鈰、釹和銪都要強,但暴露在空氣中會產生一層易碎的黑色氧化物,鐠在空氣中緩慢形成黑色易碎氧化物層;鐠通常以三價氧化態存在,也以4價形式存在。
| CAS號 | 7440-10-0 |
| 原子量 | 140.907.65 [2] |
| 原子序數 | 59 [2] |
| 原子體積(立方厘米/摩爾) | 20.8 |
| 氧化態 | K-L-M-N-O-P |
| 外圍電子層排布 | 4f3 6s2 |
| 鐠的化合物 | 氟化物;PrF 2;PrF 3;PrF 4 |
| 氯化物 | PrCl 3 |
| 溴化物 | PrBr 3、Pr 2Br 5 |
| 碘化物 | PrI 2、PrI 3、Pr 2I 5 |
| 氧化物 | PrO 2、Pr 2O 3 |
| 硒化物 | PrSe |
| 碲化物 | PrTe、Pr 2Te 3 |
| 氮化物 | PrN |
元素特性
自然界中鐠只有一種穩定同位素,141-Pr。但有38种放射性同位素,其中比較穩定的有143-Pr,半衰期為13.57天;142-Pr,半衰期為19.12小時。其他的放射性同位素的半衰期都超不過5.985小時,大部分的半衰期少於33秒。鐠還有6個亞穩態,比較穩定的是138m-Pr(t½2.12小時),142m-Pr(t½14.6分)和134m-Pr(t½11分)。鐠的同位素原子量從120.955u(121-Pr)到158.955u(159-Pr)。穩定同位素141-Pr如果放出β射線,會俘獲電子。主要放射產物為鈰的同位素鈰58和釹的同位素釹60。主要存在於獨居石中。常由水合氯化鐠PrCl3•XH2O經脫水後用金屬鈣還原,或由無水氯化鐠經熔融後電解而製得。
名稱由來
鐠的名稱 praseodymium 來源於希臘語詞prasios(綠色)和didymos(成對的)。1841年發現鑭的瑞典化學家卡爾•古斯塔夫•莫散德從含鑭的礦物中分離出一種稀有的didymium土,1874年瑞典地質學家波•提奧多•克萊夫證實了didymium土實際是兩種元素的混合物。1879年, 勒考•德•布瓦包得蘭從鈮釔礦(samarskite) 中取得的didymium 土中分離出一種新元素釤,因此取名(praseodymium)。 直到1885年奧地利化學家 C•F•奧爾•馮•韋耳斯拔男爵才成功地將didymium土分離為鐠和釹。兩種元素的金屬鹽的顏色不同。
自莫桑德爾先後發現鑭、鉺和鋱以後,各國化學家特別注意從已發現的稀土元素去分離新的元素。在發現釤和釓的同一時期里,1885年奧地利化學家韋爾塞巴赫從didymium(當時被認為是一種稀土元素)的氧化物中分離出兩種新元素的氧化物,其中一種被命名為preseodidymium,後來被簡化為praseodymium,元素符號Pr。發展歷史
 |
| 鐠瑪科技 |
鐠、釓、釤、釹都是從當時被認為是一種稀土元素的didymium中分離出來的。由於它們的發現,didymium不再被保留。而正是它們的發現打開了發現稀土元素的第三道大門,是發現稀土元素的第三階段。但這僅是完成了第三階段的一半工作。確切的將應該是打開了鈰的大門或完成了鈰的分離,另一半就將是打開釔的大門或是完成釔的分離。
鐠是稀土金屬中的一種。稀土是歷史遺留的名稱,從18世紀末葉開始被陸續發現。當時人們慣於把不溶於水的固體氧化物稱作土,例如把氧化鋁叫做陶土,氧化鎂叫苦土。稀土是以氧化物狀態分離出來,很稀少,因而得名稀土,稀土元素的原子序數是21(Sc)、39(Y)、57(La)至71(Lu)。它們的化學性質很相似,這是由於核外電子結構特點所決定的。它們一般均生成三價化合物。鈧的化學性質與其它稀土差別明顯,一般稀土礦物中不含鈧。鉕是從鈾反應堆裂變產物中獲得,放射性元素147Pm半衰期2.7年。過去認為鉕在自然界中不存在,直到1965年,荷蘭的一個磷酸鹽工廠在處理磷灰石中,才發現了鉕的痕量成分。
因此,中國1968年將鉕劃入64種有色金屬之外。 1787年瑞典人阿累尼斯(C.A.Arrhenius)在斯德哥爾摩(Stockholm)附近的伊特比(Ytterby)小鎮上尋得了一塊不尋常的黑色礦石,1794年芬蘭化學家加多林(J.Gadolin)研究了這種礦石,從其中分離出一種新物質,三年後(1797年),瑞典人愛克伯格(A.G.Ekeberg)證實了這一發現,並以發現地名給新的物質命名為Ytteia(釔土)。後來為了紀念加多林,稱這種礦石為Gadolinite(加多林礦,即矽鈹釔礦)。 1803年德國化學家克拉普羅茲(M.H.Klaproth)和瑞典化學家柏齊力阿斯(J.J.Berzelius)及希生格爾(W.Hisinger)同時分別從另一礦石(鈰矽礦)中發現了另一種新的物質---鈰土(Ceria)。1839年瑞典人莫桑得爾(C.G.Mosander)發現了鑭和鐠釹混合物(didymium)。
1885年奧地利人威斯巴克(A.V.Welsbach)從莫桑得爾認為是“新元素”的鐠釹混合物中發現了鐠和釹。1879年法國人布瓦普德朗(L.D.Boisbauder)發現了釤。1901年法國人德馬爾賽(E.A.Demarcay)發現了銪。1880年瑞士馬利納克(J.C.G.De Marignac)發現了釓。1843年莫桑得爾發現了鋱和鉺。1886年布瓦普德朗發現了鏑。1879年瑞典人克利夫(P.T.Cleve)發現了鈥和銩。1974年美國人馬瑞斯克(J.A.Marisky)等從鈾裂產物中得到鉕。1879年瑞典人尼爾松(L.F.Nilson)發現了鈧。從1794年加多林分離出釔土至1947年製得鉕,歷時150多年。
礦產分布
鐠在地殼中的含量約為5.53×10-4%,主要存在於獨居石和氟碳鈰礦中,核裂變產物中也含有鐠。自然界存在的鐠均為穩定同位素鐠–141。套用領域
鐠在石油化工方面可用作催化劑。
鐠作為用量較大的稀土元素,很大一部分是以混合稀土的形式被利用,比如用作金屬材料的淨化變質劑、化工催化劑、農用稀土等等。以鐠釹富集物的形式加入Y型沸石分子篩中製備石油裂化催化劑,可提高催化劑的活性、選擇性和穩定性。作為塑膠改性添加劑,在聚四氟乙烯(PTFE)中加入鐠釹富集物,可明顯提高PTFE的耐磨性能。
稀土永磁材料是當今最熱門的稀土套用領域。鐠單獨用作永磁材料性能並不突出,但它卻是一個能改善磁性能的優秀協同元素。無論是第一代稀土永磁材料釤鈷永磁合金,還是第三代稀土永磁材料釹鐵硼,加入適量的鐠都能有效地提高和改善永磁材料性能。如在SmCo5中加入部分Pr取代Sm可以提高永磁材料的磁能積,兩者的比例一般為80%Sm—20%Pr,若鐠加入過多反而會降低材料的矯頑力和穩定性。在第三代稀土永磁材料釹鐵硼中,添加鐠可以提高材料的矯頑力,德國、日本等國在生產高矯頑力釹鐵硼磁體時,均加入部分鐠。鐠的加入量為5%~8%,最高達10%,可取代1/3的釹。磁性材料對鐠質量要求較高,至少應達到釹的同等質量。加入鐠還能提高磁體抗氧化性能(耐空氣腐蝕)和機械性能,已被廣泛套用於各類電子器件和馬達上。
鐠還可用於研磨和拋光材料。純鈰基拋光粉通常為淡黃色,是光學玻璃的優質拋光材料,已取代拋光效率低又污染生產環境的氧化鐵紅粉。氧化
釹對拋光作用不大,但鐠卻有良好的拋光性能。含鐠的稀土拋光粉會呈紅褐色,也被稱作紅粉,但這種紅不是氧化鐵紅,而是由於含有氧化鐠使稀土拋光粉顏色變深。鐠還被用新型磨削材料,製成含鐠剛玉砂輪。與白剛玉相比,在磨削碳素結構鋼、不鏽鋼、高溫合金時,效率和耐用性可提高30%以上。為了降低成本,過去多用鐠釹富集物為原料,故稱鐠釹剛玉砂輪。
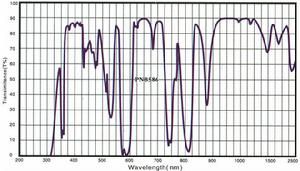
鐠在光纖領域的用途也越來越廣,已開發出在1300~1360nm譜區起放大作用的摻鐠光纖放大器(PDFA),技術日趨成熟。PDFA以其優異的性能價格比,對中國當前大量鋪設的1550nm的CATV系統光纖有線電視的興建改造與系統升級有著重大的實際意義。PDFA將從根本上改變現有的1550nmCATV的網路格局,使1310nmCATV系統在HFC系統改造中成為替代1550nm系統的理想選擇。
同位素
自然界中鐠只有一種穩定同位素,141-Pr。但有38种放射性同位素,其中比較穩定的有143-Pr,半衰期為13.57天;142-Pr,半衰期為19.12小時。其他的放射性同位素的半衰期都超不過5.985小時,大部分的半衰期少於33秒。鐠還有6個亞穩態,比較穩定的是138m-Pr(t½2.12小時),142m-Pr(t½14.6分)和134m-Pr(t½11分)。
鐠的同位素原子量從120.955u(121-Pr)到158.955u(159-Pr)。穩定同位素141-Pr如果放出β射線,會俘獲電子。主要放射產物為鈰的同位素鈰58和釹的同位素釹60。
製備方法
工業上用溶劑萃取法和離子交換法從處理氟碳鈰礦或獨居石得到的混合稀土溶液中分離和提純鐠。金屬鐠用鈣還原鐠的氟化物或氯化物來製取。鑭、鈰、鐠、釹等輕稀土金屬,由於熔點較低,在電解過程可呈熔融狀態在陰極上析出,故一般均採用電解法製取。
常由水合氯化鐠PrCl3·XH2O經脫水後用金屬鈣還原,或由無水氯化鐠經熔融後電解而製得。
注意事項
像其他稀土元素一樣,鐠具有慢性低毒,不是生物必須元素。
化學元素周期表
| 族→ | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 電子層 | 0族電子數 | |
| 周期↓ | I A | 0 | |||||||||||||||||||
| 1 | 1 H 氫 | 2 He 氦 | K | 2 | |||||||||||||||||
| II A | III A | IV A | V A | VI A | VII A | ||||||||||||||||
| 2 | 3 Li 鋰 | 4 Be 鈹 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 | L K | 8 2 | |||||||||||
| 3 | 11 Na 鈉 | 12 Mg 鎂 | 13 Al 鋁 | 14 Si 矽 | 15 P 磷 | 16 S 硫 | 17 Cl 氯 | 18 Ar 氬 | M L K | 8 8 2 | |||||||||||
| III B | IV B | V B | VI B | VII B | VIII | I B | II B | ||||||||||||||
| 4 | 19 K 鉀 | 20 Ca 鈣 | 21 Sc 鈧 | 22 Ti 鈦 | 23 V 釩 | 24 Cr 鉻 | 25 Mn 錳 | 26 Fe 鐵 | 27 Co 鈷 | 28 Ni 鎳 | 29 Cu 銅 | 30 Zn 鋅 | 31 Ga 鎵 | 32 Ge 鍺 | 33 As 砷 | 34 Se 硒 | 35 Br 溴 | 36 Kr 氪 | N M L K | 8 18 8 2 | |
| 5 | 37 Rb 銣 | 38 Sr 鍶 | 39 Y 釔 | 40 Zr 鋯 | 41 Nb 鈮 | 42 Mo 鉬 | 43 Tc 鎝 | 44 Ru 釕 | 45 Rh 銠 | 46 Pd 鈀 | 47 Ag 銀 | 48 Cd 鎘 | 49 In 銦 | 50 Sn 錫 | 51 Sb 銻 | 52 Te 碲 | 53 I 碘 | 54 Xe 氙 | O N M L K | 8 18 18 8 2 | |
| 6 | 55 Cs 銫 | 56 Ba 鋇 | 57- 71 鑭系 | 72 Hf 鉿 | 73 Ta 鉭 | 74 W 鎢 | 75 Re 錸 | 76 Os 鋨 | 77 Ir 銥 | 78 Pt 鉑 | 79 Au 金 | 80 Hg 汞 | 81 Tl 鉈 | 82 Pb 鉛 | 83 Bi 鉍 | 84 Po 釙 | 85 At 砹 | 86 Rn 氡 | P O N M L K | 8 18 32 18 8 2 | |
| 7 | 87 Fr 鍅 | 88 Ra 鐳 | 89- 103 錒 | 104 Rf 鑪 | 105 Db | 106 Sg | 107 Bh | 108 Hs | 109 Mt | 110 Ds 鐽 | 111 Rg 錀 | 112 Uub | 113 Uut | 114 Uuq | 115 Uup | 116 Uuh | 117 Uus | 118 Uuo | |||
| 鑭系元 素 | 57 La 鑭 | 58 Ce 鈰 | 59 Pr 鐠 | 60 Nd 釹 | 61 Pm 鉕 | 62 Sm 釤 | 63 Eu 銪 | 64 Gd 釓 | 65 Tb 鋱 | 66 Dy 鏑 | 67 Ho 鈥 | 68 Er 鉺 | 69 Tm 銩 | 70 Yb 鐿 | 71 Lu 鑥 | ||||||
| 錒系元 素 | 89 Ac 錒 | 90 Th 釷 | 91 Pa 鏷 | 92 U 鈾 | 93 Np 鎿 | 94 Pu 鈽 | 95 Am 鎇 | 96 Cm 鋦 | 97 Bk 錇 | 98 Cf 鐦 | 99 Es 鑀 | 100 Fm 鐨 | 101 Md 鍆 | 102 No 鍩 | 103 Lr 鐒 | ||||||

