概述
元素名稱:鈧
英文名:Scandium
 鈧
鈧元素符號:Sc
原子序數:21
元素系類:過渡金屬
CAS號:7440-20-2
地殼含量:
 %
%相對原子質量:44.955912(6)
原子半徑:160(184)pm
共價半徑:144pm
價電子排布:![]()
電子在每能級的排布:2,8,9,2
常見氧化價:+3(弱鹼性)
晶體結構:六方密排晶格
理化性質
物理性質
熔點:1814K(1541°C)沸點:3103K(2830°C)
密度:
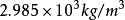
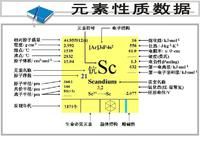
性狀:一種柔軟、銀白色的金屬
摩爾體積:

汽化熱:314.2kJ/mol
熔化熱:14.1kJ/mol
蒸汽壓:22.1Pa(1812K)
聲速:無數據(293.15K)
電負性:1.36(鮑林標度)
比熱容:568J/(kg·K)
電導率:
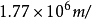 Ω熱導率:15.8W/(m·K)
Ω熱導率:15.8W/(m·K) | 其他性質 | |
|---|---|
| 第一電離能 | 633.1 kJ/mol |
| 第二電離能 | 1235.0 kJ/mol |
| 第三電離能 | 2388.6 kJ/mol |
| 第四電離能 | 7090.6 kJ/mol |
| 第五電離能 | 8843 kJ/mol |
| 第六電離能 | 10679 kJ/mol |
| 第七電離能 | 13310 kJ/mol |
| 第八電離能 | 15250 kJ/mol |
| 第九電離能 | 17370 kJ/mol |
| 第十電離能 | 21726 kJ/mol |
化學性質
鈧(Sc),是銀色的柔軟金屬,被空氣氧化時略帶淺黃色或粉紅色。鈧容易風化和大多數稀酸中緩慢溶解。它不與硝酸(HNO3)和氫氟酸(HF)1:1混合物反應,可能是由於形成了一個不滲透的鈍化層。化合物
鈧可以形成Eb2O3形式的化合物,其比重3.5,鹼性強於氧化鋁,弱於氧化釔和氧化鎂;是否能與氯化銨反應還是疑問。鈧土Sc2O3,其比重3.86,鹼性強於氧化鋁,弱於氧化釔和氧化鎂,與氯化銨不反應。
鹽類無色,與氫氧化鉀和碳酸鈉形成膠體沉澱,各種鹽類均難以完好結晶。鈧鹽無色,與氫氧化鉀和碳酸鈉形成膠體沉澱,硫酸鹽極難結晶。
碳酸鹽不溶於水,可能形成鹼式碳酸鹽沉澱。碳酸鈧不溶於水,並容易脫掉二氧化碳。
硫酸復鹽可能不形成礬。鈧的硫酸復鹽不成礬。
無水氯化物ScCl3揮發性低於氯化鋁,比氯化鎂更容易水解。ScCl3升華溫度850℃,AlCl3則為100℃,在水溶液中水解。
歷史發現
歷史簡介
在1869年,Mendeleev注意到原子質量在鈣(40)和鈦(48)之間有一個間隙,並預言這裡還有一個未被發現的中間級原子質量的元素。他預測其氧化物是X2O3。在1879年發現了它——鈧,由瑞典的烏普薩拉大學的LarsFrederikNilson發現的。他從黑稀金礦中提取了它,一種複雜的礦石,其包含8種金屬氧化物。他已經從黑稀金礦中提取了氧化鉺,並從這個氧化物中他獲得了氧化鐿,且還有另一個更輕元素的氧化物,它的光譜顯示它是一種未知的金屬。這就是Mendeleev預言的金屬,其氧化物為Sc2O3。鈧金屬自身在1937年才由電解熔化的氯化鈧生產出來。詳細內容
在元素化學裡,有一系列性質非常接近的金屬元素被稱為稀土元素。這一系列中包括了十五個鑭系元素--鑭(La)、鈰(Ce)、鐠(Pr)、釹(Nd)、鉕(Pm)、釤(Sm)、銪(Eu)、釓(Gd)、鋱(Tb)、鏑(Dy)、鈥(Ho)、鉺(Er)、銩(Tm)、鐿(Yb)、鑥(Lu);以及和這些同族而性質相似的兩個更輕的元素:鈧(Sc)和釔(Y)。這一系列元素最初是從瑞典產的比較稀少的礦物中發現的,\"土\"是當時對不溶於水的金屬氧化物的統稱,因此得名稀土(Rareearth)。在這十七個元素裡面,鈧的排位是最靠前的,原子序數只有21,不過就發現而言,鈧比他在元素周期表上面的左鄰右舍都要晚了差不多上百年,即使在稀土裡面,鈧的發現也不是較早的,排列在釔、鈰、鑭、鉺、鋱和鐿後面,名列第七。作為最輕的先鋒官,他的出場委實晚了一些。原因很簡單,鈧在地殼裡的含量並不高,只有5*10-6,也就相當於每一噸地殼物質裡面有5克(一小塊德芙朱古力或者大白兔奶糖),不但和其他輕元素相比要低不少,在整個稀土元素中含量也僅屬中等,大概只有他最富裕的兄弟鈰的1/10。另外呢,稀土元素感覺很有點集體領導的意思,他們的礦藏仿佛是在開政治局會議一樣,只要一開會,這一夥元素就往往要全部列席會議,這樣一來,想從混生的礦藏中找到我們的鈧,其實並不容易。不過雖然一直沒被發現,這個元素的存在卻已經有人作出過預言。在門捷列夫1869年給出的第一版元素周期表中,就赫然在鈣的後面留有一個原子量45的空位。後來門捷列夫將鈣之後的元素暫時命名為類硼(Eka-Boron),並給出了這個元素的一些物理化學性質。不過這個預言就像放在漂流瓶中的信箋一樣,暫時被汪洋的學術大海靜靜湮沒了。門捷列夫的預言沒有得到人們的注意,但是在十九世紀晚期,對稀土元素的研究卻成為了一股熱潮。在鈧發現之前一年,瑞士的馬利納克(deMarignac)從玫瑰紅色的鉺土中,通過局部分解硝酸鹽的方式,得到了一種不同於鉺土的白色氧化物,他將這種氧化物命名為鐿土,這就是稀土元素髮現裡面的第六名。當時老馬手頭樣品沒多少了,就建議手頭有充足鉺土的科學家多製備一些鐿土,以研究它的性質。當時瑞典烏潑撒拉大學的尼爾森手頭正好有鉺土的樣品,他就想按照馬利納克的方法將鉺土提純,並精確測量鉺和鐿的原子量(因為他這個時候正在專注於精確測量稀土元素的物理與化學常數以期對元素周期律作出驗證)。當他經過13次局部分解之後,得到了3.5g純淨的鐿土。但是這時候奇怪的事情發生了,馬利納克給出的鐿的原子量是172.5,而尼爾森得到的則只有167.46。尼爾森敏銳地意識到這裡面有可能是什麼輕質的元素魚目混珠進去,才讓這個原子量的測定不再準斤足兩。於是他將得到的鐿土又用相同的流程繼續處理,最後當只剩下十分之一樣品的時候,測得的原子量更是掉到了134.75;同時光譜中還發現了一些新的吸收線。尼爾森的判斷是正確的,因此也就獲得了給孩子起名的權利。他用他的故鄉斯堪的納維亞半島給鈧命名為Scandium。1879年,他正式公布了自己的研究結果,在他的論文中,還提到了鈧鹽和鈧土的很多化學性質。不過在這篇論文中,他沒有能給出鈧的精確原子量,也還不確定鈧在元素周期中的位置。尼爾森的好友,也是同在烏潑撒拉大學任教的克利夫也在一起做這個工作。他從鉺土出發,將鉺土作為大量組分排除掉,再分出鐿土和鈧土之後,又從剩餘物中找到了鈥和銩這兩個新的稀土元素。做為副產物,他提純了鈧土,並進一步了解了鈧的物理和化學性質。這樣一來,門捷列夫放出的漂流瓶沉睡了十年之後,終於被克利夫撈了起來,他認識到,鈧,就是門捷列夫的類硼。我們來看看鈧的一些化學性質和瓶中那張古舊的羊皮紙上寫過的預言是否吻合吧。
Eb不由光譜發現。Sc不由光譜發現。
在那個不但對於元素的電子層結構一無所知(連電子都是1899年才發現的),甚至還有權威如杜馬這樣的化學家對原子論都持懷疑態度。能將一個未發現的元素的性質描述得如此精準,真是讓讀者後背泛起一層隱隱的涼意。
相關人物
門捷列夫(1834-1907)預言了鈧的存在。尼爾森(1840-1899)和克利夫(1840-1905)發現了鈧。
提取方法
在被發現後相當長一段時間裡,因為難於製得,鈧的用途一直沒有表現出來。隨著對稀土元素分離方法的日益改進,如今用於提純鈧的化合物,已經有了相當成熟的工藝流程。因為鈧比起釔和鑭系元素來,氫氧化物的鹼性是最弱的,所以包含了鈧的稀土元素混生礦,經過處理轉入溶液後用氨處理時,氫氧化鈧將首先析出,故套用"分級沉澱"法可比較容易地把它從稀土元素中分離出來。另一種方法是利用硝酸鹽的“分級分解”進行分離,由於硝酸鈧最容易分解,可以達到分離出鈧的目的。另外,在鈾、釷、鎢、錫等礦藏中綜合回收伴生的鈧也是鈧的重要來源之一。獲得了純淨的鈧的化合物之後,將其轉化為ScCl3,與KCl、LiCl共熔,用熔融的鋅作為陰極進行電解,使鈧就會在鋅極上析出,然後將鋅蒸去可以得到金屬鈧。這是一種輕質的銀白色金屬,化學性質也非常活潑,可以和熱水反應生成氫氣。所以圖片中大家看到的金屬鈧被密封在瓶子裡,用氬氣加以保護,否則鈧會很快生成一個暗黃色或者灰色的氧化層,失去那種閃亮的金屬光澤。同位素
鈧(原子質量單位:44.955912(6))共有37個同位素,其中有1個同位素(47Sc)是穩定的。| 符號 | 質子 | 中子 | 質量 | 半衰期 | 核自鏇 | 相對豐度 |
|---|---|---|---|---|---|---|
| 激發能量 | ||||||
| 36Sc | 21 | 15 | 36.01492(54)# | |||
| 37Sc | 21 | 16 | 37.00305(32)# | 7/2-# | ||
| 38Sc | 21 | 17 | 37.99470(32)#鈧元素性質數據 | <300 ns | (2-)# | |
| 39Sc | 21 | 18 | 38.984790(26) | <300 ns | (7/2-)# | |
| 40Sc | 21 | 19 | 39.977967(3) | 182.3(7) ms | 4- | |
| 41Sc | 21 | 20 | 40.96925113(24) | 596.3(17) ms | 7/2- | |
| 42Sc | 21 | 21 | 41.96551643(29) | 681.3(7) ms | 0+ | |
| 43Sc | 21 | 22 | 42.9611507(20) | 3.891(12) h | 7/2- | |
| 44Sc | 21 | 23 | 43.9594028(19) | 3.97(4) h | 2+ | |
| 45Sc | 21 | 24 | 44.9559119(9) | 穩定 | 7/2- | 1.0000 |
| 46Sc | 21 | 25 | 45.9551719(9) | 83.79(4) d | 4+ | |
| 47Sc | 21 | 26 | 46.9524075(22) | 3.3492(6) d | 7/2- | |
| 48Sc | 21 | 27 | 47.952231(6) | 43.67(9) h | 6+ | |
| 49Sc | 21 | 28 | 48.950024(4) | 57.2(2) min | 7/2- | |
| 50Sc | 21 | 29 | 49.952188(17) | 102.5(5) s | 5+ | |
| 51Sc | 21 | 30 | 50.953603(22) | 12.4(1) s | (7/2)- | |
| 52Sc | 21 | 31 | 51.95668(21) | 8.2(2) s | 3(+) | |
| 53Sc | 21 | 32 | 52.95961(32)# | >3 s | (7/2-)# | |
| 54Sc | 21 | 33 | 53.96326(40) | 260(30) ms | 3+# | |
| 55Sc | 21 | 34 | 54.96824(79) | 0.115(15) s | 7/2-# | |
| 56Sc | 21 | 35 | 55.97287(75)# | 35(5) ms | (1+) | |
| 57Sc | 21 | 36 | 56.97779(75)# | 13(4) ms | 7/2-# | |
| 58Sc | 21 | 37 | 57.98371(86)# | 12(5) ms | (3+)# | |
| 59Sc | 21 | 38 | 58.98922(97)# | 10# ms | 7/2-# | |
| 60Sc | 21 | 39 | 59.99571(97)# | 3# ms | 3+# | |
現代套用
備註:畫上#號的數據代表沒有經過實驗的證明,只是理論推測而已,而用括弧括起來的代表數據不確定性。照明
比較有趣的是,鈧的用途(作為主要工作物質,而不是用於摻雜的)都集中在很光明的方向,稱他為光明之子也不為過。鈧的第一件法寶叫做鈧鈉燈,可以用來給千家萬戶帶來光明。這是一種金屬鹵化物電光源:在燈泡中充入碘化鈉和碘化鈧,同時加入鈧和鈉箔,在高壓放電時,鈧離子和鈉離子分別發出他們的特徵發射波長的光,鈉的譜線為589.0和589.6nm兩條著名的黃色光線,而鈧的譜線為361.3~424.7nm的一系列近紫外和藍色光發射,因為互為補色,產生的總體光色就是白色光。正是由於鈧鈉燈具有發光效率高、光色好、節電、使用壽命長和破霧能力強等特點,使其可廣泛用於電視攝像和廣場、體育館、馬路照明,被稱為第三代光源。在中國這種燈還是作為新技術被逐漸推廣的,而在一些已開發國家,這種燈早在80年代初就被廣泛使用了。
 鈧用途
鈧用途他的第三件法寶叫做γ射線源,這個法寶自己就能大放光明,不過這種光亮我們肉眼接收不到,是高能的光子流。我們平常從礦物中提煉出來的是45Sc,這是鈧的唯一一種天然同位素,每一個45Sc的原子核中有21個質子和24箇中子。倘若我們像把猴子放到太上老君的煉丹爐中煉上七七四十九天一樣將鈧放在核反應堆中,讓他吸收中子輻射,原子核中多一個中子的46Sc就誕生了。46Sc這種人工放射性同位素可以當作γ射線源或者示蹤原子,還可以用來對惡性腫瘤進行放射治療。還有像釔鎵鈧石榴石雷射器,氟化鈧玻璃紅外光導纖維,電視機上鈧塗層的陰極射線管之類的用途簡直不知凡幾,看來鈧生來就和光明有緣呢。
神奇調料
上面說了鈧的一些套用,不過,因為價格高昂,考慮到成本在工業產品里很少會用到很大數量鈧和鈧的化合物,都是像燈泡里那樣薄薄的一層鈧箔之類的用法。而在更多一些領域,鈧和鈧的化合物更是被作為神奇的調料使用,好像大廚手中的鹽、糖或味素,只需要一星半點,就有畫龍點睛的作用。
套用領域
在無機化學裡,摻雜是一個非常重要的手段。在一個作為基體的晶體結構中摻入少量的其他化合物,因為被摻雜物質在化學性質上和原有基體的不同,晶格結構會出現各種各樣的變化和缺陷,從而或者提升原有基體的性質,或者增添原來不具有的活性。比如大家最耳熟能詳的P型和N型半導體原料,就是分別在導通能力很差的單晶矽裡面,添加了因為缺少價電子導致空穴的硼,和因為富餘價電子而產生自由電子的磷獲得的。我們的鈧也是一個重要的摻雜原料,很多材料就是因為摻入了鈧獲得了意料之外的性質。[6]單質形式的鈧,已經被大量套用於鋁合金的摻雜。在鋁中只要加入千分之幾的鈧就會生成Al3Sc新相,對鋁合金起變質作用,使合金的結構和性能發生明顯變化。加入0.2%~0.4%的Sc(這個比例也真的和家裡炒菜放鹽的比例差不多,只需要那么一點)可使合金的再結晶溫度提高150~200℃,且高溫強度、結構穩定性、焊接性能和抗腐蝕性能均明顯提高,並可避免高溫下長期工作時易產生的脆化現象。高強高韌鋁合金、新型高強耐蝕可焊鋁合金、新型高溫鋁合金、高強度抗中子輻 鈧合金
鈧合金 金屬鈧
金屬鈧從尼爾森注意到原子量數據的虧欠到今天,鈧進入人們的視野不過一百年二十多年,卻差不多坐了一百年的冷板凳,直到上個世紀後期材料科學的蓬勃發展才給他帶來了生機。到今天,連同鈧在內的稀土元素都已經成為了材料科學中炙手可熱的明星,在成千上萬的體系中發揮著千變萬化的作用,每天都在給我們的生活帶來多一點的便利,創造的經濟價值更是難以計量。按陰陽五行的說法,土生金,其信然乎?
人體影響
鈧單質被認為是無毒。鈧化合物的動物試驗已經完成,氯化鈧的半數致死量已被確定為4毫克/公斤腹腔和755毫克/千克口服給藥。從這些結果看來鈧化合物應處理為中度毒性化合物。相關詞條
化學元素周期表
| 族→ | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 電子層 | 0族電子數 | |
| 周期↓ | I A | 0 | |||||||||||||||||||
| 1 | 1 H 氫 | 2 He 氦 | K | 2 | |||||||||||||||||
| II A | III A | IV A | V A | VI A | VII A | ||||||||||||||||
| 2 | 3 Li 鋰 | 4 Be 鈹 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 | L K | 8 2 | |||||||||||
| 3 | 11 Na 鈉 | 12 Mg 鎂 | 13 Al 鋁 | 14 Si 矽 | 15 P 磷 | 16 S 硫 | 17 Cl 氯 | 18 Ar 氬 | M L K | 8 8 2 | |||||||||||
| III B | IV B | V B | VI B | VII B | VIII | I B | II B | ||||||||||||||
| 4 | 19 K 鉀 | 20 Ca 鈣 | 21 Sc 鈧 | 22 Ti 鈦 | 23 V 釩 | 24 Cr 鉻 | 25 Mn 錳 | 26 Fe 鐵 | 27 Co 鈷 | 28 Ni 鎳 | 29 Cu 銅 | 30 Zn 鋅 | 31 Ga 鎵 | 32 Ge 鍺 | 33 As 砷 | 34 Se 硒 | 35 Br 溴 | 36 Kr 氪 | N M L K | 8 18 8 2 | |
| 5 | 37 Rb 銣 | 38 Sr 鍶 | 39 Y 釔 | 40 Zr 鋯 | 41 Nb 鈮 | 42 Mo 鉬 | 43 Tc 鎝 | 44 Ru 釕 | 45 Rh 銠 | 46 Pd 鈀 | 47 Ag 銀 | 48 Cd 鎘 | 49 In 銦 | 50 Sn 錫 | 51 Sb 銻 | 52 Te 碲 | 53 I 碘 | 54 Xe 氙 | O N M L K | 8 18 18 8 2 | |
| 6 | 55 Cs 銫 | 56 Ba 鋇 | 57- 71 鑭系 | 72 Hf 鉿 | 73 Ta 鉭 | 74 W 鎢 | 75 Re 錸 | 76 Os 鋨 | 77 Ir 銥 | 78 Pt 鉑 | 79 Au 金 | 80 Hg 汞 | 81 Tl 鉈 | 82 Pb 鉛 | 83 Bi 鉍 | 84 Po 釙 | 85 At 砹 | 86 Rn 氡 | P O N M L K | 8 18 32 18 8 2 | |
| 7 | 87 Fr 鍅 | 88 Ra 鐳 | 89- 103 錒 | 104 Rf 鑪 | 105 Db | 106 Sg | 107 Bh | 108 Hs | 109 Mt | 110 Ds 鐽 | 111 Rg 錀 | 112 Uub | 113 Uut | 114 Uuq | 115 Uup | 116 Uuh | 117 Uus | 118 Uuo | |||
| 鑭系元 素 | 57 La 鑭 | 58 Ce 鈰 | 59 Pr 鐠 | 60 Nd 釹 | 61 Pm 鉕 | 62 Sm 釤 | 63 Eu 銪 | 64 Gd 釓 | 65 Tb 鋱 | 66 Dy 鏑 | 67 Ho 鈥 | 68 Er 鉺 | 69 Tm 銩 | 70 Yb 鐿 | 71 Lu 鑥 | ||||||
| 錒系元 素 | 89 Ac 錒 | 90 Th 釷 | 91 Pa 鏷 | 92 U 鈾 | 93 Np 鎿 | 94 Pu 鈽 | 95 Am 鎇 | 96 Cm 鋦 | 97 Bk 錇 | 98 Cf 鐦 | 99 Es 鑀 | 100 Fm 鐨 | 101 Md 鍆 | 102 No 鍩 | 103 Lr 鐒 | ||||||
化學與物理術語(一)
| 通過對化學和物理的了解,來明白生活中的細節,從而使我們更好的明白一些事物。 |

