基本概述
 糖元
糖元由於人的進食時間是間斷的,食後血糖升高,必須貯存一定量糖以備不進食時的生理需要。糖元是糖的貯存形式,進食後過多的糖可在肝臟和肌肉等組織中合成糖元貯存起來,以免血糖濃度過高。肝糖元不僅可以從葡萄糖、果糖和半乳糖生成,還可以從甘油、乳酸和某些胺基酸等非糖物質合成。肝糖元可調節血糖濃度,當血糖高時,可在肝臟合成肝糖元;血糖低時,肝糖元則分解成葡萄糖以補充血糖,因此肝糖元對維持血糖的相對恆定十分重要。但肌糖元只能由葡萄糖生成,而不能直接分解為血糖。當肌肉活動劇烈時,肌糖元分解產生大量乳酸,除一部分可氧化供能外,大部分隨血液循環到肝臟,通過糖異生轉變成肝糖元或血糖。血糖經血循環送到肌肉等組織氧化或合成肌糖元貯存。這種肌糖元→血乳酸→肝糖元→血糖→肌糖元的循環過程,又稱乳酸循環。
異生作用
 糖元
糖元肝臟是進行糖異生的主要器官,糖異生作用是飢餓時從非糖類物質供給糖的途徑,此時肝外組織脂肪動員增加,肌肉組織蛋白質分解加強,它們的分解產物進入肝臟,通過糖元異生作用,就能維持飢餓時的血糖濃度;肌肉激烈運動產生的大量乳酸進入肝臟經糖元異生作用轉變為糖元或葡萄糖,不僅能節約糖而且可防止乳酸積聚影響機體的酸鹼平衡;由於某些胺基酸脫氨基產生的酮酸可通過糖元異生作用轉變為糖,因此糖異生作用,也有利於胺基酸的分解代謝。
生物合成
 糖元
糖元由葡萄糖(包括少量果糖和半乳糖)合成糖原的過程稱為糖原合成,反應在細胞質中進行,需要消耗ATP和UTP。
糖原合成酶催化的糖原合成反應不能從頭開始合成第一個糖分子,需要至少含4個葡萄糖殘基的α-1,4-多聚葡萄糖作為引
 糖元
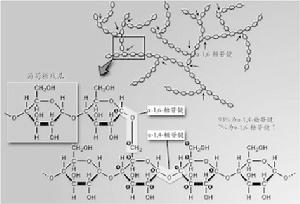
糖元物(primer),在其非還原性末端與UDPG反應,UDPG上的葡萄糖基C1與糖原分子非還原末端C4形成α-1,4-糖苷鏈,使糖原增加一個葡萄糖單位,UDPG是活潑葡萄糖基的供體,其生成過程中消耗UTP,故糖原合成是耗能過程,糖原合成酶只能促成α-1,4-糖苷鍵,因此該酶催化反應生成為α-1,4-糖苷鍵相連構成的直鏈多糖分子如澱粉。
機體記憶體在一種特殊蛋白質稱為glycogenin,可做為葡萄糖基的受體,從頭開始如合成第一個糖原分子的葡萄糖,催化此反應的酶是糖原起始合成酶(glycogeninitiaorsynthase),進而合成一寡糖鏈作為引物,再繼續由糖原合成酶催化合成糖。同時糖原分枝鏈的生成需分枝酶(branchingenzyme)催化,將5-8個葡萄糖殘基寡糖直鏈轉到另一糖原子上以α-1.6-糖苷鍵相連,生成分枝糖鏈,在其非還原性末端可繼續由糖原合成酶催化進行糖鏈的延長。多分枝增加糖原水溶性有利於其貯存,同時在糖原分解時可從多個非還原性末端同時開始,提高分解速度。
機體分解
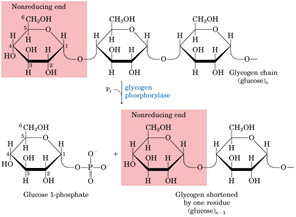
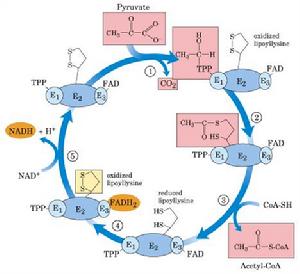 糖元
糖元將糖原中1個糖基轉變為1分子葡萄糖,但是磷酸化酶只作用於糖原上的α(1→4)糖苷鍵,並且催化至距α(1→6)糖苷鍵4個葡萄糖殘基時就不再起作用,這時就要有脫枝酶(debranchingenzyme)的參與才可將糖原完全分解。
脫枝酶是一種雙功能酶,它催化糖原脫枝的兩個反應,第一種功能是4-α-葡聚糖基轉移酶(4-α-D-glucanotrnsferase)活性,即將糖原上四葡聚糖分枝鏈上的三葡聚糖基轉移到酶蛋白上,然後再交給同一糖原分子或相鄰糖原分子末端具自由4羥基的葡萄糖殘基上,生成α(1→4)糖苷鍵,結果直鏈延長3個葡萄糖,而α(1→6)分枝處只留下1個葡萄糖殘基,在脫枝酶的另一功能,即1,6-葡萄糖苷酶活性催化下,這個葡萄糖基被水解脫下,為游離的葡萄糖,在磷酸化酶與脫枝酶的協同和反覆的作用下,糖原可以完全磷酸化和水解。
代謝調節
 糖元
糖元(一)糖原代謝的別構調節
6-磷酸葡萄糖可激活糖原合成酶,刺激糖原合成,同時,抑制糖原磷酸化酶阻止糖原分解,ATP和葡萄糖也是糖原磷酸化酶抑制劑,高濃度AMP可激活無活性的糖原磷酸化酶b使之產生活性,加速糖原分解。Ca2+可激活磷酸化酶激酶進而激活磷酸化酶,促進糖原分解。
(二)激素的調節
體內腎上腺素和胰高血糖素可通過cAMP連鎖酶促反應逐級放大,構成一個調節糖原合成與分解的控制系統。
當機體受到某些因素影響,如血糖濃度下降和劇烈活動時,促進腎上腺素和胰高血糖素分泌增加,這兩種激素與肝或肌肉等組織細胞膜受體結合,由G蛋白介導活化腺苷酸環化酶,使cAMP生成增加,cAMP又使cAMP依賴蛋白激酶(cAMpdependentproteinkinase)活化,活化的蛋白激酶一方面使有活性的糖原合成酶a磷酸化為無活性的糖原合成酶b;另一面使無活性的磷酸化酶激酶磷酸化為有活性的磷酸化酶激酶,活化的磷酸化酶激酶進一步使無活性的糖原磷酸化酶b磷酸化轉變為有活性的糖原磷酸化酶a,最終結果是抑制糖原生成,促進糖原分解,使肝糖原分解為葡萄糖釋放入血,使血糖濃度升高,肌糖原分解用於肌肉收縮。
肝糖元
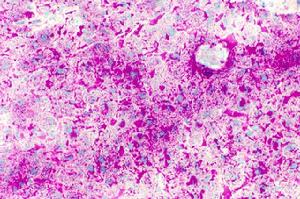 糖元
糖元糖元遇碘液程紅棕色。主要生物學功能是作為動物和細菌的能量儲存物質。人體主要儲存在肝臟和肌肉中。葡萄糖聚合物以糖原的形式儲存於肝臟,當機體需要時,便可分解成葡萄糖,轉化為能量。一般肝中糖原含量約100克。
肝糖元的生成來源有:①食物在飯後由腸道消化吸收入血液,葡萄糖、果糖、乳糖被輸入肝臟,有60%~70%轉化為糖原儲存起來。②空腹時糖原異生增加,即蛋白質分解成胺基酸,脂肪分解成甘油在肝臟轉化成糖原;肌肉收縮生成的乳酸,通過肝臟的代謝,亦可能轉化為肌糖元。正常飲食能使肝糖原不斷得到補充,以減少糖原異生作用,同時體內蛋白質亦可得到較好的保存。應該是飯後1——2小時開始分解。
血糖來源
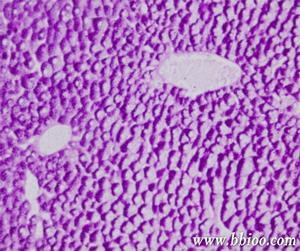 糖元
糖元①食物中的糖類(如澱粉、蔗糖等)經過消化道的消化吸收,使血糖濃度上升,一般飯後約1小時最高正常人也僅達150mg/dL。而後血糖又迅速降低。在2~3小時即降至正常水平。
②肝糖元分解為葡萄糖進入血液可升高血糖濃度,條件是血糖含量降低時;當血糖含量升高時,多餘的血糖又可合成肝糖元貯存起來。
③甘油、胺基酸、乳酸等非糖物質可以在血糖濃度降低時、貯存的肝糖元被分解減少時,轉化為糖類物質(這一過程也稱為“糖的異生”)
(2)血糖的主要去路有以下三條途徑:
①在細胞質基質和線粒體中通過呼吸作用將血糖氧化分解得到CQ2、H2O和能量,若在缺氧條件下則進行無氧呼吸生成乳酸和能量,為生命活動提供能量。
②當血糖濃度升高時,多餘的糖元可轉變為肝糖元將能量暫時儲備起來,也可以合成肌糖元,供給人肌肉活動需要。
③合成糖元後剩餘的血糖可轉變為脂肪;還可以在轉氨酶的催化作用下轉變為非必需的胺基酸,即並不是必須從食物中獲得的胺基酸種類。
積累症狀
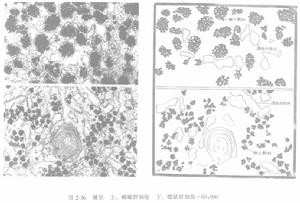 糖元
糖元糖原累積症是指組織中糖原過多的一組疾病,有多種類型,由遺傳性酶的缺陷或糖原結構異常所致。
治療措施
1、糖原累積症Ⅲ型
高蛋白飲食可改善生長發育狀態和肌力,但最近研究認為高澱粉、標準蛋白飲食效果好。
2、糖原累積症Ⅳ型
無特效療法,高蛋白低糖飲食,加食玉米油未能阻止肝硬化進程。用純化的葡萄糖素未能取得肯定效果。麴黴菌屬提取物可使肝糖原急劇減少,因而是一有研究前途的治療方法。此外,可施行肝移植。
病因學
1、糖原累積症Ⅲ型 病因為肝和肌肉內澱粉-1,6-葡萄糖苷酶(脫支酶)缺陷,糖原由磷酸化酶分解後,不能進一步徹底分解為葡萄糖。
2、糖原累積症Ⅳ型 由於澱粉-(1,4-1,6)-轉葡萄糖苷酶(分支酶)缺陷所致。所積貯的糖原結構異常,外鏈長、分支減少,結構似支鏈澱粉,故又稱支鏈澱粉病。所積貯的異常糖原溶解度遠低於正常糖原。本病罕見,為常染色體隱性遺傳,雜合子的成纖維細胞內有分子酶缺陷。
 糖元
糖元糖原累積症至少分成12種類型之多,其中0型(糖原合成障礙)和Ⅳ型(澱粉-1-4,1-6轉葡萄糖苷酶缺乏),都會導致肝硬化和肝功能衰竭。Ⅰ型(葡萄糖-6-磷酸酶缺乏)可發展為良性肝腺瘤和腺癌,Ⅲ型(澱粉-1,6-葡萄糖苷酶缺乏、脫支酶缺乏)可發展為肝纖維化或肝硬化。
病理改變
1、糖原累積症Ⅲ型 本型有①肝內纖維隔;②無脂肪沉積,此兩點與GSD-Ⅰ不同。GSD-Ⅲ型,肝硬化往往發生在兩個酶以上同時缺陷,即除脫支酶缺陷外,還有磷酸酶和/或磷酸激酶的缺陷。與GSD-Ⅰ比較,GSD-Ⅲ超微結構示脂肪滴小且少。除肝臟病變外,肌肉也有糖原累積。
2、糖原累積症Ⅳ型 本型肝臟呈小結節性肝硬化伴有寬纖維束圍繞或插入肝小葉。門脈區膽管輕度增生。白色的兩染性物質或嗜鹼性染色物質沉積在肝細胞、心肌、骨骼肌和腦細胞。肝小葉周邊細胞內可發現嗜酸性或無色包涵體沉積在細胞漿,把肝細胞核推向一側,構成了GSD-Ⅳ的特徵性病變。組織化學染色顯示肝細胞內沉積物系異常糖原。
臨床表現
1、糖原累積症Ⅲ型
體檢檢查本身難與GSD-Ⅰ型區別。嬰兒期肝腫大、發育障礙較突出,部分患兒在4~6歲時可出現脾腫大,此患兒可有肝纖維化的證據,但不一定發展為肝硬化和肝功能衰竭。
除肝病變外,大部分有肌無力,尤其疾走和爬山時,但不會發生肌肉痙攣。部分患者有肌肉萎縮。糖原可累積在心臟,出現心臟增大。心電圖有非特異性變化,但不發生心力衰竭和心律失常,腎臟不大。
低血糖較GSD-Ⅰ輕,青春期時肝臟有縮小趨勢,只有伴有磷酸酶或磷酸酶缺乏者才會走向肝硬化。
2、糖原累積症Ⅳ型
嬰兒出生後幾個月多無症狀,一歲內症狀隱匿,但最早出現症狀可在3個月時,最晚是15個月。可有一些非特異性消化道症狀,肝、脾腫大,肝功能不全生長遲緩等症狀和體徵,肌肉張力低、萎縮。隨病情發展可有腹壁靜脈曲張、肝硬化門脈高壓、腹水和食道靜脈曲張,該病診斷後存活期多為2~37個月,偶3~4年,最後多死於慢性肝功能不全、上消化道出血、心力衰竭、感染。
輔助檢查
1、糖原累積症Ⅲ型
本型血脂升高,程度與血糖降低程度相關,但血脂升高幅度較GSD-Ⅰ小。少數患者有尿酸輕度升高,血清轉氨酶升高(300~600IU)。
半乳糖、蔗糖、胺基酸和蛋白質轉變為糖的過程正常,因而些食物可使血糖升高。空腹腎上腺素或胰高糖素反應差,若進食數小時後再作腎上腺或胰高糖素試驗則反應正常。
2、糖原累積症Ⅳ型
血清轉氨酶和鹼性磷酸酶升高,晚期膽固醇輕度升高,在肝功能衰竭發生後,可有一系列變化如低蛋白血症,膽紅素升高,球蛋白升高及血氨變化。胰高糖素、腎上腺素耐量試驗血糖呈陽性反應,使血糖升高0.83mmlo/L至1.28mmol/L。高峰出現在注藥後30min。口服葡萄糖和蔗糖耐量試驗都正常。血清乳酸和丙酮酸正常。
相關詞條
人體探秘(一)
| 人作為世界上最高級的動物,小小的身軀里包含了無數的秘密,我們要通過科學來了解自己的身體,才能更好的開發運用和保護自己的身體。 |
