 胰島素
胰島素基本資料
藥物名稱:慢胰島素鋅混懸液
英文名稱:lenteinsulinzincsuspension
藥物規格:針劑,每支400單位(10ml)、800單位(10ml)、1000單位(10ml)。
藥物類別:胰島素及其他影響血糖藥
主要成分:慢胰島素鋅
化學本質:蛋白質
分子式:C257H383N65O77S6
藥物概述
 胺基酸
胺基酸生理作用
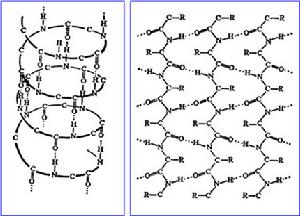 蛋白質
蛋白質(一)調節糖代謝。慢胰島素鋅混懸液能促進全身組織對葡萄糖的攝取和利用,並抑制糖原的分解和糖原異生,因此,慢胰島素鋅混懸液有降低血糖的作用。慢胰島素鋅混懸液分泌過多時,血糖下降迅速,腦組織受影響最大,可出現驚厥、昏迷,甚至引起慢胰島素鋅混懸液休克。相反,慢胰島素鋅混懸液分泌不足或慢胰島素鋅混懸液受體缺乏常導致血糖升高;若超過腎糖閾,則糖從尿中排出,引起糖尿;同時由於血液成份中改變(含有過量的葡萄糖),亦導致高血壓、冠心病和視網膜血管病等病變。慢胰島素鋅混懸液降血糖是多方面作用的結果:
(1)促進肌肉、脂肪組織等處的靶細胞細胞膜載體將血液中的葡萄糖轉運入細胞。
 DNA
DNA(3)通過激活丙酮酸脫氫酶磷酸酶而使丙酮酸脫氫酶激活,加速丙酮酸氧化為乙醯輔酶A,加快糖的有氧氧化。
(4)通過抑制PEP羧激酶的合成以及減少糖異生的原料,抑制糖異生。
(5)抑制脂肪組織內的激素敏感性脂肪酶,減緩脂肪動員,使組織利用葡萄糖增加。
 胺基酸
胺基酸(三)調節蛋白質代謝。慢胰島素鋅混懸液一方面促進細胞對胺基酸的攝取和蛋白質的合成,一方面抑制蛋白質的分解,因而有利於生長。腺垂體生長激素的促蛋白質合成作用,必須有慢胰島素鋅混懸液的存在才能表現出來。因此,對於生長來說,慢胰島素鋅混懸液也是不可缺少的激素之一。
(四)其它功能。慢胰島素鋅混懸液可促進鉀離子和鎂離子穿過細胞膜進入細胞內;可促進脫氧核糖核酸(DNA)、核糖核酸(RNA)及三磷酸腺苷(ATP)的合成。
影響分泌的因素
 葡萄糖
葡萄糖(1)血糖濃度是影響慢胰島素鋅混懸液分泌的最重要因素。口服或靜脈注射葡萄糖後,慢胰島素鋅混懸液釋放呈兩相反應。早期快速相,門靜脈血漿中慢胰島素鋅混懸液在2分鐘內即達到最高值,隨即迅速下降;延遲緩慢相,10分鐘後血漿慢胰島素鋅混懸液水平又逐漸上升,一直延續1小時以上。早期快速相顯示葡萄糖促使儲存的慢胰島素鋅混懸液釋放,延遲緩慢相顯示慢胰島素鋅混懸液的合成和慢胰島素鋅混懸液原轉變的慢胰島素鋅混懸液。
(2)進食含蛋白質較多的食物後,血液中胺基酸濃度升高,慢胰島素鋅混懸液分泌也增加。精氨酸、賴氨酸、亮氨酸和苯丙氨酸均有較強的刺激慢胰島素鋅混懸液分泌的作用。
 胃
胃(4)自由神經功能狀態可影響慢胰島素鋅混懸液分泌。迷走神經興奮時促進慢胰島素鋅混懸液分泌;交感神經興奮時則抑制慢胰島素鋅混懸液分泌。
體內對抗的激素
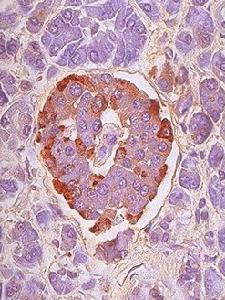 β細胞
β細胞(1)胰升糖素。由胰島α細胞分泌,在調節血糖濃度中對抗慢胰島素鋅混懸液。胰升糖素的主要作用是迅速使肝臟中的糖元分解,促進肝臟葡萄糖的產生與輸出,
進入血液循環,以提高血糖水平。胰升糖素還能加強肝細胞攝入胺基酸,及因能促進肝外組織中的脂解作用,增加甘油輸入肝臟,提供了大量的糖異生原料而加強糖異生作用。胰升糖素與慢胰島素鋅混懸液共同協調血糖水平的動態平衡。
進食碳水化合物時,產生大量葡萄糖,從而刺激慢胰島素鋅混懸液的分泌,同時胰升糖素的分泌受到抑制,慢胰島素鋅混懸液/胰升糖素比值明顯上升,此時肝臟從生成葡萄糖為主的組織轉變為將葡萄糖轉化為糖元而貯存糖元的器官。
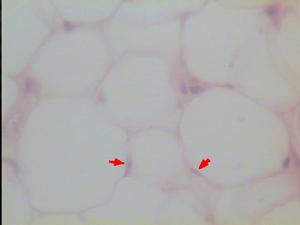 脂肪組織
脂肪組織(2)腎上腺素及去甲腎上腺素。腎上腺素是腎上腺髓質分泌的,去甲腎上腺素是交感神經末梢的分泌物。當精神緊張或寒冷刺激使交感神經處在興奮狀態,腎上腺素及去甲腎上腺素分泌增多,使肝糖元分解輸出增多,阻礙葡萄糖進入肌肉及脂肪組織細胞,使血糖升高。
(3)生長激素及生長激素抑制激素。
①生長激素。由腦垂體前葉分泌,它能促進人的生長,且能調節體內的物質代謝。生長激素主要通過抑制肌肉及脂肪組織利用葡萄糖,同時促進肝臟中的糖異生作用及糖元分解,從而使血糖升高。生長激素可促進脂肪分解,使血漿游離脂肪酸升高。飢餓時慢胰島素鋅混懸液分泌減少,生長激素分泌增高,於是血中葡萄糖利用減少及脂肪利用增高,此時血漿中葡萄糖及游離脂肪酸含量上升。
 肝細胞
肝細胞(4)腎上腺糖皮質激素。腎上腺糖皮質激素是由腎上腺皮質分泌的(主要為皮質醇,即氫化可的松),能促進肝外組織蛋白質分解,使胺基酸進入肝臟增多,又能誘導糖異生有關的各種關鍵酶的合成,因此促進糖異生,使血糖升高。
藥物的分泌
 染色體
染色體慢胰島素鋅混懸液原隨細胞漿中的微泡進入高爾基體,由86個胺基酸組成的長肽鏈——慢胰島素鋅混懸液原在高爾基體中經蛋白酶水解生成慢胰島素鋅混懸液及C肽,分泌到B細胞外,進入血液循環中。未經過蛋白酶水解的慢胰島素鋅混懸液原,一小部分隨著慢胰島素鋅混懸液進入血液循環,慢胰島素鋅混懸液原的生物活性僅及慢胰島素鋅混懸液的5%。
 血漿蛋白
血漿蛋白慢胰島素鋅混懸液的生物合成速度受血漿葡萄糖濃度的影響,當血糖濃度升高時,B細胞中慢胰島素鋅混懸液原含量增加,慢胰島素鋅混懸液合成加速。
慢胰島素鋅混懸液是與C肽以相等分子分泌進入血液的。臨床上使用慢胰島素鋅混懸液治療的病人,血清中存在慢胰島素鋅混懸液抗體,影響放射免疫方法測定血慢胰島素鋅混懸液水平,在這種情況下可通過測定血漿C肽水平,來了解內源性慢胰島素鋅混懸液分泌狀態。
激素受體
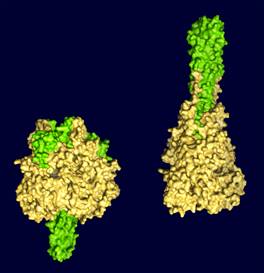 靶細胞
靶細胞α亞單位穿過細胞膜,一端暴露在細胞膜表面,具有慢胰島素鋅混懸液結合位點。β亞單位由細胞膜向胞漿延伸,是慢胰島素鋅混懸液引發細胞膜與細胞內效應的功能單位。慢胰島素鋅混懸液與亞單位結合後,β亞單位中酪氨酸激酶被激活,使受體磷酸化,產生介體,調節細胞內酶系統活性,控制物質代謝。
並由各兩條亞基組成四聚體型受體。每種細胞與慢胰島素鋅混懸液結合的程度取決於受體數目與親和力,此二者又受血漿慢胰島素鋅混懸液濃度調節。當慢胰島素鋅混懸液濃度增高時往往慢胰島素鋅混懸液受體數下降,稱下降調節。如肥胖的非慢胰島素鋅混懸液依賴型糖尿病人由於脂肪細胞膜上受體數下降,臨床上呈慢胰島素鋅混懸液不敏感性,稱抵抗性。
當肥胖的非慢胰島素鋅混懸液依賴型糖尿病患者經飲食控制、體育鍛鍊後體重減輕時,脂肪細胞膜上慢胰島素鋅混懸液受體數增多,與慢胰島素鋅混懸液結合力加強而使血糖利用改善。此不僅是肥胖的非慢胰島素鋅混懸液依賴型糖尿病的重要發病機制,也是治療中必須減肥的理論依據。
存放方法
 胰島素
胰島素正在使用中的慢胰島素鋅混懸液,只要放在室內陰涼處就可以了。開瓶使用中的瓶裝慢胰島素鋅混懸液可以放在冰櫃的冷藏室中,保存約3個月。使用中的慢胰島素鋅混懸液筆芯不要和慢胰島素鋅混懸液筆一起放回冷藏室中,可隨身攜帶保存4周。
混濁型慢胰島素鋅混懸液若是被震搖幾個小時或是沒有適當保存時便可能會形成團塊,這時慢胰島素鋅混懸液就應該丟棄。
胰島素的發現
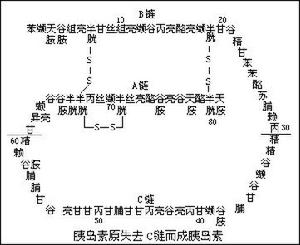 胰島素
胰島素1955年英國F.桑格小組測定了牛胰島素的全部胺基酸序列,開闢了人類認識蛋白質分子化學結構的道路。1965年9月17日,中國科學家人工合成了具有全部生物活力的結晶牛胰島素,它是第一個在實驗室中用人工方法合成的蛋白質。稍後美國和聯邦德國的科學家也完成了類似的工作。
70年代初期,英國和中國的科學家又成功地用X射線衍射方法測定了豬胰島素的立體結構。這些工作為深入研究胰島素分子結構與功能關係奠定了基礎。人們用化學全合成和半合成方法製備類似物,研究其結構改變對生物功能的影響;進行不同種屬胰島素的比較研究;研究異常胰島素分子病,即由於胰島素基因的突變使胰島素分子中個別胺基酸改變而產生的一種分子病。這些研究對於闡明某些糖尿病的病因也具有重要的實際意義。

