 遺傳性黏多糖貯積症
遺傳性黏多糖貯積症病症概念
 遺傳性黏多糖貯積症
遺傳性黏多糖貯積症症狀體徵
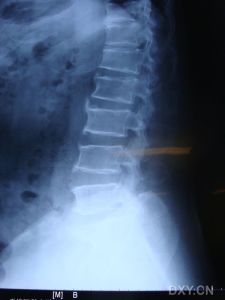
 軟骨病
軟骨病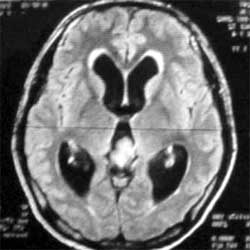 腦積水
腦積水疾病病因
 遺傳性黏多糖貯積症
遺傳性黏多糖貯積症2.黏多糖貯積症Ⅱ型(Hunter綜合徵)為伴性(X)連鎖遺傳性疾病,僅見於男性,由於體內缺乏艾杜糖醛酸硫酸酶而患病,臨床表現與X線檢查同MPS-1,但其臨床進展慢於前者,臨床表現輕於前者,該型根據臨床表現輕重,又分2個亞型是:①MPSⅡA,又稱重症型;②MPSⅡB,又稱輕症型。
3.黏多糖貯積症Ⅲ型(Sanfilippo綜合徵)舊稱營養不良性智力發育不全(polydystrophicoligophrenia),為常染色體隱性遺傳性疾病,體內多種酶缺乏,特徵性臨床表現為進行性智力低下,其他如面貌、身材改變,嚴重程度不一。根據缺乏酶的不同和臨床表現的差異等,又可分4個亞型,即MPSⅢA、MPSⅢB、MPSⅢC和MPSⅢD。
4.黏多糖貯積症Ⅳ型(Morquio綜合徵)為較多見的黏多糖貯積症,屬常染色體隱性遺傳。臨床表現較獨特。本型分2個亞型: (1)MPSⅣA型,其相關缺乏酶為N-乙醯-半乳糖氨糖-6-硫酸鹽硫酸酯酶(N-acetyl-galactosamine-6-sulfatesulfatase)。 (2)MPSⅣB型,缺乏酶為β-半乳糖苷酶(bata-galactosidase)。該2個亞型,臨床表現嚴重程度上可差異較大,通常A型病情較嚴重。
5.黏多糖貯積症Ⅴ型現認為該型即為黏多糖貯積症Ⅰ型的Seheie型,與Hrular綜合徵不同之處表現為無嚴重的角膜混濁,且混濁為周邊性,患者智力正常,身材正常或稍矮,壽命基本正常,但有多毛,關節強直。背柱、頭顱X線示僅有輕微改變。
6.黏多糖貯積症Ⅵ型(Maroteaux-Lamy綜合徵)或稱芳基硫酸酯酶B缺乏症(anglsulfataseBdeficiency)。為常染色體隱性遺傳疾病,缺乏酶即為芳基硫酸酯酶。本型與Hurler綜合徵基本相似,但智力正常,與Hurler不同者為部分病人尚有骨骺,尤其是股骨頭骺後缺血壞死樣改變可存在。該症預後較MPSⅠ綜合徵壽命長。與Hurler鑑別診斷主要根據壽限較長,智力基本正常,及骨骺可存在Hurler尿中硫酸皮膚素及硫酸肝素均增多,而Ⅵ型僅後者增多。在缺乏酶方面Ⅰ型缺α-L-艾杜糖醛酶,Ⅵ型缺芳基硫酸酯酶B。
7.黏多糖貯積症Ⅶ型(Sly綜合徵)為常染色體隱性遺傳病,極罕見,患者缺乏β-葡萄糖醛酸酶(β-glucuronidase),患者嬰兒期即見身材矮小,智力遲鈍,雞胸,背柱側彎等。本症分重症和輕症2個亞型,前者發病早,並有關節攣縮,後者發病晚,常有股骨頭缺血壞死樣改變。
病理生理
除MPSⅡ型呈X連鎖隱性遺傳外,其餘各型的遺傳方式均為常染色體隱性遺傳。有缺陷的基因定位於常染色體上,且只有純合子基因型才會發病。在父母均為雜合子的子女中,其基因突變與正常的幾率均為25%,其餘50%均為雜合子基因攜帶者。由於MPSⅡ型的缺陷基因位於性染色體X上,因此只有男性才患病,女性均為基因攜帶者,子代中男性患病以及女性成為攜帶者的幾率各為50%。
目前已證實的基因突變種類繁多,且不同人群之間的差異較大。黏多糖包括4-硫酸軟骨素、6-硫酸軟骨素、硫酸軟骨素、硫酸類肝素、硫酸角質素、肝素及透明質酸等成分,為角膜、軟骨、骨骼、皮膚、筋膜、心瓣膜和血管結締組織的結構成分。MPSⅠ型的α-艾杜糖醛酸酶缺乏、MPSⅡ型的艾杜糖醛酸硫酸酯酶缺乏以及MPSⅦ型的β-葡萄糖醛酸酶缺乏,均導致硫酸軟骨素和硫酸類肝素的降解受阻。MPSⅢ型的各種酶缺乏均可引起硫酸類肝素的降解障礙。MPSⅣ型的β-半乳糖苷酶缺乏主要影響硫酸角質素的降解。MPSⅥ型的醯基硫酸酯酶B缺乏主要使硫酸軟骨素的降解受阻。不能降解的各種黏多糖成分在體內大量積蓄,並沉積於上述各組織中,引起器官損害及功能障礙。同時,過多的黏多糖可從尿液中不斷排出。
診斷檢查
診斷:
根據病史、臨床表現、實驗室檢查和X線、CT、磁共振、B超、產前檢查等手段可確診。
實驗室檢查:
1.尿液檢查
 遺傳性黏多糖貯積症
遺傳性黏多糖貯積症(2)酶活性測定:可測定尿中各種酶的活性,各型黏多糖增多症均有相應的酶活性降低。
2.血液檢查
(1)Reilly小體:各型黏多糖增多症均可在末梢血或骨髓的淋巴細胞和中性粒細胞內見有大小不等、形態各異的深紫色黏多糖顆粒,即Reilly小體。MPSⅥ型除白細胞以外,尚可在血小板內見到Reilly小體。
(2)酶活性測定:測定末梢血白細胞中的酶活性,是診斷和鑑別各型黏多糖增多症的主要依據。其他輔助檢查: 1.X線檢查 (1)MPSⅠ型:在MPSⅠ型的各亞型中,骨骼改變的X線表現亦是以Hurler綜合徵最為嚴重。 ①頭顱:出生後6個月以內基本正常。其後逐漸出現顱縫早閉,前囟門閉合延遲。頭顱前後徑增大呈舟狀。腦脊膜增厚可引起阻塞性腦積水,可使頭顱進一步增大。蝶鞍前後徑增大,呈仰臥的“J”形或鞋形;有蛛網膜下囊腫者,可出現蝶鞍增大。顱骨板緻密,板障增厚,顱底及眶頂亦有硬化。蝶竇、乳突與鼻旁竇發育及氣化不良。下頜骨粗短,鉤狀突發育不良,呈扁平或凹陷,踝狀窩變淺、不規則。牙齒小,排列稀疏、不齊,磨牙常位於下頜支內。 ②脊柱:椎體上下緣呈雙凸或橢圓形,齒狀突短小,可有寰樞關節半脫位。胸椎下段和腰椎上段(胸12、腰1或腰1、腰2)椎體短小,呈卵圓形,其前下緣變尖,呈“鳥嘴”樣突起,並向後移位形成後凸畸形。 ③胸廓:肋骨脊柱端細小,中段至胸骨端逐漸增寬,呈“船槳”樣改變。鎖骨內側段明顯增粗,外側段較細並上翹。肩胛骨位置升高,略呈等邊三角形,下角變尖,肩胛盂淺而小,甚至消失。肱骨頭扁小,頸-乾角變小,甚至可呈直角,可有內翻畸
 遺傳性黏多糖貯積症
遺傳性黏多糖貯積症2.CT與磁共振(MRI)可準確地了解包括大腦、脊柱、骨(軟骨)、關節、呼吸道及心血管系統等結構改變的程度和範圍。二者均可清楚地顯示顱骨發育不良、大腦白質改變、腦積水、蛛網膜下腔狹窄、蛛網膜囊腫、顱頸關節的硬腦膜增厚、脊髓壓縮等。但在腦白質檢查方面,磁共振較CT更為敏感和可靠。通常,病程越長則CT與磁共振檢查的改變越明顯。
3.B型超聲用於宮內檢查時,可發現胎兒有無骨關節畸形、肝脾腫大和腦積水等異常。
4.組織活檢活體組織檢查顯示肝細胞、皮膚或結締組織中的成纖維細胞所含的黏多糖代謝酶活性均顯著降低。
5.產前檢查通常不作為正常妊娠的常規檢查。對於生有甘露糖苷增多症患兒的女性,再次懷孕時可行羊水黏多糖濃度及羊水細胞的酶活性測定。如果羊水黏多糖濃度明顯增高、羊水細胞酶活性顯著降低,則產前診斷可以確定。
鑑別診斷
黏多糖增多症尚需與以下疾病進行鑑別:
1.多發性硫酸脂酶缺陷症本病的臨床表現與黏多糖增多症有相似之處,但智力低下和神經系統症狀較黏多糖增多症出現更快,常類似於異染性白質萎縮症。患者常有肝腫大和固定的皮膚魚鱗癬。實驗室檢查無黏多糖尿及細胞酶缺乏。
2.全身性神經節脂苷沉積症(GML神經節脂苷病)兼有脂肪和黏多糖貯積病的臨床特點。患兒在嬰兒期即有嚴重的全身神經節脂苷沉積,智慧型發育遲緩,肌張力低下,肝脾腫大,半數以上的患者有皮膚黃斑和櫻紅點。
 遺傳性黏多糖貯積症
遺傳性黏多糖貯積症4.岩藻糖病患者面容醜陋,肝脾腫大,嚴重的精神、運動發育遲緩,多發性骨發育不良。尿中排泄含有低聚糖的岩藻糖,無黏多糖尿。
5.天門冬醯氨葡萄糖尿症容易與Hurler綜合徵及Hunter綜合徵相混淆。患兒出生時正常,逐漸出現寬鼻、塌鼻樑、鼻孔前屈、厚唇等醜陋面容,並有短頸,頭顱不對稱,脊柱側凸,肝脾腫大,尿中含有大量的天門冬醯氨葡萄糖。
6.黏脂病黏脂病Ⅰ型的臨床表現和X線改變與Hurler綜合徵有許多共同之處。但黏脂病多數有肌陣攣性抽搐,肌肉萎縮、舞蹈病樣手足徐動,眼球震顫,以及皮膚黃斑和櫻紅點。尿中涎酸結合的低聚糖排泄量增加,黏多糖水平正常。黏脂病Ⅱ型的精神、運動發育遲緩發生較早,且發展較快。早期有牙齦增生,胸廓狹小,心瓣膜病多見,無角膜混濁,半歲左右即可見長骨骨膜形成,患兒常早年夭折。尿中無黏多糖增多。黏脂病Ⅳ型亦可有智力發育遲緩、角膜混濁等,但無黏多糖尿。
7.Kneist綜合徵臨床表現與Morquio綜合徵相似,包括大頭,鼻樑塌陷,齶裂,短頸,鍾狀胸,視網膜剝離,聽力損害,腹外疝,肢體和軀幹短小,弓形脛骨,脊柱後凸,關節強直等。患兒亦可有硫酸角質素尿,但無N-乙醯半乳糖苷-6-硫酸酯酶或β-半乳糖苷酶缺乏。
治療方案
 遺傳性黏多糖貯積症
遺傳性黏多糖貯積症併發症
1.神經系統可並發痙攣性癱瘓。
2.循環系統可並發心臟肥大肺動脈高壓冠狀動脈廣泛梗死可引起猝死勱。
4.消化系統可並發肝脾腫大有時可有臍疝或股疝勱。
5五官可並發,眼球突出或視網膜病變勱,傳導性耳聾健康搜尋,可能是由於聽骨畸形所致。
預後及預防
預後:
 遺傳性黏多糖貯積症
遺傳性黏多糖貯積症2.黏多糖貯積症Ⅱ型患者存活較長,一般可存活20~30年,病變為進行性發展,病人因心臟、呼吸系統嚴重受累死亡。
3.黏多糖貯積症Ⅲ型本病有進行性智力減退,骨骼改變常在兒童期可修復,甚至在骨骺融合後可完全消失。但骨關節畸形和塑形異常,則無法完全恢復。少數病人因呼吸道受累而死亡。
4.黏多糖貯積症Ⅳ型很少於兒童期死亡,多數病存活數十年,但本病易累及主動脈瓣和呼吸道,致心肺功能不全死亡。患者還可因寰樞關節半脫位引起中樞神經系統嚴重受損。
5.黏多糖貯積症Ⅶ型重型者常因心臟病變夭折。因關節攣縮可影響到患者正常生活。存活者,均可過早發生繼發症、退行性骨關節病。黏多糖增多症患者的壽命明顯縮短,平均預期壽命一般為10~20歲。主要的死亡原因為冠狀動脈和主動脈瓣損害以及肺部感染。如能早期診斷,並有效減少體內黏多糖的堆積,將有助於患者智力狀況的改善,混濁的角膜可恢復透明,腫大的肝臟和脾臟得以縮小,阻止骨骼畸形的進一步發展,從而大大地改善患者的生活質量,延長壽命。
預防:黏多糖增多症是一組先天性黏多糖代謝障礙性疾病,屬於溶酶體疾病。目前尚缺乏有關預防資料。
相關疾病
代謝系統疾病、黏多糖貯積症Ⅵ型、黏多糖貯積症Ⅴ型、黏多糖貯積症Ⅷ型、黏多糖貯積症Ⅲ型、黏脂貯積症Ⅰ型、黏多糖貯積症Ⅱ型、黏多糖貯積症Ⅳ型、黏多糖貯積症Ⅶ型、黏脂貯積症Ⅱ型。
