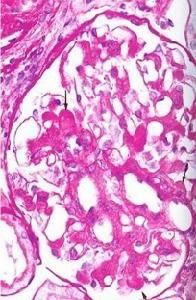
流行病學
世界各地報導的發病率有很大差別,似以西太平洋地區為最高日本報導占活檢證實的腎小球疾病的50%,而歐洲約為10%~30%美國則不到2%中國各地報導也不盡相同,約在20%~30%左右這種差別顯然也受到各地腎活檢指征和尿液普查的影響,例如英國一般報導在5%左右,然而蘇格蘭地區一組無症狀血尿活檢中則達到37%。IgA腎炎以男性為多見,男女比例約為2∶1。種族間存在著差別,例如美國新墨西哥地區印弟安人中占35%,黑人中卻十分罕見雖然發現黑人中IgA2m(1)明顯低於白人,但未能證明這與發病率低有肯定關係。自1978年以來,有一些報導提示IgA腎炎有家族中高發傾向,提示至少在某些IgA腎病病人中存在著基因的易感性HLA分析發現與Bw35和DR4有關。最近的一組因IgA引起的終末期腎衰中的分析提示B27和DR1頻度增高而DR2頻度下降。
發病機制
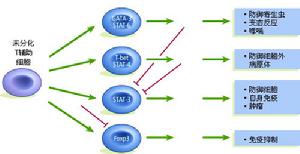 T輔助細胞分化及作用
T輔助細胞分化及作用眾多的抗原,包括多種病毒和多種食物的抗原可在IgA腎炎病人的系膜區中被檢出,並常常伴有IgA1沉積。這些抗原的抗體也屬IgA1。由於這些抗體也可存在於正常人的循環中,上述抗原並無專一性或特徵性。
有證據提示IgA腎炎存在免疫調節異常。IgA腎炎的含IgA1循環免疫複合物中,發現有多聚的IgA1類風濕因子;抗α重鏈Fab片斷的IgG抗體增多而IgM抗體減少。有趣的是HIV感染者也存在類似的抗免疫球蛋白模式,卻不發生腎臟IgA沉積。這證明單單這些循環的自身抗體存在,並不是系膜IgA沉積的原因。此外還發現了二種抗內皮細胞的自身抗體(屬IgG)。IgA腎炎腎組織中常有C3沉積,提示激活了補體旁路途徑然而IgA本身無激活補體的能力,IgA免疫複合物雖可激活補體旁路途徑,但它結合補體和C3b的能力很弱。通常認為在腎臟發生補體激活和形成膜攻擊複合物,需有IgG-IgA複合物但是IgA腎炎腎組織中有IgA和C3沉積而沒有IgG或IgM沉積卻很常見。因此,IgA腎炎補體激活的機制尚不清楚細胞免疫也參與了發病機制已發現IgA腎炎可有T輔助細胞(CD4)增加和T抑制細胞(CD8)減少;具有轉換IgM合成為IgA合成的TA4細胞增加,與之有關的Sa1等位基因的頻度也增加;引起IgA同型轉換的TGFβ、促進產生IgA的B淋巴細胞分化的IL-5和介導IgA產生的IL-4形成均有增加。雖然T細胞和B細胞均參與了增加IgA合成的過程,但IgA合成增多並不是系膜區IgA沉積的原因,因為在IgA多發性骨髓瘤病人中罕見有組織IgA沉積因此結構-免疫學/理化異常才可能是系膜IgA沉積的原因。
臨床表現
 蛋白尿
蛋白尿腎病綜合徵可見於5%~20%的病人中以兒童和青年病例為多常屬瀰漫性增生型伴或不伴腎小球硬化此外,有時系膜IgA沉積為主的現象也可以出現在以足突融合為特徵的微小病變腎病中。
約不到10%患者可呈急性腎功能衰竭表現,通常能自行緩解其中20%~25%則可能需要透析,多因患有新月體腎炎在病程活動期有氮質瀦留者並不少見,約占25%。起病時即有高血壓約占10%,然在30歲以後起病者中顯著增多;隨病程延長,伴高血壓者超過40%。
診斷
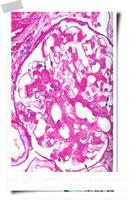 IgA腎炎病理圖
IgA腎炎病理圖檢查:
鏡下血尿者,尿紅細胞以畸形者為主。約50%患者血清IgA增高,但與病情活動無關。血清IgA中λ輕鏈濃度增高。尿免疫球蛋白測定無特殊意義。血補體成分大多正常。某些補體成分或因子可能減少,主要見於有家族高發傾向病人中,但不具有診斷價值。約半數病人IgA-纖維連線蛋白聚集物測定值可有一過性增高,雖然有助於與其他腎病鑑別但其與IgA腎炎活動無關,故並無診斷價值10%~15%病人可有IgA循環免疫複合物增高,32%病人有IgA類風濕因子水平增高多項免疫學指標,包括病毒和食物抗原、抗體、T細胞亞群、HLA位點抗原等測定結果可有改變,但均無診斷價值。50%病人前臂掌側皮膚活檢中可見毛細血管內有IgA和C3等沉積。
治療
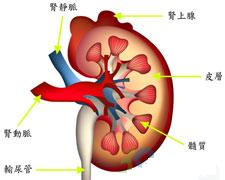 腎臟結構圖
腎臟結構圖終末期IgA腎病者接受腎移植後,移植腎很快發生系膜區IgA沉積;若供腎者有亞臨床IgA腎病,植入非IgA腎病尿毒症者後,供腎系膜區IgA沉積物常迅速消失移植腎伴復發性IgA腎病並不必然發生進行性腎衰,然而腎移植後所施免疫抑制治療,包括環孢素A也並不能阻止其發展。對屍體腎移植而言、1年和3年移植腎存活率可達87%和77%,然而個別有抗HLA抗原的IgA抗體的IgA腎移植者2年移植腎存活率可達100%,有理由認為這些抗HLA抗原的抗體對增加移植腎存活率起了有益的作用。
預後:
IgA腎炎可有自發緩解,約占4%~20%。每年約有1%~2%病例進入終末期腎衰。壽命表統計分析顯示10年腎存活率為80%~90%。估計最終發展成尿毒症者約35%左右。其餘為持續的血尿或蛋白尿。提示預後不良的因素有:起病時即有腎功能不全、蛋白尿超過1.5g/d、高血壓和無肉眼血尿;腎活檢有腎小球硬化、間質纖維化腎小球毛細血管被侵犯、瀰漫增生和瀰漫新月體形成等。
流行病學
世界各地報導的發病率有很大差別,似以西太平洋地區為最高。日本報導占活檢證實的腎小球疾病的50%,而歐洲約為10%~30%,美國則不到2%。我國各地報導也不盡相同,約在20%~30%左右。這種差別顯然也受到各地腎活檢指征和尿液普查的影響,例如英國一般報導在5%左右,然而蘇格蘭地區,一組無症狀血尿活檢中則達到37%。本病以男性為多見,男女比例約為2∶1。種族間存在著差別,例如美國新墨西哥地區印弟安人中占35%,黑人中卻十分罕見。雖然發現黑人中iga2m(1)明顯低於白人,但未能證明這與發病率低有肯定關係。自1978年以來,有一些報導提示本病有家族中高發傾向,提示至少在某些iga腎病病人中存在著基因的易感性。hla分析發現與bw35和dr4有關。最近的一組因iga引起的終末期腎衰中的分析提示b27和dr1頻度增高而dr2頻度下降。