疾病概述
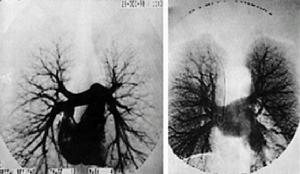 α-半乳糖苷酶A缺乏病
α-半乳糖苷酶A缺乏病本病腎臟受累多出現在20歲後主要表現為輕度蛋白尿,偶爾伴隨血尿偶見腎病綜合徵和較輕度的高血壓症狀一般腎功能減退緩慢,患者常於40歲以後發生終末腎衰偶爾有嚴重腎小管功能障礙出現腎性尿崩症腎小管酸中毒或腎性糖尿。
法布里病患者的平均壽命為50歲。法布里(Fabry's)病為溶酶體α-半乳糖苷酶A缺乏症,由於N-脂醯鞘氨醇三已糖苷(globotriaosylceramide)及相關的糖鞘脂(glycosphingolipids)進行性積聚而引起,受累病人有腎臟、心臟和腦微血管病變,導致腎衰,中風,心臟併發症等疾病。
疾病原因
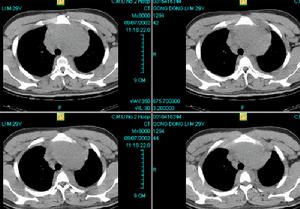 法布里病--影像
法布里病--影像1967年Brady等闡明了該病的生物化學缺陷。他們認為溶酶體酶醯基鞘氨醇己三糖苷酶活性缺陷導致了神經氨醇分解代謝減低從而導致細胞內神經氨醇半乳糖苷醯基鞘氨醇的沉積。上述細胞內沉積物a末端連線一個半乳糖苷殘基。由於人們對這一特異酶缺陷的認識,現在可以準確地診斷半合子的男性,並可以辨認雜合子女性攜帶者以及在宮內受到影響的胎兒。
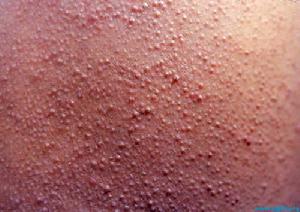 法布里病
法布里病現已明確法布里病是一種X連鎖遺傳的疾病,缺陷基因位於X染色體長臂上。半合子中該基因的外顯率很高酶缺陷的臨床表現既有家族內也有家族間變異α-半乳糖苷酶的整個基因組序列都已被破譯而且可以得到足夠長度的cD-NA不同家族分子排列不同,存在著外顯子突變、基因重排和鹼基對缺失受影響的半合子男性表現出多系統臨床表現,雜合子的女性則有著不同的臨床表現,也可無症狀但可找到脂質貯積的證據。
本病最常見於白種人也見於亞洲人,而西班牙人、葡萄牙人及黑人發生率只有1/4萬幾乎所有患者都為正常核型,只有一例患者組型為47,XYY本病男性發病及病情較女性重;發病年齡在兒童後期到青少年早期存活期在50歲左右,女性攜帶者可存活至70歲。
臨床表現
1.腎臟表現
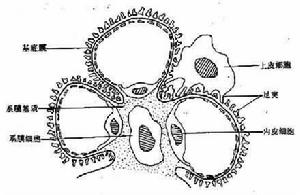 蛋白尿
蛋白尿2.系統的表現
(1)皮膚血管角質瘤:是本病特徵性損害,發病率約90%,平均發病年齡17歲。以陰囊部角化血管瘤最為明顯,常伴有面部毛細血管擴張在皮膚超表層呈簇或葡萄狀的點狀的鮮紅紫紅或紅黑色的靜脈血管擴張區有出血傾向,壓之不褪色較大皮疹可有過度角化。系皮膚血管的內皮細胞與平滑肌因鞘糖脂的沉積而弱化後擴張而來出生時僅可見以後可擴展成4mm,可高出表面分布於臍膝之間的所謂“坐浴區”(軀幹下部臂股、髖部及會陰處),常兩側對稱。隨年齡增長角質瘤的數量與面積也增多增大。
(2)自主神經系統功能失常:神經系統表現常是本病最早出現的症狀,發病年齡在10歲最初表現可發生在年僅5歲的小兒可先於血管角質瘤多年前出現,故兒科醫師對此現象的認識十分必要
Fabrys病神經系統受損的表現,主要是發作性痙攣掌痛(Fabrys危象)與四肢蟻爬感Fabrys病患者痙攣掌痛與四肢蟻爬感典型表現是在冷熱、運動勞動後,手掌和足底間歇發作性刺痛燒灼痛,向四肢近端放射嚴重的周期性發作持續數分鐘到數周。呈周期性發作疼痛者為77%慢性病程者為89%終身持續者,為90%也可表現為雷諾征腹痛隨年齡增長疼痛發作次數減少、程度減輕誘發因素有發熱天氣變暖運動緊張飲酒疼痛程度劇烈時,常伴有疲乏無力發熱、出汗與血沉增快而誤為風濕查體無神經系統體徵。
此外尚有37%患者有中樞神經系統損害症狀,發病年齡一般大於26歲,表現為腦卒中(占24%),痴呆、被動和壓抑社會交往活動障礙等人格改變(占18%)腦脊液檢查正常,腦部磁共振成像(MRI)檢查可早期發現白質和灰質小的病灶。
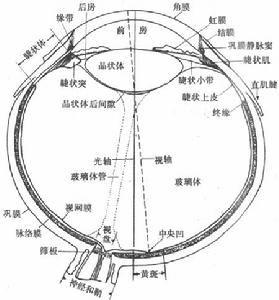 法布里病--眼部病變
法布里病--眼部病變(3)眼部病變:眼部體徵是Fabrys病具有特徵性變化之一角膜混濁可見於所有的雜合子和大多數的半合子。患者可表現有晶狀體前部和後部的異常,出現白內障及視網膜血管迂曲擴張角膜混濁、角膜漩渦狀沉積物儘管這不影響視力或視力輕度減退,特別是女性患者70%~80%可以僅表現出該病的眼部體徵,當眼科醫師發現患者角膜變性或者晶狀體的改變時,應該想到Fabrys病並建議患者去做基因檢查,以便發現該患者的其他家庭成員是否,也患有此病。因此眼科醫師在Fabrys病的診斷中應起著非常重要的作用。
(4)心臟損害:心臟受損常常是Fabrys病患者的死因之一主要表現為傳導障礙心肌病,冠狀動脈功能不全或冠狀動脈阻塞導致心肌梗死,高血壓(腎臟缺血導致腎素分泌增加)瓣膜與升主動脈退行性病變(二尖瓣脫垂多見)一般來講Fabrys病患者溶酶體酶α-半乳糖苷酶A酶活性僅有正常人的1%~17%如果殘餘酶活性高,患者可以無症狀或僅出現心臟的病變當引起缺血性心臟病時患者可出現心絞痛、心肌梗死和充血性心力衰竭而死亡。
(5)其他系統器官:Fabrys病患者除以上臨床表現外,還可以見到進行性感覺神經性聽力喪失(78%);面部出現水腫嘴唇增厚,唇皺褶增多畸形(56%);此外,部分患者可出現溶血性貧血淋巴結病、肝脾腫大骨無菌性壞死肌病、肺功能減退免疫功能低下血小板聚集增強而易發生血栓與栓塞。
常見併發症有胃腸道病變如餐後上腹不適、早飽感噁心嘔吐、腹瀉和腹部痙攣性疼痛、空腸憩室並腸穿孔如腎血管病變比腎小球病變嚴重可並發腎梗死其他如心臟損害嚴重者可出現心絞痛心肌梗死和充血性心力衰竭而死亡。
疾病診斷
診斷
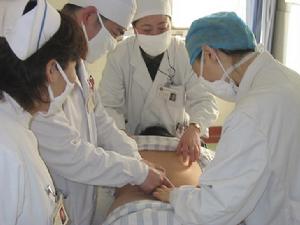 法布里病--疾病診斷
法布里病--疾病診斷由於Fabrys病患者神經醯胺三己糖苷的正常分解代謝所需的溶酶體酶α-半乳糖苷酶A功能缺乏或活力降低糖鞘脂代謝存在障礙致使脂質分解代謝過程中神經鞘脂類,主要為腦胺三已糖苷(ceramidetrihexosideCTH)在全身各種組織中廣泛沉積,如血管內皮與平滑肌的細胞內、中樞神經系統,神經元周圍神經系統,神經節皮膚眼胃腸道、心臟腎臟等,因此臨床症狀表現為多系統損害,有時以某一系統症狀為主通常依據臨床表現、特徵性體徵以及陽性家族史活檢組織以及培養的皮膚成纖維細胞內α-半乳糖苷酶活性低下等明確診斷並不困難。如果臨床表現提示為α-半乳糖苷酶A缺陷通過測定從外周血分離出來的白細胞中該酶的濃度可助診斷。半合子患者幾乎無酶的活性。如果該酶活性達正常人6%~20%則可無臨床症狀在雜合子,該酶活性水平介於正常人和半合子之間。測定白細胞中α-半乳糖苷酶A活性不是辨別攜帶者的敏感方法辨別攜帶者最好是測定尿中醯基鞘氨醇雙半乳糖化物和三羥化物濃度。測定培養的羊膜細胞α-半乳糖苷酶A水平可進行產前診斷。
只有很少的貯積疾病有與法布里病一樣的腎臟病變和貯積物的分布。腎小球小管上皮細胞空泡形成無特異性,但包涵體超微結構特點有診斷意義。在考慮為本病且有症狀的男性患者如包涵體分布廣泛且受累細胞中包涵體數目眾多,尤其是在腎小球的上皮細胞中,應考慮本病診斷尿沉渣發現含有典型包涵體和游離髓磷脂體的完整細胞,對診斷有重要價值。
鑑別診斷
在疾病的早期或症狀不典型時應與以下疾病相鑑別:
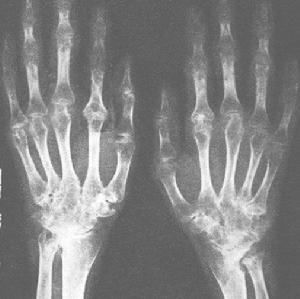 法布里病--風濕病
法布里病--風濕病2.藥物性眼損害:藥物性眼損害有明確的服藥史,如氯喹可引起與Fabrys病相似的角膜混濁現象
3.心腦血管性疾病:年輕人出現嚴重的痛性神經病變或有抽風偏癱、人格與行為改變,伴進行性腎心血管和腦血管的功能障礙,應想到本病,MRI可早期發現腦損害
此外注意與其他原因引起的腎小球腎炎和腎小管功能障礙的疾病相鑑別
疾病檢查
實驗室檢查
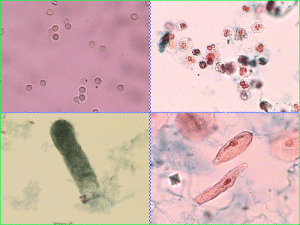 尿沉渣檢查
尿沉渣檢查2.血液生化檢查血漿白細胞或成纖維細胞中的α-半乳糖苷酶活性明顯降低其原理是由於溶酶體酶α-半乳糖苷酶A將醯基鞘氨醇水解為鞘氨醇和一個自由脂肪酸,當缺乏該酶時糖鞘脂在血漿中的濃度和組織中的沉積增多半合子患者血漿中醯基鞘氨醇三羥化物濃度增高可達正常值3倍在一些組織中增多可達300倍
3.羊膜或絨毛囊穿刺通過檢測羊水及絨毛中(妊14周時)α-半乳糖苷酶的活性有助於產前診斷
其它輔助檢查
腎活檢病理檢查:
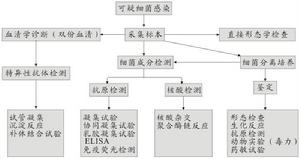 光鏡檢查信息
光鏡檢查信息本病腎小球變化最顯著,石蠟切片顯示腎小球髒層上皮細胞擴大,細胞內空泡形成空泡通常小而均一故細胞呈蜂窩狀,胞漿幾乎消失而不宜辨認壁層上皮細胞受累相對少見,內皮細胞和系膜細胞偶可見到空泡。在早期或較輕的患者,腎小球可無其他異常,隨著病情進展至腎功能衰竭,逐漸進展至腎小球節段性或全球性硬化在硬化小球仍能發現有空泡形成的細胞,為進展性腎病患者的診斷提供了線索腎小管有相似空泡細胞以遠曲小管和亨勒(Henle)襻最為明顯。近曲小管細胞較少受累。動脈及小動脈中有大量空泡細胞。內皮細胞常受累細胞擴大呈泡沫狀。血管中層平滑肌細胞內有大小不等的空泡。
鋨固定塑膠包埋組織切片用甲苯胺或亞甲藍處理後,可在先前提到的細胞內包涵體的相應部位見到細的暗染的顆粒狀包涵體。這種技術診斷價值更大,尤其是在完全或局灶硬化的腎小球,這種方法也可以用來辨認受累的間質細胞。
 法布里病--透射電鏡檢查
法布里病--透射電鏡檢查3.電鏡檢查:電鏡下顯示上述細胞包含無數圓或卵圓形層狀小體(這些小體被稱為“斑馬小體”或“髓鞘脂影”)對本病診斷很有意義。
本病幾乎所有腎臟細胞均可受累以腎小球毛細血管上皮細胞最甚,受累細胞溶酶體內可見典型的同心圓排列的層板樣異常包涵物為電子緻密的嗜鋨性層狀小體,由於切面不同可呈太陽光環狀、蠕動的絨毛狀或斑馬紋狀結構。多種細胞胞質內有多種形態擴大的溶酶體呈洋蔥皮樣、層板樣緻密實心球狀或空泡狀因此該病的溶酶體改變亦可呈多樣性此外,還可有上皮細胞足突融合基膜灶性增厚等改變
相關檢查
1、α-半乳糖苷酶
2、沉渣(尿)
疾病治療
 法布里病--治療
法布里病--治療1.基因治療和去除酶解物治療
美國生物學評估和研究中心(CBER)2003年批准了Genzyme公司生產的Fabrazyme(agalsidasebeta,agalsidase-ß),並用於Fabrys病患者Fabrazyme是經基因工程制出的α-半乳糖苷酶A代替了患者體內缺乏脂肪代謝酶。臨床試驗顯示Fabrazyme能通過彌補溶酶體酶的缺陷啟動,積聚的脂質分解定期,清除器官細胞內的脂肪沉積緩解患者的疼痛症狀,改善心臟功能和穩定腎功能,但仍不能逆轉已存在的腎臟損害,儘管Fabrazyme在美國剛被批准,但它在歐洲的套用已有2年,在對58人的研究中,每2周靜脈用藥1次,可明顯清除2/3患者腎臟和其他組織的脂肪積聚,患者疼痛症狀也有明顯減輕擺脫了麻醉鎮痛藥獲得了較好的療效,Fabrazyme的有效性研究和最終是否對患者有益,還有待進一步的研究。因Fabrazyme有一些嚴重的副作用,包括疼痛的輸液反應和變態反應,美國食品及藥品管理局(FDA)提醒在患者輸液時應仔細監測,注意臨床副反應其他提高酶活性的方法包括:如輸正常人血漿移植胎兒肝、血漿置換輸注白細胞、血小板胎肝等效果尚不肯定。
2.腎移植
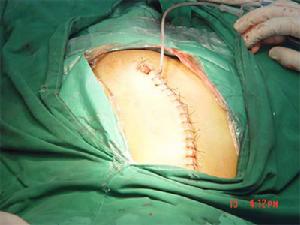 腎移植
腎移植對法布里病腎移植患者要多加注意,因其常有不可預期的高死亡率(1年和5年的死亡率分別為43%,47%);這多是由於膿毒血症所致,現無證據表明法布里病腎功能衰竭患者的細胞和體液免疫系統與其他尿毒症患者有什麼不同。儘管典型的糖鞘脂包涵體會在移植腎中再次出現,但程度和嚴重性少有臨床意義
3.對症治療
主要是針對神經性疼痛、慢性腎功能不全心臟病變等臨床表現的對症治療疼痛對加巴噴丁(Neurontin)、卡馬西平或鴉片類藥物反應差;阿司匹林可套用治療;高血壓可用血管緊張素轉換酶(ACE)抑制藥。對脂肪不耐受者,可套用專為脂肪吸收功能障礙者配製的Lipisorb液。此外,活血化瘀的中藥可能對控制本病的症狀有所幫助。
