疾病概述
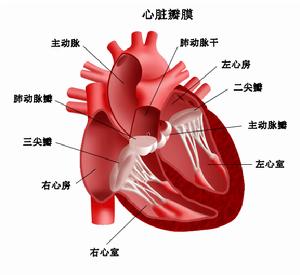 舒張性心力衰竭
舒張性心力衰竭症狀體徵
 舒張性心力衰竭
舒張性心力衰竭2.體徵單純或早期舒張性心力衰竭的特徵性體徵並不多,雙肺呼吸音可減弱,聞及肺部水泡音;心濁音界常無擴大,可聞及舒張期奔馬律。但它們往往與原發心臟病體徵並存,如高血壓心臟病所致的舒張性心力衰竭可有心尖搏動增強、心尖部可聞及收縮期雜音、主動脈瓣第二音亢進;梗阻性肥厚型心肌病可在胸骨左緣第四肋間聞及較粗糙的收縮期雜音;主動脈瓣狹窄可在主動脈瓣第一聽診區聞及較響的收縮期雜音;缺血性心臟病可能伴有心尖部第一心音低鈍、病理性第三心音等。合併存在收縮性心力衰竭或持久性舒張性心力衰竭,其體徵與典型的充血性心力衰竭無異,主要是左、右心衰竭體徵加原發心臟病體徵,仔細體檢便可發現。
疾病病因
 舒張性心力衰竭
舒張性心力衰竭①影響左室鬆弛性能的疾病:如高血壓性心臟病、肥厚型心肌病、主動脈瓣狹窄、缺血性心臟病、老年人心臟病和糖尿病。
②影響左室僵硬度的疾病:如心肌澱粉樣變性、血色素沉著症、限制型心肌病、心肌間質纖維化和心內膜纖維化。
③影響心室間相互作用的疾病:如右室容量負荷增加(房間隔缺損)、右室壓力負荷增加(肺動脈高壓)及急性右室擴張(如急性三尖瓣反流、右室梗死、急性肺動脈栓塞等)。
④影響左室充盈的疾病:如縮窄性心包炎、大量心包積液和心包填塞以及快速性室性心動過速等(由於這類疾病中的左室本身舒張功能並無異常,故有人對此能否作為舒張性心力衰竭的病因還持有異議)。最常見引起左室舒張性心力衰竭的疾病做一介紹:
1.高血壓高血壓是引起舒張性心力衰竭主要的危險因素之一。25%無症狀高血壓患者存在舒張功能障礙,90%有左室肥厚的高血壓患者存在舒張功能障礙。臨床研究顯示這部分患者多為舒張早期心室充盈受損。心房代償,舒張晚期心室充盈增強。患者舒張早期充盈受損通常與後負荷增加及心室重量增加有關。高血壓患者舒張功能受損涉及多種機制:
①心室弛緩異常:高血壓患者未出現心臟結構異常前即可有舒張功能障礙,多為心肌細胞功能障礙導致等容弛緩異常。等容弛緩異常使等容弛緩時間延長,左室壓力下降緩慢,舒張早期心室充盈減少,心房充盈代償性增多。此外高血壓心肌肥厚嚴重時,即使沒有冠狀動脈異常也可有心內膜下心肌缺血加重損害心室舒張功能。當有室內差異傳導或束支傳導阻滯時,心室的不均一性也將減少心室弛緩率。
②心肌僵硬度增加:左心室肥厚是血壓升高心臟後負荷增加的代償性表現。增高的後負荷可通過直接機械刺激及神經內分泌途徑如AngⅡ促進心肌細胞生長及表型改變,膠原產生,最終使心室重量增加,心肌僵硬度增高,舒張功能障礙。高血壓患者可由單純的舒張功能障礙發展成為收縮功能障礙。高血壓患者心房由代償發展至失代償常發生心房擴大、心房收縮功能下降及心房纖顫。心房收縮充盈占總充盈量約40%,心房失代償將促進心室舒張功能障礙向典型心力衰竭發展。高血壓患者病情發展一般經歷幾個階段:
①無症狀,但有舒張期充盈異常;
②有症狀,充盈壓升高,儘管收縮功能正常仍有肺充血症狀體徵;
③左室充盈不足導致心排出量下降;
④逐步發展至收縮和舒張功能障礙,表現為充血性心力衰竭。
2.肥厚型心肌病肥厚型心肌病被認為是舒張型心力衰竭的原型。左心室肥厚程度與最大舒張期充盈密切相關,此外還受心室腔幾何構型(室壁厚度/直徑比增加)、心肌缺血及纖維化等因素影響。心肌肥厚、心肌排列紊亂、心肌間質纖維化使心臟僵硬度增加。而肥厚型心肌病患者心肌弛緩障礙與下列因素有關:
①舒張早期壓力階差及收縮負荷的改變;
②原發及繼發於心肌缺血的鈣超負荷;
③即使左室是輕中度肥厚的病患者也可有短暫的局部運動不均一。
3.冠狀動脈疾病:90%冠狀動脈疾病患者存在舒張功能障礙。各種形式的心肌缺血通過多種機制損害心臟舒張功能及充盈。心絞痛患者心肌缺血是發作性及可逆性的,伴隨有心絞痛的發作,存在可逆性心室舒張功能障礙,導致左心室舒張壓升高及呼吸困難。實驗模型證實其發生機制主要是心肌弛緩功能受損。心肌缺血能量供應障礙,ATP產生障礙導致:
①舒張期Ca2+濃度增加;
②形成可逆性的緊密結合體;
③局部不均一性暫時的增加。心肌缺血最早表現為舒張功能障礙,只有持續的缺血並導致局部室壁運動障礙,才引起收縮功能障礙。大約60%急性心肌梗死患者有舒張功能障礙。舒張功能障礙是急性心肌梗死最早改變,表現為舒張期壓力-容量曲線向上、向右移位,其中40%表現為弛緩功能障礙,25%表現為限制型舒張功能障礙。其發生可能與下列因素有關:心肌細胞鈣超負荷,心室鬆弛延緩且不完全,心房或心室容量增加,左室活動不均一,左右心室相互作用,心包對心室舒張的限制,瓣膜功能受損乳頭肌功能障礙。心肌梗死後心肌結構發生改變:替代性纖維化、剩餘心肌細胞肥大、膠原網改建、心肌細胞重排,將使心肌僵硬度增加,阻礙左心室充盈。此外有心肌頓抑及心肌冬眠的患者同樣有心室弛緩障礙,且與缺血的程度與持續時間相關。
4.瓣膜性心臟病瓣膜性心臟病患者由於長期壓力及容量負荷導致左心室向心性肥厚及離心性肥厚,並使其舒張功能受損。二尖瓣或主動脈瓣反流引起容量負荷增加,使舒張期室壁應力增加,左心室擴大。主動脈瓣狹窄引起壓力負荷增加使收縮期室壁應力增加,心室向心性肥厚。兩種形式的心室肥厚均伴有心室弛緩障礙,但心室腔僵硬度僅是在向心性肥厚時增加,而在離心性肥厚時減少。舒張功能障礙在瓣膜性心臟病早期即出現,其後才是收縮功能障礙,換瓣手術後儘管患者左室心肌重量及EF值恢復正常,運動時舒張功能障礙仍可持續數年。
5.糖尿病性心臟病儘管沒有明確冠狀動脈粥樣硬化性心臟病及高血壓臨床表現,糖尿病患者仍常常發生心力衰竭,其中30%~50%表現為弛緩延遲,等容鬆弛時間延長。糖尿病患者心臟改變與其他併發症一樣,均與結締組織病理改變有關。因此,糖尿病性心臟病患者的基本特點是主動弛緩及被動順應性輕度異常,但也常合併有收縮功能障礙、EF值降低。
6.縮窄性心包炎及限制型心肌病縮窄性心包炎為心包膜纖維化、僵硬及鈣化束縛心臟,使四個心腔舒張期充盈受限。限制型心肌病則是心內膜、心肌纖維化、或心肌異常組織沉積,使室壁僵硬度增加,心臟舒張功能障礙以舒張中晚期顯著。兩者血流動力學改變相似,均為心室充盈受阻,心室舒張末壓力升高,壓力曲線呈舒張早期下陷,後期呈高原波、肺動脈壓及肺動脈阻力增高,心排血量減少。
病理生理
 舒張性心力衰竭
舒張性心力衰竭(1)鈣離子復位障礙:心肌復極時,肌漿網、線粒體主動攝取Ca2+能力降低,Ca2+復位延遲。見於:
①ATP不足,影響鈣泵功能;
②鈣泵ATP酶活性降低;
③肌漿網對Ca2+攝取力明顯降低;
④鈣超負荷。
(2)肌球-肌動蛋白集合體解離障礙:心肌舒張首先需解除橫橋,即在ATP參與下,Ca2+脫離形成肌球蛋白-ATP和肌動蛋白。
①Ca2+復位延遲;
②肌鈣蛋白與Ca2+親和力增加;
③ATP缺乏時,解離障礙,導致舒張功能障礙。
(3)心室舒張負荷降低:正常人決定心室舒張負荷的因素有心室收縮過程中幾何形態的改變、容積縮小及心臟射血晚期阻力等。幾何形態縮小愈明顯,形成的舒張勢能越大,舒張越完全,反之亦然。射血晚期阻抗增大心肌壓力增高,阻礙心臟舒張。
(4)心肌受損程度不一:使心肌弛緩在時間、空間上表現不均一,局部舒張功能不協調,心臟舒張功能降低。
2.心室順應性降低心室順應性是指心室在單位壓力變化下所引起的容積改變。心室順應性舒張開始於快速充盈期末,止於下一心動周期初,是一被動過程。心室的僵硬度是指單位容積變化下能引起的壓力改變,常用心室舒張末期壓力-容積曲線表示。心室順應性與心室僵硬度互為倒數。導致心室順應性下降的因素有:
(1)心包因素:包括縮窄性心包炎及心包積液。
(2)心內膜因素:各種原因引起心內膜增生、纖維化,均可影響心臟舒張功能,如心內膜纖維化症和嗜酸細胞增生性心內膜炎等。
(3)心內因素:增生(如高血壓)、異常物質沉積和浸潤(如澱粉樣物質和鐵沉積浸潤等)、炎性細胞浸潤等導致心室重量增加或心肌肥大,心肌水腫,心肌僵硬度增加。
診斷檢查
 舒張性心力衰竭心電圖
舒張性心力衰竭心電圖①臨床存在導致左心室舒張功能異常的病因,如高血壓、冠心病、糖尿病、肥厚型心肌病、主動脈瓣狹窄、心內膜彈力纖維增生症等。
②患者有靜息或勞力性呼吸困難。
③體檢和X線檢查顯示肺淤血而心臟不擴大。
④超聲心動圖異常,常用E/A比值大於l來判斷左心室舒張功能障礙。但舒張功能嚴重障礙時可出現E/A比值偽正常化。其他超聲心動圖表現有左心房擴大和左心室肥厚。但左心室內徑不大,且左心室收縮功能正常或接近正常。
⑤排除其他可導致呼吸困難(如合併二尖瓣反流)的病變。
⑥必要時可進行診斷性治療,如傳統抗心力衰竭治療效果不佳而使用鈣拮抗藥或β受體阻滯藥有效,可進一步提示為單純舒張性心力衰竭。
實驗室檢查:血液化驗:可發現病人血色素是否正常,有無高血脂、高血糖及高黏滯血症等。
輔助檢查
 舒張性心力衰竭
舒張性心力衰竭2.心電圖:心電圖改變無特異性,單純舒張性心力衰竭多見的改變為P波增寬、增高及左心室肥厚等表現。
3.心機械圖同步記錄心電圖、心音圖與心尖搏動圖可以測得反映左心室舒張性能的時間間期及某些數值的改變。舒張性心力衰竭時可見等容舒張期、快速充盈期及緩慢充盈時間延長,a/H比值及舒張振幅時間指數(DATI)增大。
4.超聲心動圖對評價舒張性心力衰竭最有價值,可提供心臟結構和功能異常的重要線索:
①結構上,可發現左心室形態異常,如高血壓、主動脈瓣狹窄等所致的向心性肥厚;肥厚型心肌病所致的非對稱性肥厚;老年患者可呈現小心腔、室壁中度增厚,即室間隔上部突入左心室流出道,甚至構成狹窄;浸潤性心肌病,特別是心臟澱粉樣變,可顯示雙心室室壁增厚、左心室室壁對稱性增厚、心肌呈斑點狀回聲等組織特徵;右室壓或容量負荷過重可致室間隔左移和右心室呈幾何形態改變。舒張性心力衰竭患者儘管左心室腔正常或變小,但左心房常有不同程度的增大。
②功能上,舒張性心力衰竭患者的收縮功能一般良好,左心室射血分數(LVEF)大多正常,部分肥厚型心肌病患者LVEF超過70%。用M型超聲心動圖檢測二尖瓣前葉曲線的E峰、A峰峰值可用於判斷左心室舒張功能,E/A比值<1提示左心室舒張功能減退。都卜勒測定二尖瓣血流頻譜是評價舒張功能的簡單易行的常用方法,可揭示左心室舒張功能異常及其進展過程。舒張早期流速峰值(EPFV)、舒張晚期血流值(APFV)、舒張早晚期流速峰值比(EPFV/APFV)及舒張早期峰速減速度(DC)都是常用的指標。舒張性心力衰竭患者的EPFV、DC減低,APFV增高,EPFV/APFV小於1。此外,當左心室鬆弛性減退時,等容舒張時間(IVRT)延長;當左心室僵硬度增加時,IVRT縮短;當左心室鬆弛性和僵硬度均有異常時,二尖瓣血流頻譜可“偽正常化”。高齡、心率加快(大於90次/min)、左心室前負荷減小或後負荷增加時可出現假陽性。房室平面位移(atrioventricularplanedisplacement,AVPD)的測定最初用於評價收縮功能,方法是用M型超聲在心尖四腔觀中室間隔與二尖瓣前葉交界點、左心室側壁與二尖瓣後葉交界點位處和在心尖二腔觀中左心室前、後壁與二尖瓣葉的交界處等四個部位記錄收縮期房室平面的最大位移程度。1992年Alam等用AVPD法評價左心室舒張功能,發現左心室舒張功能異常患者時常表現為心房收縮所致的AVPD值在總的AVPD值中所占的比例增高,且這種改變與用脈衝都卜勒測量二尖瓣血流頻譜所得的A/E比值改變有良好相關。
肺靜脈血流頻譜分析也有助於評價左心室舒張功能。多數正常人肺靜脈血流頻譜為三相峰,由收縮峰(S)、舒張峰(D)及心房收縮峰(A)組成。正常時S低於D,但測值接近(參考值為0.55m/s);A很小,約為0.18m/s。左心室舒張功能異常的患者表現為右上肺靜脈血流頻譜S值升高、D值降低、S/D比值增加、A值升高,這種異常與左心室結構和功能密切相關。聲學定量(AQ)方法通過自動檢測心內膜邊界得出左心室面積隨時間變化的曲線及面積變化率(dA/dt)隨時間變化的曲線。後者為雙峰形態,即舒張早期峰值充盈率與舒張晚期充盈率。脈衝都卜勒超聲測量二尖瓣血流頻譜可以發現,E/A比值下降,而AQ方法可發現峰值充盈率/晚期充盈率比值下降。在有些無左心室肥厚的輕度高血壓患者,脈衝都卜勒超聲左心室充盈參數在正常範圍,而AQ方法可檢出E峰加速時間(AT)延長及早期充盈時間延長。脈衝都卜勒心肌顯像(DMI)技術通過在不同心肌節段放置取樣容積以進行在機定量分析,可檢出不同心肌節段受損的範圍和程度。舒張功能不全累及的心肌節段越多,左心室整體舒張功能的損害越大。另外,可用負荷試驗來提高早期舒張功能異常患者的檢出率,例如握力超聲心動圖試驗可用於高血壓患者潛在性舒張功能異常和心肌缺血的診斷。超聲心動圖對左心室舒張功能的檢測結果受許多因素如取樣容積的部位、聲速與血流方向的夾角、年齡、生化和代謝因素(血漿腦利鈉肽、血漿心房利鈉肽等)、藥物如血管緊張素轉換酶(ACE)抑制藥等的影響,故必須結合臨床、心臟形態及功能等資料進行綜合分析。
5.放射性核素顯影主要觀察高峰充盈率(PFR)和高峰充盈時間(TPFR)。從左心室時間-放射活性曲線可以測得舒張性心力衰竭患者的左心室舒張期PFR降低、TPFR延長,則提示舒張功能障礙。此外,舒張功能異常患者的舒張前1/3、1/2、2/3充盈分數(分別為前1/3、1/2、2/3充盈時間內的充盈量與總充盈量的比值)下降。
6.心導管檢查舒張性心力衰竭患者可出現左心室內壓力下降速率(-dp/dt)及其最大值(-dp/dtmax)的顯著降低、T值延長,而左心室僵硬度dp/du增加,心肌僵硬度常數KP即心室僵硬度與其壓力關係的斜率(dp/du-1)增大。
7.運動試驗舒張性心力衰竭早期可無臨床表現,但可有運動耐量減退,程度較收縮性心力衰竭為輕。
鑑別診斷
 舒張性心力衰竭X線
舒張性心力衰竭X線1.收縮性心力衰竭亦可有靜息或勞力性呼吸困難,但它常有體循環淤血症狀和體徵,心臟房室腔明顯擴大,心壁多變薄,射血分值<50%,傳統抗心力衰竭治療有效。
2.慢性肺部疾病:慢性阻塞性肺氣腫、彌散性肺纖維化、塵肺等均可有呼吸困難症狀,但這些疾病既往常有呼吸系統疾病病史,後期可有右心繫統改變,而左心室多無異常。
治療方案
 舒張性心力衰竭治療
舒張性心力衰竭治療1.一般治療預防和控制危險因素如治療高血壓、降血糖、調整血脂、保持正常體重;避免過度勞累和精神刺激等;預防和治療感染,特別是呼吸道感染;如有水鈉瀦留徵象,則應限制鈉鹽攝入等。
2.藥物治療
(1)ACE抑制劑:主要作用為抑制血管緊張素Ⅱ的形成,降低過高的交感神經活動,降低心臟後負荷,同時還能減少醛固酮的分泌,降低室壁的應力和硬度,使心肌肥厚逆轉,增加心室舒張期順應性。理論上,ACE抑制劑有望成為治療心臟舒張功能異常的理想藥物之一,但尚未見ACE抑制劑治療舒張性心力衰竭的大規模臨床試驗。
(2)洋地黃類強心劑:以往認為洋地黃的主要作用是抑制細胞膜的Na+-K+泵,使細胞內Na+增多,與Ca2+競爭向外運動,其結果使細胞內Ca2+增多,心肌收縮力增強。原發性舒張功能障礙的患者往往收縮功能無顯著異常,且常有細胞內Ca2+超載現象,故洋地黃類藥物不能改善舒張功能。最近發表的DIG試驗結果證實,左心室收縮功能正常或接近正常而有心力衰竭臨床表現的患者套用洋地黃,其結果與收縮功能受損的心力衰竭患者相似,即與對照組相比,洋地黃組的總病死率無顯著差異,但再入院率及心功能惡化顯著減少。
(3)利尿藥:利尿藥通過利尿能減輕水鈉瀦留,減少循環血量,降低肺及體循環靜脈壓力,改善心力衰竭症狀。當舒張性心力衰竭為代償期時,左心房及肺靜脈壓增高雖為舒張功能障礙的結果,但同時也是其重要的代償機制,以緩解因心室舒張期充盈不足和(或)障礙所致的舒張期末容積不足和心排血量的減少,從而保證全身各組織的基本血液供應。如此時盲目或大量使用利尿藥,可能加重業已存在的舒張功能不全,使其由代償轉為失代償。可見,利尿藥對代償期舒張性心力衰竭患者似無特殊益處。當舒張性心力衰竭患者出現明顯充血性心力衰竭的臨床表現並可發生肺水腫時,利尿藥則可通過減少部分血容量使症狀得以緩解。
(4)血管擴張藥:由於靜脈血管擴張藥能擴張靜脈,使回心血量及左室舒張期末容積減少,故對代償期舒張性心力衰竭可能進一步降低心排血量;而對容量負荷顯著增加的失代償期患者,可減輕肺循環、體循環壓力,緩解充血症狀。動脈血管擴張藥能有效降低心臟後負荷,對伴周圍血管阻力增加如高血壓心臟病患者的心室舒張功能改善可能有效,但對左心室流出道梗阻的肥厚型心肌病患者可能加重梗阻,使心排血量進一步減少。因此,靜脈擴張劑不宜用於代償期舒張性心力衰竭的治療,而動脈擴張劑則應避免用於左心室流出道梗阻的肥厚型心肌病。
(5)鈣拮抗藥:除硝苯地平、維拉帕米(異搏定)、地爾硫卓外,用於臨床的還有尼群地平及非洛地平等。鈣拮抗劑作用機制:
①Ca2+通道阻滯作用:減輕心舒張期細胞內Ca2+超負荷,加速舒張期Ca2+復位,改善主動舒緩。
②負性頻率作用:心率減慢可減少心肌耗氧量,改善心肌血供,增加舒張期充盈時間。
③負性肌力作用:可減輕心臟收縮期過度收縮所致的幾何構型異常,增加心肌舒縮活動協調性。
④外周血管及冠狀動脈擴張作用:可減輕心臟前、後負荷及增加心肌供血,恢復心肌細胞對Ca2+的良性運轉,加強心肌去收縮活動。故鈣拮抗藥能改善或治療心室舒張功能異常。但梗阻性肥厚型心肌病患者在選擇鈣拮抗藥時,亦應注意強烈外周血管擴張可能加重梗阻。
(6)β受體阻滯藥:此類藥物具有降低心率和負性肌力作用。對左心室舒張功能障礙有益的機制可能是:
①降低心率可使舒張期延長,改善左心室充盈,增加舒張期末容積。
②負性肌力作用可降低耗氧量,改善心肌缺血及心肌活動的異常非均一性。
③抑制交感神經的血管收縮作用,降低心臟後負荷。
④能阻止通過兒茶酚胺引起的心肌損害和灶性壞死。臨床研究證明,此類藥物可使左心室容積-壓力曲線下移,具有改善左心室舒張功能的作用。
(7)抑制心肌收縮的藥物:如丙吡胺具有較強的負性肌力作用,可用於流出道梗阻的肥厚型心肌病。實驗研究發現,此藥縮短射血時間,增加心排血量,降低左室舒張期末壓。多數患者長期服用此藥有效。丙吡胺的另一個作用是抗心律失常,而嚴重肥厚型心肌病患者,尤其靜息時有流出道梗阻者,常有心律失常,此時用丙吡胺可達到一舉兩得的效果。
(8)糾正心律失常:心動過速主要縮短舒張期,故導致左心室舒張充盈時間不足,可加重左心室舒張功能障礙。因此,心動過速時控制心率是非常重要的。心房收縮對心室的補充充盈具有重要意義,尤其當左心室舒張功能障礙時更加重要,故糾正房性心律失常,尤其是轉復心房顫動,可改善左心室的舒張功能。
(9)其他藥物:
①鈣敏感性藥物匹莫苯(Pimobedan):此藥具有強心、擴血管作用,可用於治療左心室舒張功能障礙。
②心房利鈉肽:具有排鈉利尿和血管擴張作用,促進心肌早期舒張作用。
③血管緊張素受體拮抗藥:可在受體水平上拮抗血管緊張素Ⅱ的作用,故具有同ACE抑制劑相似的心血管作用,能改善左心室舒張功能。已套用於臨床的有氯沙坦等。
3.手術治療對於瓣膜性心臟病與縮窄性心包疾病,可分別行球囊擴張術、瓣膜置換術或心包剝離術。梗阻性肥厚型心肌病患者可通過切除肥厚心肌使舒張功能得到改善;或用心室雙腔起搏,通過改變心室電激動順序,減輕左心室流出道梗阻,進而改善左心室舒張功能。冠狀動脈搭橋術可減輕心肌缺血,改善患者的舒張功能,對造成心臟舒縮協調性明顯異常的室壁瘤亦可考慮手術切除。
預後預防
 舒張性心力衰竭檢測儀
舒張性心力衰竭檢測儀 預防:左室舒張功能障礙常早於收縮功能障礙。及早採取保護心肌的措施是有益的。早期診斷和治療舒張衰竭有重要臨床意義。
