流行病學
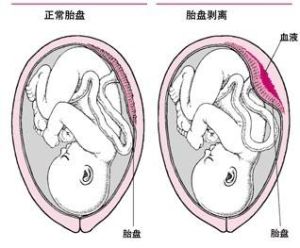
 胎盤早期剝離
胎盤早期剝離病因
經過科學家數十年的研究,發現胎盤早期剝離與高血壓(包括妊娠高血壓綜合徵原發性高血壓腎性高血壓)、創傷,胎膜早破、孕婦年齡、吸菸,使用古柯鹼等因素相關,其發病可能與以下主要危險因素有關。1.高血壓高血壓包括妊娠高血壓綜合徵(簡稱妊高征特別是重度妊高征)、原發性高血壓、慢性腎炎合併高血壓、它們是引起胎盤早期剝離的首要病因。有學者研究報導妊娠期高血壓者發生胎盤早期剝離較妊娠期血壓正常者高5倍。其發病機制主要是胎盤附著部位的底蛻膜螺鏇小動脈發生痙攣急性動脈粥樣硬化,引起遠端毛細血管缺血壞死、破裂而出血,形成血腫,逐步擴大,使胎盤與子宮壁剝離而導致胎盤早期剝離。若孕婦原來就有血管病變如原發性高血壓再並發妊高征,使血管病變加劇則發生胎盤早期剝離的機會更多。
2.機械性因素腹部直接受到撞擊,常是胎盤早期剝離的病因,例如汽車的撞擊、乘公車時突然剎車的碰撞、跌跤時腹壁首先著地、毆打等都可導致胎盤早期剝離。外倒轉糾正胎位時受阻而用力過大,亦可發生胎盤早期剝離。胎盤位於子宮前壁時,羊膜腔穿刺術也可能導致胎盤早期剝離。其他一些間接因素如羊水過多突然胚膜破裂時羊水驟然流出,或雙胎妊娠時第一個胎兒娩出過快,這都可使宮腔內壓力驟降,而發生胎盤早期剝離美國研究資料報導因孕婦外傷所引起的胎盤早期剝離占1%~2%。
3.吸菸近10年的研究證實了吸菸與胎盤早期剝離的相關性,有報導吸菸使胎盤早期剝離發生危險增加90%,並隨著每天吸菸數量的增加胎盤早期剝離發生的危險性也增加。吸菸使血管發生退行性變而增加了毛細血管的脆性,並尼古丁對血管收縮的影響以及血清中一氧化碳結合蛋白濃度升高均可導致血管痙攣缺血,從而誘發胎盤早期剝離。
4.胎膜早破國內外很多研究報導了胎膜早破與胎盤早期剝離的相關性胎膜早破孕婦發生胎盤早期剝離的危險性較無胎膜早破者增加3倍。其發生的機制不明確可能與胎膜早破後伴發絨毛膜羊膜炎有關。
5.濫用古柯鹼有報導指出,在妊娠期間濫用古柯鹼50例孕婦,其中8例死胎是由於胎盤早期剝離引起的。另有報導112例孕婦在孕期濫用古柯鹼,結果發生胎盤早期剝離者占13%。
6.孕婦年齡及產次孕婦年齡與胎盤早期剝離發生是相關的,但有學者報導產次比年齡更傾向於與胎盤早期剝離有關。隨著產次的增加,發生胎盤早期剝離的危險性呈幾何級數增加。
7.其他孕婦長期仰臥或半臥位,使增大的子宮壓迫下腔靜脈,阻礙靜脈回液,導致蛻膜層靜脈淤血或破裂引起部分或全部胎盤剝離。臍帶過短或臍帶繞頸,繞體,在分娩過程中胎先露下降,臍帶長度不足而被強力牽引,也可以導致胎盤早期剝離。
發病機制
 胎盤早期剝離
胎盤早期剝離胎盤早期剝離的主要病理變化是底蛻膜出血,形成血腫,使胎盤自附著處剝離。若剝離面積小出血停止後血液很快凝固,臨床多無症狀,只是凝血塊壓迫胎盤,在胎盤母體面上遺留一壓跡,往往於產後檢查胎盤時方發現;若剝離面積大,繼續出血形成胎盤後血腫,使胎盤剝離部分不斷擴大此時因胎兒尚未娩出,子宮不能收縮,故不能起止血作用,出血不斷增多,可衝破胎盤邊緣,沿胎膜與子宮壁之間經宮頸管向外流出,即為顯性剝離(revealedabruption)或外出血。若胎盤邊緣仍附著於子宮壁上,或胎膜與子宮壁未分離,或胎頭固定於骨盆入口都能使胎盤後血液不能外流,胎盤後血腫逐漸增大,胎盤剝離面也隨之擴大,宮底不斷升高,即為隱性剝離(conealedabruption)或內出血。當隱性出血積聚過多時,血液仍可沖開胎盤邊緣與胎膜而外流,形成混合型出血(mixedhemorrhage)。有時出血可透過羊膜進入羊水中成為血性羊水。
隱性胎盤早期剝離,血液不能外流,出血逐漸增多而形成胎盤後血腫,因之壓力增加,使血液浸入子宮肌層,引起肌纖維分離,斷裂、變性、血液浸入甚至可達漿膜層子宮表面呈現紫色瘀斑,嚴重時整個子宮呈紫銅色,尤以胎盤附著處為著稱子宮胎盤卒中(uteroplacentalapoplexy)。此時肌纖維受血液浸漬,收縮力減弱,有可能發生產後大出血。有時血液還可滲入腹腔,也可浸潤至闊韌帶,輸卵管等處。
嚴重的胎盤早期剝離,尤其胎死宮內病例可以發生凝血功能障礙,剝離處的壞死胎盤絨毛和蛻膜組織,釋放大量組織凝血活酶進入母體循環激活凝血系統導致DIC。肺腎等臟器的毛細血管內均可有微血栓形成,引起臟器損害。血小板及纖維蛋白原等凝血因子大量損耗,最終激活纖維蛋白溶解系統,產生大量纖維蛋白降解產物(FDP)繼而引發纖溶亢進,加劇凝血功能障礙。
臨床表現
 症狀
症狀胎盤早期剝離最常見的典型症狀是伴有疼痛性的陰道出血,然而胎盤早期剝離的症狀和體徵的變化是較大的。
1.輕型輕型的胎盤早期剝離多以陰道出血及輕度腹痛為主,胎盤剝離面通常不超過胎盤面積的1/3,在分娩期多見。主要症狀為陰道出血量較多,色暗紅,可伴有輕度腹痛或腹痛不明顯貧血體徵不顯著。腹部檢查:子宮軟宮縮有間歇,子宮大小與妊娠周數相符胎位清楚,胎心率多正常,若出血量多胎心率可有改變。腹部壓痛不明顯或僅有局部輕壓痛(胎盤剝離處)。產後檢查胎盤母體面有凝血塊及壓跡。甚至少數在分娩前無症狀與體徵,僅在胎盤檢查時才發現有胎盤早期剝離。
2.重型以內出血和混合性出血為主,胎盤剝離面超過胎盤面積的1/3同時有較大的胎盤後血腫,多見於重度妊高征,主要症狀是突然發生的持續性腹痛、腰酸、腰背痛、疼痛程度與胎盤後積血多少呈正相關嚴重時可出現噁心、嘔吐、面色蒼白、出汗、脈弱、血壓下降等休克徵象。陰道不流血或少量流血,其貧血程度與外出血不相符,常為隱性胎盤早期剝離。子宮觸診硬如板狀,處於高張狀態,無間隙性放鬆,子宮有壓痛且超過妊娠月份應有的大小並隨病情發展宮底不斷升高,胎位摸不清,若胎盤剝離面積超過1/2或以上,胎兒常因嚴重缺氧而死亡。
併發症
 胎盤早期剝離
胎盤早期剝離2.胎兒母體出血在外傷性的胎盤早剝,可以發生胎兒至母體的出血。一般非外傷性的胎盤早剝有胎兒至母體的出血僅為20%,其量亦少於10ml;但有嚴重外傷者年Stettler曾報導8例胎兒母體出血達80~100ml。
3.彌散性血管內凝血(DIC)與凝血功能障礙胎盤早期剝離是妊娠期發生凝血功能障礙的最常見原因。重型胎盤早期剝離,尤其是胎死宮內病例很有可能發生DIC和凝血功能障礙胎盤和蛻膜含有豐富的組織凝血活酶,胎盤早期剝離時促凝物質通過損傷的血管進入母體血循環,激活凝血系統,導致DIC。肺、腎等臟器的毛細血管內均可有微血栓形成,引起臟器損害。血小板及纖維蛋白原等凝血因子大量消耗。因此,胎盤早期剝離的時間越長,促凝物質進入母血循環也越多,DIC繼續發展,即激活纖維蛋白溶解系統,產生大量纖維蛋白降解產物(fibrindegradationproductFDP)。由於凝血因子大量消耗,加之FDP又有抗凝作用,導致並加劇凝血功能障礙臨床表現為皮下黏膜下或注射部位出血,子宮出血不凝或僅有軟凝血塊,甚至發生尿血、咯血或嘔血1987年首屆中華血凝學會提出DIC(修正案)的實驗室檢查有下列3項或以上異常者可診斷為DIC①血小板<100×109/L或進行性下降;②纖維蛋白原<1.5g/L或進行性下降;③3P試驗陽性或血FDP>20mg/L;④凝血酶原時間(PT)縮短或延長3s以上,或動態變化,或激活的部分凝血活酶時間(PTT)縮短或延長10s以上;⑤優球蛋白溶解時間縮短,或纖溶酶降低。對於重型胎盤早期剝離,常有血紅蛋白和紅細胞計數降低、PT、PTT延長,3P陽性,纖維蛋白原降低,FDP升高提示DIC發生。在足以使胎兒死亡的30%的病例中發生DIC沒有胎兒窘迫的DIC是不常見的。
4.急性腎功能衰竭重型胎盤早期剝離多由重度妊娠高血壓綜合徵引起。重度妊娠高血壓綜合徵時全身小動脈痙攣,腎內小動脈也痙攣從而引起組織缺氧,腎小球血管內皮細胞腫脹、體積增大,使血流阻滯;腎臟缺血;加之胎盤早期剝離時失血過多,休克時間較長及DIC等因素,使腎血流量急驟減少,嚴重時可使雙腎皮質或腎小管發生缺血壞死或由於大量纖維素沉積於進球小動脈內形成堵塞,而致腎臟急性缺血壞死出現急性腎功能衰竭。臨床表現為:①少尿或無尿,少尿(<400ml/24h=,無尿(<100ml/24h=,多數患者少尿期每天尿量為50~100ml;②高血鉀(>7mmol/L),高血鉀是少尿期引起患者死亡原因之一;③氮質血症,由於少尿腎臟不能將尿素氮及肌酐排出,致使血中尿素氮及肌酐等升高;④代謝性酸中毒,由於酸性代謝產物在體內蓄積並消耗鹼儲備血pH值下降,導致細胞內酶活性抑制和改變中間代謝產物增多而出現代謝性酸中毒。
5.羊水栓塞胎盤早期剝離時剝離面的子宮血竇開放,若胎盤後的出血穿破羊膜,血液進入羊水,則羊水也可反流入開放的子宮血管進入母體循環,形成栓子在肺臟造成肺栓塞從而引起肺動脈高壓,呼吸循環衰竭,DIC,多臟器損傷等一系列羊水栓塞症狀,多在胎兒娩出前發生。如果搶救不及時,有可能危及患者的生命。
6.產後出血產後子宮收縮乏力及凝血功能障礙均可發生產後出血。臨床表現為胎盤娩出後發生大量陰道出血,血液常不凝固檢查時發現宮底不清,子宮輪廓不明顯,患者臉色蒼白,表情淡漠,出冷汗,脈率增加,血壓下降等出血性休克症狀。
7.胎兒宮內死亡當胎盤剝離面積達1/3時胎兒可發生宮內窘迫甚至死亡;當剝離面積達1/2時胎兒多數死亡。即使不典型胎盤早期剝離症狀較輕,對圍生兒危害也是很大的,故即使臨床症狀不嚴重有胎盤早期剝離可疑時,應嚴密監測胎兒宮內情況並予積極處理。
診斷
 診斷
診斷(1)可有外傷史、血管病變史。
(2)有伴有腹痛的陰道流血。
(3)子宮有局限性輕壓痛,並呈高張狀態,宮底升高。
(4)胎心減弱甚至消失。
(5)超聲檢查子宮壁與胎盤之間出現液性暗區羊水中回聲增強增多,絨毛板向羊膜腔突出。
(6)血蛋白降低,可出現凝血功能障礙。
(7)產後檢查胎盤可見胎盤母體面上有凝血塊及壓跡。
2.分類診斷
(1)輕型胎盤早剝:胎盤剝離面通常不超過胎盤面積的1/3表現為陰道流血,貧血體徵不顯著,有輕度腹痛或無腹痛,宮縮有間歇胎位清楚,胎心率多正常,有時症狀與體徵均不明顯,僅在檢查胎盤母體面時發現凝血塊及壓跡。
(2)重型胎盤早剝:胎盤剝離面超過胎盤面積的1/3,表現為腹痛劇烈而持續,無陰道流血或少量陰道流血,貧血程度與外出血不相符,子宮硬如板狀,壓痛,無宮縮間歇,胎位不清,羊水血性,病情嚴重時胎心可消失。
3.須注意發病的誘因凡有妊高征特別是中、重度妊高征者,易並發胎盤早期剝離有資料報導胎盤早期剝離並發妊高征者占40.5%,而有外傷者,占14.8%。認為妊高征伴有胎兒生長受限及貧血者更易發生胎盤早期剝離,應予以注意。
4.根據臨床症狀及體徵綜合分析輕型胎盤早期剝離絕大部分病例開始可能為無痛性少量陰道出血,繼而發展為有痛性陰道出血,故須結合病史,嚴密觀察陰道出血和宮縮的性質、胎心的變化,結合輔助檢查及早作出診斷和處理。重型胎盤早期剝離症狀與體徵比較典型,診斷多無困難但應判斷其嚴重程度,當子宮出血不止,皮膚及黏膜有出血,這常提示有DIC存在,應特別警惕。
5.胎盤附著於子宮後壁的胎盤早期剝離此種最易被忽略,特別是在早期其特點為凡是在妊娠晚期,無論有無陰道出血,只要是原因不明的子宮張力增高,而又非羊水過多,且未臨產,不屬高張性子宮收縮,特別是有妊高征伴有胎兒生長受限者,雖然胎心尚正常必須考慮胎盤附著於子宮後壁的早期胎盤早期剝離可能性。可通過B型超聲檢查,胎心監護來協助診斷。
鑑別診斷
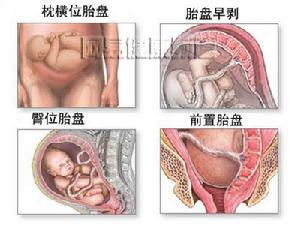
1.前置胎盤前置胎盤的出血無誘因,為無痛性陰道流血可反覆發生,子宮收縮為陣發性,間歇期完全放鬆,無壓痛,貧血程度與外出血量相符,B超可發現胎盤位置低,無胎盤後血腫。
2.先兆子宮破裂往往發生在梗阻性分娩過程中,或有剖宮產史,子宮下段有壓痛並出現病理性縮復環患者有強烈宮縮陰道出血量少血尿。胎盤早期剝離主要與前置胎盤及先兆子宮破裂相鑑別見表1。
 表1
表1治療
 胎盤早期剝離
胎盤早期剝離1.糾正休克對處於休克狀態的危重患者,應立即予以面罩吸氧積極開放靜脈通路,快速補足血容量主要是輸新鮮血,使血細胞比容達30%或稍高,尿量至少30ml/h,輸新鮮血尚可補充凝血因子。搶救休克的同時應做中心靜脈壓的測量以指導補液量。
2.及時終止妊娠胎盤一旦早期剝離,在胎兒娩出前,胎盤剝離可能繼續加重,難以控制出血,持續時間越長病情越嚴重,出現併發症的機會也越大,因此一旦確診重型胎盤早期剝離必須及時終止妊娠。
(1)經陰道分娩經產婦一般情況較好病情較輕以顯性出血為主子宮頸口已開大估計短時間內能迅速結束分娩者,可選擇經陰道分娩。先行破膜使羊水緩慢流出,子宮容積得以逐漸縮小並用腹帶包裹孕婦腹部,壓迫胎盤使其不再繼續剝離。並可促進宮縮,必要時靜脈滴注縮宮素縮短產程。分娩過程中密切觀察患者的血壓、脈搏、子宮底高度、宮縮與出血情況。用胎兒電子監護儀監測胎心變化,早期發現異常情況及時處理必要時改行剖宮產。若宮口開全,應酌情縮短第二產程胎兒娩出後,立即人工剝離胎盤,及時套用縮宮素並按摩子宮,密切觀察子宮縮復情況及陰道出血量,有無凝血塊。
(2)剖宮產:因剖宮產是快速終止妊娠,搶救母兒生命的有效措施,出現下列情況應立即行剖宮產術:①重型胎盤早期剝離,特別是初產婦,不能在短時間內結束分娩者;②輕型胎盤早期剝離,出現胎兒窘迫徵象,須搶救胎兒者;③重型胎盤早期剝離,孕婦病情惡化,即使胎死宮內者;④破膜後產程無進展者。
剖宮產取出胎兒與胎盤後,應立即給予宮縮劑並按摩子宮,子宮收縮良好可以控制產後出血。若發現子宮胎盤卒中,經上述處理並給予熱鹽水紗墊濕熱敷子宮,多數子宮收縮轉佳若不奏效可行子宮動脈上行支結紮,或用可吸收線大8字縫合卒中部位的漿肌層,多能止血而保留子宮萬一子宮不收縮,出血多且血液不凝應快速輸入新鮮血,並當機立斷行子宮切除術。
(3)併發症處理:
①產後出血:胎盤早期剝離常發生嚴重產後出血。分娩後及時套用子宮收縮藥,如縮宮素、馬來酸麥角新鹼、米索前列醇、卡前列甲酯等,持續按摩子宮;若仍有不能控制的出血,應即時考慮行子宮切除。若大量出血且無血凝塊,應考慮凝血功能障礙立即行必要的化驗同時按凝血功能障礙處理。
②凝血功能障礙:在迅速終止妊娠,去除病因的基礎上才能阻斷促凝物質繼續進入母血循環,從而阻止DIC發展。
A.肝素套用:套用肝素治療雖有很大爭議但多主張在DIC的高凝階段套用。但胎盤早期剝離並發DIC的關鍵性處理在於終止妊娠杜絕凝血活酶來源,從而阻止凝血活酶繼續進入血循環。此外對於已發生凝血障礙而有活動性出血的患者來說,如子宮有一個大創面的存在,套用肝素會更加重出血故一般不用肝素治療。
B.補充凝血因子:及時足量輸入新鮮血是補充血容量及凝血因子的有效措施,庫存血超過4h,血小板功能即受破壞效果差為糾正血小板減少,可輸新鮮血小板濃縮液。如無法得到新鮮血時,可選新鮮冰凍血漿應急,1L的新鮮冰凍血漿含纖維蛋白原3g,且可提高Ⅴ、Ⅷ因子至最低有效水平。同時還可輸注冷凝沉澱物,凝血酶原複合物等如血纖維蛋白原低於2g/L,應輸纖維蛋白原,每4g纖維蛋白原可提高血纖維蛋白原1g/L常用量為3~6g。
C.纖溶抑制劑若妊娠已終止而DIC由高凝階段轉入纖溶亢進階段出血不止,可套用抗纖溶藥物以抑制纖維蛋白溶酶原的激活因子,使纖維蛋白溶酶原不能轉變為纖維蛋白溶酶纖維蛋白就不溶解,常用氨基己酸4~6g,氨甲環酸0.25~0.5g,或酚苄明0.1~0.2g溶於5%葡萄糖液100ml內靜脈滴注。
③急性腎功能衰竭,應根據中心靜脈壓的測定及時補充血容量,出現少尿(<17ml/h=或無尿,應靜注呋塞米40~80mg必要時重複,3h後尿量仍不增加者按急性腎功能衰竭處理。
A.少尿無尿期處理:尿量<400ml/24h或<17ml/h為少尿;<100ml/24h為無尿a.防治水中毒,嚴格限制液體入量,準確記錄出入水量每天液體需要量800ml(不顯性失水量)加每天異常損失量(嘔吐腹瀉)加前1天尿量,減去400ml(內生水量)即為當天液體入量b.飲食控制,在少尿早期(48~72h)應禁食蛋白質少尿3~4天后病情好轉,蛋白質的攝入可按每天0.5g/kg計算,套用丙酸睪酮可減少蛋白質分解。c.糾正電解質平衡失調,測定血鉀、鈉、氯、二氧化碳結合力注意血氣變化。如患者出現嘔吐、精神錯亂抽搐、尿素氮≥35.5mmol/L或每天上升>27mmoL/L、CO2CP<15mmol/L血K+>6.5mmol/L均是血液透析的指征。
B.多尿期處理:當尿量≥1500ml/24h適當補充Na+、K+及H2O如尿量≥2000ml/24h,液體的補充只須補充尿量的2/3,並需補充K+Na+、Cl-同時可肌注醋酸去氧皮質酮3mg以減少尿量。
預防
胎盤早剝由於胎盤在胎兒娩出前即從宮壁剝離,影響了胎兒的血液供應,剝離面過大時胎兒多因缺氧而發生嚴重的窘迫,甚至死亡;由於從剝離處的胎盤絨毛和蛻膜中釋放大量組織凝血活酶,進入母體循環誘發DIC,可引起產前產後出血,如治療不及時,可並發急性腎功能衰竭、席漢綜合徵(希恩綜合徵,Sheehanssyndrome)等嚴重併發症。