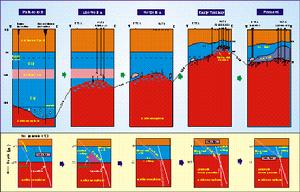
 海洋地球化學
海洋地球化學海洋地球化學是研究海洋中化學物質的含量、分布、形態、轉移和通量的學科。它是地球化學中以海洋為主體的一個分支,也是化學海洋學的主體。
研究簡史
地球化學,主要研究地球的岩石圈、大氣圈、水圈和生物圈的各種化學元素含量(又稱豐度)的分布。研究初期比較著名的代表人物有美國的F.W.克拉克和挪威的V.M.戈德施米特等。50年代以來,C.B.布魯耶維奇、А.Л.維諾格拉多夫、E.D.戈德堡等在海洋地球化學研究方面作了大量工作。研究對象
海洋地球化學的研究對象較廣泛,包括:①主要溶解成分,②溶解氣體,③微量元素,④有機物,⑤核素,⑥懸浮物,⑦熱泉物質,⑧沉積物間隙水。
 相關書籍
相關書籍主要溶解成分
海水中含有11種主要溶解成分,其中有鈉、鎂、鈣、鉀和鍶等 5種陽離子,氯根、硫酸根、碳酸氫根(包括碳酸根)、溴根和氟根等5種陰離子,還有硼酸分子,它們占海水中溶質總量的99.9%以上,各主要溶解成分含量,有一定的比例關係。海水中含量大於1毫克/千克的11種化學成分。它們包括:①鈉、鎂、鈣、鉀和鍶等5種陽離子;②氯根、硫酸根、碳酸氫根(包括碳酸根)、溴根和氟根等 5種陰離子;③硼酸分子。這些成分的總量占海水中所有溶解成分的99.9%以上。被河川搬運入海的岩石風化產物和火山等的噴發物,是海水主要溶解成分的主要來源。 自從地球表面出現海洋之後,在漫長的地質年代中,不但經歷了海陸變遷,而且海水中的溶解成分,曾有過組成的演變。儘管各大洋海水的含鹽量隨海域和深度而異,但海水主要溶解成分的含量間有恆定的比例,就稱海水的組成是恆定的,並稱這些成分是保守成分。
溶解氣體
海洋和大氣有遼闊的交界面,它們之間存在各種物質交換。因此,大氣層中的各種氣體,不斷溶入海水;海水中的溶解氣體(見海水溶解氣體,則不斷逸出而進入大氣。這些氣體溶入或逸出海水的速率,受到富集於海洋表面的某些表面活性物質所構成的微表層的影響(見氣體在海洋與大氣間的交換)。研究得比較多的溶解氣體,有氧(見海水溶解氧)、二氧化碳(見海水二氧化碳系統)、氡-222、碳-14等。
微量元素
海洋中的微量元素,如氮、磷、矽和鐵、鋁、錳等。前三者屬營養元素(見海水營養鹽),其餘的微量元素在海水中的溶解態濃度雖低,有些卻是無機懸浮顆粒中除矽以外的主要成分。還有一些有經濟價值或與生態平衡和環境保護有關的微量元素,如銅、鉛、鋅、鎘、鉻、鈾等(見海水微量元素)。
有機物
海水中有機化合物的濃度雖然不大,但是種類很多(見海水有機物),它們對重金屬在海水中的存在形式,對海水微表層性質和懸浮顆粒表面性質,對海洋中的生物活動,對海水和海底沉積物的氧化還原狀態等,都有直接影響。此外,對海洋中的元素或成分的分布、遷移和通量等海洋地球化學過程也有重要的作用。
核素
包括穩定核素和放射性核素兩種。利用同一元素的穩定同位素在不同自然條件下的比值的差異,或者利用海洋中某些放射性核素的含量作為指標,可以研究各種海洋過程,判別海洋中某些物質的來源和年齡(見海洋中放射性核素、核素在海洋學中的套用)。
懸浮物
海洋中的懸浮物,在河口區水中的含量最大,在大洋海水中的含量最小。它們在海洋物質的遷移中起了相當大的作用。除懸浮顆粒本身的機械搬運外,水中的沉澱析出,懸浮物的分解或溶解,顆粒的絮凝,尤其是這些微小顆粒表面對海水中的化學組分的吸附,顆粒結構的轉化等過程,大部分在固態顆粒的表面進行,屬於微小尺度的表面化學問題(見海水中的懸浮物)。當懸浮顆粒沉降到海底時,就逐漸形成海底沉積層,進行成岩過程。
 海底熱泉
海底熱泉熱泉物質
從海底某些地方噴出的熱泉,含有許多金屬的硫化物等,這也是海洋地球化學的研究對象(見海底熱泉)。熱液噴口是海底的間歇泉,人們稱它為海底熱泉。地殼的巨大板塊一刻不停地運動著,它們的碰撞形成了海底山脈,它們的分離造就了海底裂隙。海水從這些開口處滲入地殼,被熾熱的岩漿“燒”得滾燙。加熱後的海水回流,又從地殼的小縫隙里湧出,形成了海底熱泉。
沉積物間隙水
它的化學組成與海水不同,對上覆水和沉積物的化學組分起著重要的化學交換作用,與沉積物的成岩作用有密切關係(見海洋沉積物間隙水)。 占據海底沉積物顆粒之間及岩石顆粒之間孔隙的水溶液,也叫孔隙水。它是地球水圈的一部分,其成分反映了沉積過程中及海水與沉積物埋藏後發生的各種變化歷程。因此,間隙水的組成和海水不同。沉積物間隙水的組成,不但隨沉積的深度而異,而且有區域分布,這和海洋沉積過程、成岩過程和生物擾動有密切的關係。
研究內容
包括以下兩方面:
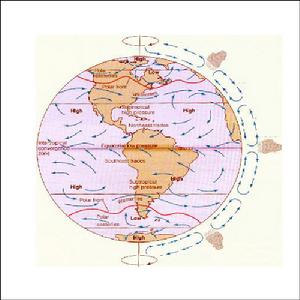 大氣圈
大氣圈① 元素或化學組分在海洋中的分布、遷移和通量。元素或化學組分在海洋各處的含量分布不同,除了受海水的鹽度或氯度(見海水鹽度、海水氯度)的影響外,主要還受海-氣界面、 河水-海水界面和海水-海底沉積層界面的物質交換的影響。這些影響,通過物質在海水中的遷移,逐漸傳給鄰近的海域。因此,要研究海洋中的物質分布,就必須研究物質的遷移過程和通量,研究某元素或某化學組分在某海區和海洋中的收支平衡。從這些通量和收支平衡出發,可以配合海洋物理學、海洋地質學和海洋生物學,研究水團的運動和混合、海-氣交換與氣候的關係、泥沙的運動與堆積、海洋生物生產力等問題。
② 元素或化學組分在海水中的存在形式。一種元素在海水介質中,往往不是以單一的化學形式出現,例如二價銅在海水中不僅以自由銅離子存在,且可形成各種無機絡合物和有機絡合物;在一定的氧化還原條件下,有些元素以兩種以上的價態同時存在,如Fe(Ⅱ)和Fe(Ⅲ)及它們的絡合態。海水中的正負離子,還有一部分締合成離子對,如MgSO孇、MgCO嬿、NaCO婣、NaSO嬄等。存在形式不同,所起的化學效應也不同。例如有機絡合的銅離子對生物的毒性,比自由銅離子低。
與鄰近學科關係
在海洋地球化學的研究中,所用的理論方法基本上來自海洋物理化學;所用的分析方法,來自海水分析化學。在研究海水中的懸浮物時,往往要涉及河口化學的內容;在研究有機物時,又與海洋有機化學交織在一起。這些學科同屬於化學海洋學,它們之間有著密切的聯繫。
發展趨勢
在海洋地球化學的研究中,越來越注重核素、微量元素和有機物的研究,並已形成海洋核素化學、海洋微量元素化學和海洋有機化學這三個新的分支。另外在海洋生物化學與海洋地球化學之間,已萌發出一門嶄新的學科──海洋生物地球化學,它既是海洋生物化學的一個分支,又是海洋地球化學的一個分支。它研究海洋生物的活動與海洋中化學物質的地球化學過程的關係。
