基本概述
 二氧化氮
二氧化氮二氧化氮是一種高度活性的氣態物質,有刺激性特殊臭味,有毒,二氧化氮易被壓縮成紅棕色液體,冷卻時液體顏色逐漸變淡,最終成為無色,二氧化氮在臭氧的形成過程中起著重要作用。人為產生的二氧化氮主要來自高溫燃燒過程的釋放,比如機動車、電廠廢氣的排放等,二氧化氮還是酸雨的成因之一,對濕地和陸生植物物種之間競爭與組成變化的影響,大氣能見度的降低,地表水的酸化,富營養化(由於水中富含氮、磷等營養物藻類大量繁殖而導致缺氧)以及增加水體中有害於魚類和其它水生生物的毒素含量。
分子結構
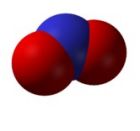 分子結構圖
分子結構圖二氧化氮分子是V形分子、極性分子。二氧化氮是含有大π鍵結構的典型分子。大π鍵含有三個電子,其中兩個進入成鍵π軌道,一個進入非鍵π軌道。NO2是一個順磁性彎曲型的分子,對稱點群為C2v。ONO鍵角為134.3°(可通過Walsh圖來解釋),N-O鍵長119.7pm。
物理性質
蒸氣壓:101.3lkPa(2l℃)溶解性:溶於鹼、二硫化碳和氯仿。
化學性質
 二氧化氮檢測儀
二氧化氮檢測儀2、二氧化氮中的N-O鍵鍵能較低,故它是一個很好的氧化劑。特定條件下可以將氯化氫、一氧化碳等還原劑氧化。有時與烴混合後,會使烴類發生爆炸性燃燒。
與水反應歧化生成硝酸和一氧化氮。該反應是工業上用氨制硝酸(奧斯特瓦爾德制硝酸法)的反應之一。3NO2+H2O─→2HNO3+NO
生成的一氧化氮遇空氣迅速氧化為二氧化氮,溶於濃硝酸即生成發煙硝酸。但二氧化氮溶於水後並不會完全反應所以會有少量二氧化氮分子存在,為黃色。因此硝酸溶液會呈現黃色。這個反應可以認為其為可逆反應,因為硝酸同時會分解。
因二氧化氮溶於水後還生成一氧化氮,所以不是硝酸的酸酐。NO2可以直接被Na2O2吸收Na2O2+2NO2=2NaNO3
3、溶於氫氧化鈉溶液歧化生成亞硝酸鈉與硝酸鈉,該反應是除去實驗中二氧化氮尾氣的常用反應。
NO2+2NaOH=NaNO3+NaNO3+H2O
4、二氧化氮分子含有一個未成對電子,因此它的很多反應類似於自由基。比如,它很容易發生二聚,且在有機合成中用作硝化劑,可以從飽和烴中奪取氫,也可以與不飽和烴或芳香烴發生加成反應。RH+NO2=R-+HONO
5、聚合反應
NO2(紅棕色順磁性氣體)很容易聚合。通常情況下與其二聚體形式——四氧化二氮(無色抗磁性氣體)混合存在,構成一種平衡態混合物。- ;
NO2到N2O4是個放熱反應,因此順磁性的NO2單體在高溫時穩定。在低溫下,二氧化氮(NO2)氣體轉化為無色的四氧化二氮(N2O4)氣體;在高溫下,由N2O4轉變回NO2。無色抗磁性的N2O4可以通過在–11.2°C的熔點熔化它的固體而得到。固態時(凝固點以下),混合物幾乎全部為四氧化二氮,二氧化氮占0.1%不到。溫度高於140°C時,則全部解離。
製備過程
工業上用空氣中的氧氣氧化一氧化氮製取二氧化氮:
2NO+O2─→2NO2
在實驗室中,可以通過氧化氮NO氧化或由濃硝酸與銅屑作用而得,也可用加熱分解硝酸鉛來製備:
2Pb(NO3)2─→4NO2+2PbO+O2↑
也可以通過五氧化二氮的熱分解來製備NO2。五氧化二氮可以通過硝酸脫水得到。
2HNO3=N2O5+H2O
2N2O5=4NO2+O2↑
生成的氣體冷凝以除去硝酸,再通過五氧化二磷乾燥,便得到較純淨的二氧化氮。銅與濃硝酸共熱也可以生成二氧化氮:
Cu+4HNO3=Cu(NO3)2+2NO2↑+H2O
主要用途
二氧化氮在化學反應和火箭燃料中用作氧化劑,在亞硝基法生產硫酸中用作催化劑。
危險說明
氮氧化物主要損害呼吸道,吸入氣體初期僅有輕微的眼及上呼吸道刺激症狀,如咽部不適、乾咳等。常經數小時至十幾小時或更長時間潛伏期後發生遲發性肺水腫、成人呼吸窘迫綜合徵,出現胸悶、呼吸窘迫、咳嗽、咯泡沫痰、紫紺等。可並發氣胸及縱隔氣腫。
肺水腫消退後兩周左右可出現遲發性阻塞性細支氣管炎。慢性作用:主要表現為神經衷弱綜合徵及慢性呼吸道炎症。個別病例出現肺纖維化。可引起牙齒酸蝕症。
環境危害:對環境有危害,對水體、土壤和大氣可造成污染。
燃爆危險:本品助燃,有毒,具刺激性。
預防措施
 二氧化氮實驗室製法
二氧化氮實驗室製法危險特性:本品不會燃燒,但可助燃。具有強氧化性。遇衣物、鋸末、棉花或其它可燃物能立即燃燒。與一般燃料或火箭燃料以及氯代烴等猛烈反應引起爆炸。遇水有腐蝕性,腐蝕作用隨水分含量增加而加劇。
滅火方法:本品不燃。消防人員必須佩戴過濾式防毒面具(全面罩)或隔離式呼吸器、穿全身防火防毒服,在上風向滅火。切斷氣源。噴水冷卻容器,可能的話將容器從火場移至空曠處。滅火劑:乾粉、二氧化碳。禁止用水、鹵代烴滅火劑滅火。
應急處理:迅速撤離泄漏污染區人員至上風處,並進行隔離,嚴格限制出入。建議應急處理人員戴自給正壓式呼吸器,穿防毒服。儘可能切斷泄漏源。若是氣體,合理通風,加速擴散。噴霧狀水稀釋、溶解。構築圍堤或挖坑收容產生的大量廢水。漏氣容器要妥善處理,修復、檢驗後再用。若是液體,用大量水沖洗,洗水稀釋後放入廢水系統。若大量泄漏,構築圍堤或挖坑收容。噴霧狀水冷卻和稀釋蒸汽。用防爆泵轉移至槽車或專用收集器內,回收或運至廢物處理場所處置。
處置儲存
操作注意事項:嚴加密閉,提供充分的局部排風和全面通風。操作人員必須經過專門培訓,嚴格遵守操作規程。建議操作人員佩戴自吸過濾式防毒面具(全面罩),穿膠布防毒衣,戴橡膠手套。遠離火種、熱源,工作場所嚴禁吸菸。遠離易燃、可燃物。防止氣體或蒸氣泄漏到工作場所空氣中。避免與還原劑接觸。搬運時輕裝輕卸,防止鋼瓶及附屬檔案破損。配備相應品種和數量的消防器材及泄漏應急處理設備。
儲存注意事項:儲存於陰涼、通風的庫房。遠離火種、熱源。庫溫不宜超過15℃。應與易(可)燃物、還原劑、食用化學品分開存放,切忌混儲。儲區應備有泄漏應急處理設備。
空氣污染
一直以來香港總是抱怨污染嚴重的內地工廠導致香港的天空總是霧氣沉沉。但分析表明,香港的污染很大程度上正是香港自己造成的。從中國官方數據來看,在中國32座主要城市中,香港的二氧化氮濃度排名第二位。
香港已經採取措施適用更嚴格的空氣品質指標,控制空氣污染的措施,比如限制當地工廠的氧化硫排放。香港還有很大的改善餘地,特別是在船舶污染方面。船舶造成的污染現在已經成為香港空氣品質問題的最大源頭之一。
2013年1月29日,北京市嚴重污染,PM2.5、PM10、二氧化氮同時超標。
你身邊的化學(一)
| 世界是由物質構成的,在我們的周圍,衣食住行各個方面都涉及到形形色色,各種各樣的物質。這些物質的組成結構和性質怎樣?物質的變化規律有哪些?化學正是研究這些問題的一門科學。可以說化學物質無處不在,正是化學才使世界變得更加絢麗多彩,魅力無限! |
無機氮化合物
氨 | 聯氨 | 三氟化氮 | 三氯化氮 | 氧氯化氮 | 一氧化二氮 | 一氧化氮 | 三氧化二氮 | 二氧化氮 | 四氧化二氮 | 五氧化二氮 | 亞硝酸 | 連二亞硝酸 | 亞硝酸 | 過氧亞硝酸 | 硝酸 | 過硝酸