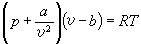實際氣體
正文
實際存在的氣體,又稱真實氣體。嚴格地說,熱機中遇到的各種氣態工質都是實際氣體,不能用理想氣體狀態方程來描述。只是在一定條件下,有些氣體(如大氣中的空氣、 鍋爐煙氣、內燃機和燃氣輪機中的燃氣等)可按理想氣體作近似處理;而另外一些氣體(如壓力比較高而溫度接近其液化溫度的水蒸汽)的性質偏離理想氣體較遠,必須按實際氣體處理。對於高壓低溫下的氣體不能忽略分子本身占有的體積和分子間的相互作用力等因素。荷蘭物理學家J.D.范德瓦耳斯於1873年導出一個後來稱為范德瓦耳斯方程的實際氣體狀態方程
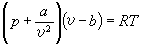
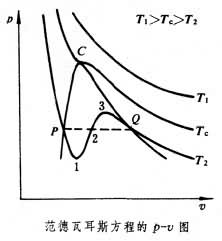
范德瓦耳斯方程是比容v的三次式,因此在不同溫度下的等溫線有如圖中的3種典型關係。T1線表示高溫下的情況,具有與理想氣體相仿的雙曲線性質。T2線表示低溫下的情況,增大壓力可把氣態壓縮成液態,中間的P-1-2-3-Q線段位於氣液兩相共存區。T0線稱為臨界等溫線,線上有一個拐點 C,叫做臨界點,相應的參數叫臨界參數。各種物質的臨界參數是完全確定的,它們的數值近似地可以由范德瓦耳斯方程算出
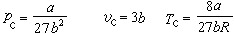

 實際氣體
實際氣體