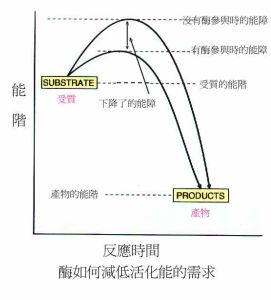
特點
 可逆反應
可逆反應2、可逆反應一定是同一條件下能互相轉換的反應,如二氧化硫、氧氣在催化劑、加熱的條件下,生成三氧化硫;而三氧化硫在同樣的條件下可分解為二氧化硫和氧氣。
3、在理想的可逆過程中,無摩擦、電阻、磁滯等阻力存在,因此不會有功的損失。
4、在同一時間發生的反應
5、同增同減
6、書寫可逆反應的化學方程式時,套用雙箭頭表示,箭頭兩邊的物質互為反應物、生成物。通常將從左向右的反應稱為正反應,從右向左的反應稱為逆反應。
7、可逆反應中的兩個化學反應,在相同條件下同時向相反方向進行,兩個化學反應構成一個對立的統一體。在不同條件下能向相反方向進行的兩個化學反應不能稱為可逆反應。
(1)“逆”:化學平衡研究的對象是可逆反應。
(2)“等”:化學平衡的實質是正、逆反應速率相等,即:v(正)=v(逆)。(3)“動”:v(正)=v(逆)≠0
(4)“定”:平衡體系中,各組分的濃度、質量分數及體積分數保持一定(但不一定相等),不隨時間的變化而變化。
(5)“變”:化學平衡是在一定條件下的平衡,若外界條件改變,化學平衡可能會分數移動。
(6)“同”:在外界條件不變的前提下,可逆反應不論採取何種途徑,即不論由正反應開始還是由逆反應開始,最後所處的平衡狀態是相同的,即同一平衡狀態。
平衡判斷
(1)速率V正=V逆(v不為0)(2)①各物質的量百分含量保持不變
②各物質的濃度不隨時間改變
③各物質的物質的量不隨時間改變
(3)如果是有氣體的反應,混合氣體的總壓強或總物質的量或氣體的平均密度不隨時間變化。(當反應兩端氣體計量係數之和不等時)
(4)如果是氣體的反應,混合氣體的平均質量不變。
(5)對於有色物質參加的可逆反應,若體系顏色不變,則反應達到平衡狀態。
(6)由於任何化學反應都伴有能量的變化,因此在其他條件不變的情況下,當總體系的溫度一定時,則反應達到平衡狀態。
平衡移動
 可逆反應
可逆反應V正>V逆:平衡向正反應方向移動
V正<V逆:平衡向負反應方向移動
(2)平衡移動方向可以據勒夏特列原理判斷
如果改變影響平衡的一個條件(如濃度、溫度、壓強等),平衡
可逆反應平衡與否
可逆反應平衡與否
就向能夠削弱這種改變的方向移動。
(3)某些特殊情況的判斷
1、對反應前後體積不變的可逆反應,V減小或增大,平衡不移動
2、充入惰性氣體(指不與體系中物質反應的物質)
a、恆溫、恆容充入惰性氣體,雖然體系的總壓強增大,但沒有改變原平衡混合物各組分的濃度,平衡不移動
b、恆溫恆壓時充入惰性氣體,體積增大,平衡混合物個組分濃度減小,相當於減小壓強,平衡向體積增大方向移動
同一平衡
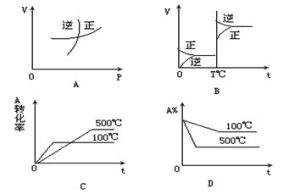 可逆反應
可逆反應(1)、當溫度、體積一定時,平衡時各物質的物質的量相同。此時各不同的起始狀態實際上相當於是一個起始狀態。
判斷的方法是將生成物按方程式完全歸至反應物或生成物,如果量相同,就是同一平衡狀態,如果量不同,就不是同一平衡狀態。
(2)、當溫度,壓強一定時(即體積可變),平衡時各物質的濃度或百分含量相同。此時各不同的起始狀態,經過將生成物歸零後,只要反應物的物質的量之比相同,就會達到同一平衡狀態。
(3)、對於反應前後氣體體積相等的反應。除了符合上麵條件外,還可以在恆溫恆容條件下,平衡時各物質的百分含量相同,但濃度不同。此時各不同的起始狀態,將生成物歸成零後,只要反應物的物質的量之比相同,就會達到同一平衡狀態。
例如:
①H2(g)+I2(g)可逆號2HI(g)[反應條件:不斷加熱]
②Cl2+H2O可逆號HCl+HClO
③N2+3H2可逆號2NH3[反應條件:高溫高壓、催化劑]
④2SO2+O2可逆號2SO3[反應條件:催化劑、加熱]
⑤CH3COOH可逆號CH3COO[陰離子團,帶一個負電荷]+H[陽離子]