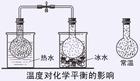
特點
化學平衡狀態具有逆,等,動,定,變、同六大特徵。
逆:化學平衡研究的對象是可逆反應。
等:平衡時,正、逆反應速率相等,即v正=v逆。
動:平衡時,反應仍在進行,是動態平衡,反應進行到了最大限度。
定:達到平衡狀態時,反應混合物中各組分的濃度保持不變,反應速率保持不變,反應物的轉化率保持不變,各組分的含量保持不變。
變:化學平衡跟所有的動態平衡一樣,是有條件的,暫時的,相對的,當條件發生變化時,平衡狀態就會被破壞,由平衡變為不平衡,再在新的條件下建立新平衡,即化學平衡發生了移動。
同:一定條件下化學平衡狀態的建立與反應的途徑無關。即無論是從正反應開始,還是從逆反應開始,或是從任一中間狀態開始建立,只要外界條件相同,達到平衡時的效果都相同。
學說發展歷史
1940-1950年
熱力學的基本規律已明確起來,但是一些熱力學概念還比較模糊,數字處理很煩瑣,不能用來解決稍微複雜一點的問題,例如化學反應的方向問題。當時,大多數化學家正致力於有機化學的研究,也有一些人試圖解決化學反應的方向問題。這種努力除了質量作用定律之外,還有其他一些人試圖從別的角度進行反應方向的探索,其中已有人提出了一些經驗性的規律。
在這一時期,丹麥人湯姆生和貝特羅試圖從化學反應的熱效應來解釋化學反應的方向性。他們認為,反應熱是反應物化學親合力的量度,每個簡單或複雜的純化學性的作用,都伴隨著熱量的產生。貝特羅更為明確地闡述了與這相同的觀點,並稱之為“最大功原理”,他認為任何一種無外部能量影響的純化學變化,向著產生釋放出最大能量的物質的方向進行。雖然這時他發現了一些吸熱反應也可以自發地進行,但他卻主觀地假定其中伴有放熱的物理過程。這一錯誤的論斷在30年代終於被他承認了,這時他才將“最大功原理”的套用範圍限制在固體間的反應上,並提出了實際上是“自由焓”的化學熱的概念。
1960-1980年
霍斯特曼、勒夏特列和范霍夫在這一方面也做了一定的貢獻。首先,霍斯特曼在研究氯化銨的升華過程中發現,在熱分解反應中,其分解壓力和溫度有一定的關係,符合克勞胥斯一克拉佩隆方程:dp/dt=Q/T(V'-V)
其中Q代表分解熱,V、V'代表分解前後的總體積。范霍夫依據一述方程式導出的下式:
lnK=-(Q/RT)+c
此式可套用於任何反應過程,其中Q代表體系的吸收的熱(即升華熱)。范霍夫稱上式為動態平衡原理,並對它加以解釋,他說,在物質的兩種不同狀態之間的任何平衡,因溫度下降,向著產生熱量的兩個體系的平衡方向移動。1874年和1879年,穆迪埃和羅賓也分別提出了這樣的原理。穆迪埃提出,壓力的增加,有利於體積相應減少的反應發生。在這之後,勒夏特列又進一步普遍地闡釋了這一原理。他說,處於化學平衡中的任何體系,由於平衡中的多個因素中的一個因素的變動,在一個方向上會導致一種轉化,如果這種轉化是惟一的,那么將會引起一種和該因素變動符號相反的變化。
然而,在這一方面做出突出貢獻的是吉布斯,他在熱力化學發展史上的地位極其重要。吉布斯在勢力化學上的貢獻可以歸納4個方面。第一,在克勞胥斯等人建立的第二定律的基礎上,吉布斯引出了平衡的判斷依據,並將熵的判斷依據正確地限制在孤立體系的範圍內。使一般實際問題有了進行普遍處理的可能。第二,用內能、熵、體積代替溫度、壓力、體積作為變數對體系狀態進行描述。並指出湯姆生用溫度、壓力和體積對體系體狀態進行描述是不完全的。他倡導了當時的科學家們不熟悉的狀態方程,並且在內能、熵和體積的三維坐標圖中,給出了完全描述體系全部熱力學性質的曲面。第三,吉布斯在熱力學中引入了“濃度”這一變數,並將明確了成分的濃度對內能的導數定義為“熱力學勢”。這樣,就使熱力學可用於處理多組分的多相體系,化學平衡的問題也就有了處理的條件。第四,他進一步討論了體系在電、磁和表面的影響下的平衡問題。並且,他導出了被認是熱力學中最簡單、最本質也是最抽象的熱力學關係,即相律,平衡狀態就是相律所表明的自由度為零的那種狀態。
吉布斯對平衡的研究成果主要發表在他的三篇文章之中。1873年,他先後將前兩篇發表在康乃狄克州學院的學報上,立即引起了麥克斯韋的注意。吉布斯前兩篇文可以說只是一個準備,1876年和1878年分兩部分發表了第三篇文章-《關於復相物質的平衡》,文章長達300多頁,包括700多個公式。前兩篇文章是討論單一的化學物質體系,這篇文章則對多組分復相體系進行了討論。由於熱力學勢的引入,只要將單組分體系狀態方程稍加變化,便可以對多組分體系的問題進行處理了。
18世紀90年代
對於吉布斯的工作,勒夏特列認為這是一個新領域的開闢,其重要性可以與質量不滅定律相提並論。然而,吉布斯的三篇文章發表之後,其重大意義並未被多數科學家們所認識到,直到1891年才被奧斯特瓦德譯成德文,1899年勒夏特列譯成法文出版之後,情況頓然改變。在吉布斯之後,熱力學仍然只能處理理想狀態的體系。這時,美國人洛易斯分別於1901年和1907年發表文章,提出了“逸度”與“活度”的概念。路易斯談到“逃逸趨勢”這一概念,指出一些熱力學量,如溫度、壓力、濃度、熱力學勢等都是逃逸趨勢量度的標度。
路易斯所提出的逸度與活度的概念,使吉布斯的理論得到了有益的補充和發展,從而使人們有可能將理想體系的偏差進行統一,使實際體系在形式上具有了與理想體系完全相同的熱力學關係式。
化學平衡狀態的標誌可概括為“一等五不變”,現以mA(g)+nB(g)==pC(g)+qD(g)為例,化抽象為具體,提高學生對此標誌的理解。 1.一等 “一等”即正反應速率等於逆反應速率,其意義是針對反應體系中同一反應物(或生成物)而言的,而不是同一反應中的不同物質。若用同一反應中不同物質來表示正反應速率和逆反應速率,必須要求兩速率反向(切忌單向速率)且兩速率之比等於其對應的化學計量數之比。 在試題中可有以下幾種具體形式出現: ⑴同一物質的正反應速率等於逆反應速率,如υA(消耗)=υA(生成)或υD(消耗)=υD(生成)。 ⑵某反應物的正反應速率與另一反應物的逆反應速率之比等於化學計量數之比,如υA(消耗):υB(生成) =m:n,或υC(消耗):υD(生成) =p:q。 ⑶某反應物的正反應速率與某生成物的逆反應速率之比等於化學計量數之比,如υA(消耗):υC(消耗) =m:p,或υB(生成):υD(生成) = n:q。 ⑷對同一物質而言,斷裂化學鍵的物質的量與形成化學鍵的物質的量相等。 2.五不變 “五不變”即反應混合物中各組分的濃度保持不變,其意義是指各組分的物質的量不變;各組分的濃度不變;各組分的百分含量不變;反應物的轉化率不變;對於全為氣體的可逆反應,當m+n╪p+q時,混合氣體總物質的量不變。 在試題中可有以下幾種具體形式出現: ⑴各組分的物質的量不變,如一定溫度的密閉容器中,A、B、C、D的分子數不再改變。 ⑵各組分的濃度不變,如外界條件不變時,對於有顏色的物質參加或生成的可逆反應,混合氣體的顏色不隨時間發生變化。 ⑶各組分的百分含量不變,如各組分的體積分數、物質的量分數、質量分數保持不變。 ⑷反應物的轉化率不變,如在一定條件下,A或B的轉化率不再改變。 以上各項既適用於反應前後氣體化學計量數之和不相等的可逆反應,又適用反應前後氣體化學計量數之和相等的可逆反應。 ⑸對於全為氣體參加的前後化學計量數改變的可逆反應,混合氣體總物質的量不變。如當m+n╪p+q時,恆溫恆容時,體系的總壓強不發生變化;當m+n╪p+q時,恆溫恆壓時,體系的總體積不發生變化;當m+n╪p+q時,恆容時混合氣體的平均相對分子質量不發生變化。 二化學平衡狀態的特殊標誌 在恆容條件下,混合氣體的密度能否作為化學平衡狀態的標誌呢?這主要看可逆反應中有無非氣態物質參加或生成。因為該條件下的氣體密度只和氣體的質量有關,若是全氣態物質參加的可逆反應,在恆容條件下,不論是否達到平衡,混合氣體的總質量都不發生變化,混合氣體的密度不發生變化,此時不能作為化學平衡狀態的判斷標誌。若有非氣態物質參與的可逆反應,在恆容條件下,只有達到平衡時,混合氣體的總質量才不會發生變化,混合氣體的密度不會發生變化,此時密度才能作為化學平衡狀態的判斷標誌。