症狀體徵
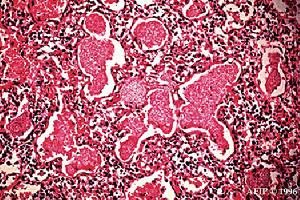 原發性滲出性淋巴瘤
原發性滲出性淋巴瘤主要表現為漿膜腔積液如腹水、胸腔積液和心包積液。臨床上病人常表現為各種受累漿膜腔大量積液及其相關的臨床表現。漿膜滲出液中含高度惡性的淋巴細胞,但沒有可檢測到的腫塊樣病灶。
疾病病因
多見於HIV 感染的病人,也可發生於HIV 血清學陰性的病人,並且偶爾見於心臟移植後的病人。
病理生理
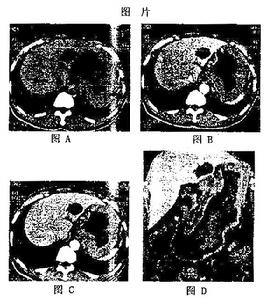 原發性滲出性淋巴瘤
原發性滲出性淋巴瘤EBV 在本病的致瘤作用尚未肯定,不像其在PCNSL 中那樣起主要作用。HHV-8 感染促進腫瘤生長的機制也未肯定。一個HHV-8 編碼的潛伏相關核抗原可能發揮重要的作用,它使HHV-8 DNA 黏附於宿主的處於有絲分裂期細胞的染色體從而使得HHV-8 附加體與子細胞分離。另有研究發現普遍激活的轉錄因子(NF-κB,可能還有其他因子)與HHV-8 感染的PEL 細胞的生存有關。通過競爭阻斷凋亡信號的實驗可以發現抑制NF-κB 將導致誘導凋亡。HHV-8 基因組編碼的病毒IL-6 是一個促進漿細胞和血管增生的細胞因子。體外研究顯示PEL 細胞能分泌IL-6,並且IL-6 的反義寡核苷酸幾乎完全抑制這些細胞株的生長,但不能抑制無HHV-8 感染的2 株B 細胞淋巴瘤的細胞株生長。以上體外實驗結果提示病毒IL-6 是促進PEL 生長的自分泌生長因子。此外,PEL 細胞表達的人類IL-10 可能是另一個重要的自分泌生長因子。
診斷檢查
診斷:以漿膜腔積液為突出的臨床表現和相應的影像學檢查結果是診斷本病的重要線索,而確診決定於滲出液中找到淋巴瘤細胞。
實驗室檢查:
1.X 線檢查 示受累漿膜腔積液。胸片和胸部CT 可發現胸腔積液和(或)心包積液以及輕度的漿膜增厚,無實質性腫塊或縱隔擴大的表現。
2.漿膜腔穿刺抽液檢查 一般均能發現惡性細胞,在形態學上腫瘤細胞介於瀰漫性大B細胞淋巴瘤(免疫母細胞變異型)和間變性大細胞淋巴瘤之間,免疫表型為CD45 和CD30 陽性,而明顯缺乏B細胞和T細胞相關的抗原表達。無c-MYC基因重排。滲出液中常可檢測到HHV-8。
其他輔助檢查:根據病情、臨床表現及症狀、體徵可選擇做心電圖、B超、生化等檢查。
鑑別診斷
主要與DLBCL 膿胸相鑑別。腫瘤細胞的免疫表型檢查有助於與其他形態學上相似的淋巴瘤如瀰漫性大B 細胞淋巴瘤和間變性大細胞淋巴瘤等鑑別。
治療方案
由於本病少見,有關PEL 的治療資料有限,目前尚無最佳治療方案。漿膜腔局部放射治療是可取的手段,常能減輕病人痛苦和延長生存期,最長可達12個月。如果由於各種原因不能放射治療或治療後復發,可選擇化學治療,方案同高度惡性淋巴瘤的治療方案。改良的CHOP 方案:第1 天環磷醯胺(CTX) 600mg/m2、多柔比星(阿黴素))45mg/m2、長春新鹼(VCR) 1.4mg/m2;第1~5 天潑尼松(Pred)60mg/day,首劑潑尼松可用地塞米松替代以減少嘔吐。每28 天為1 個療程。如果達到預期療效,可根據臨床情況再給予4~6 個療程的治療,反之,以後再用也不會有效。此外,與所有 AIDS 相關的淋巴瘤一樣,套用高強度的抗HIV 治療對控制淋巴瘤也是非常重要的。儘量提高宿主的免疫功能是治療這些腫瘤的重要組成部分。
預後及預防
預後:儘管PEL 不容易擴散至全身,但可導致局部器官組織的破壞,並且預後很差。資料顯示診斷後平均生存時間為75 天(6~240 天),屍檢後發現惡性淋巴瘤滲出液是死亡的直接原因。
流行病學
本病明顯好發於男性。
