概述
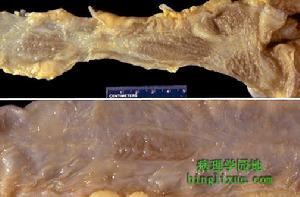 十二指腸胃反流
十二指腸胃反流體徵
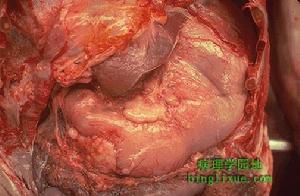 十二指腸胃反流
十二指腸胃反流患者常訴中上腹持續性疼痛,飯後加劇,制酸藥無效,甚至反而加重症狀。少數患者可表現為胸骨後疼痛,“不消化”感,常在晚間或清晨空腹時嘔吐“苦水”或膽汁,時而混有食物,嘔吐後並不緩解。患者常有貧血、體重減輕、慢性腹瀉和失眠多夢、心悸等神經官能症症狀,體徵常表現為上腹壓痛。
十二指腸反流液致病尚有以下因素:
1.膽汁在酸性介質中,特別在缺血條件下對胃黏膜損害作用加重。
2.膽汁加胰液和含有溶血卵磷脂的十二指腸液對胃黏膜的破壞作用最大。
3.胃潰瘍患者,胃內膽汁濃度較高者,胃腸吸引液中革蘭陰性需氧菌的生長增多。
4.在有臨床症狀的患者中,胃液中去氧膽酸的濃度增高。
5.胃排空遲緩,延長了膽汁和胃黏膜的接觸時問。
生理
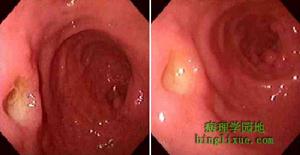 十二指腸胃反流
十二指腸胃反流多數時間處於開放狀態,少量十二指腸反流至胃內不足以引起症狀和損傷胃黏膜稱生理性DGR。大量DGR的發生常見於以下幾種情況:
(1)胃手術後DGR:術後胃DGR發生率5%~60%。術後胃由於損害了幽門正常的解剖結構和生理功能,導致幽門抗DGR屏障作用喪失,使過量的含膽汁成分的鹼性腸液反流入胃,並導致殘胃炎和膽汁性嘔吐。Griffiths報告7l例術後胃,41.9%見膽汁反流,61.5%有瀰漫性胃炎。胃手術後膽汁從十二指腸或小腸向胃反流,由於部分手術是胃空腸吻合,故確切的應稱為小腸胃反流(entro-gastricreflux),小腸胃反流的嚴重程度與術式有明顯關係,按出現的嚴重性依次排列如下:
①幽門成形術。
②迷走神經乾切斷加幽門成形術。
③胃空腸吻合術。
④BillrothⅠ式胃切除術。
⑤BillrothⅡ式胃切除術。
(2)原發性幽門功能障礙:現代的胃腸運動功能研究證明某些病理性DGR並非胃術後發生,而是源於幽門本身的缺陷,幽門括約肌功能失調,如幽門開放時間延長,幽門高壓帶功能障礙等導致大量十二指腸內容物反流入胃。1973年Fisher套用灌注式法測定幽門高壓帶的壓力為(5.3±0.5)mmHg,國內張錦坤及羅金燕等也曾用腔內金屬感測器法證實了幽門高壓帶的存在。人們認為胃十二指腸屏障壓(GDBP=幽門壓-十二指腸壓)具有抗反流作用,當GDBP降低時,則引起DGR發生。國內報告DGR病人胃十二指腸屏障壓低於正常對照組。動物實驗觀察到在消化期間移行性複合運動(interdigestivemigratingmotorcomplex,MMC)Ⅱ相時,由於非典型的節段性收縮同時伴有DGR發生。在人DCR也同樣發生在MMCⅡ相,其機制可能是:
①在MMCⅡ相時,膽汁和胰腺分泌,集聚在十二指腸。
②由於MMCⅡ相小規則的運動和壓力變化而產生一定的壓力梯度使十二指腸內壓增加而發生腸胃反流。
(3)胃排空遲緩:無論是特發性或繼發性的胃排空遲緩(如特發性胃輕癱,糖尿病胃輕癱),由於胃蠕動和幽門功能
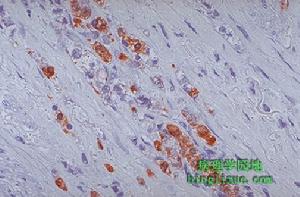 十二指腸胃反流
十二指腸胃反流(4)肝膽疾患:肝硬化門脈高壓患者有較高的DGR發生率,其機制被認為是由於門脈高壓引起循環障礙,加之繼發性高胃泌素血症,抑制縮膽囊素和促胰液素對幽門括約肌和Oddi括約肌的調節,使後兩者張力下降,膽汁和胰液反流入胃。許多膽道疾患(膽囊炎、膽結石、膽囊切除術後等)伴有明顯的DGR現象,由於膽道疾病,使膽囊儲備、濃縮膽汁的功能減退和消失,致使膽汁源源不斷地自膽管流入十二指腸,並逆行經幽門入胃。自主神經功能紊亂,過度吸菸、飲酒、情緒波動、生活規律變化等這些情況可引起胃腸激素分泌紊亂,並引起胃竇、十二指腸的逆蠕動和幽門的張力下降,導致胃、十二指腸動力功能失衡,為反流物通過幽門提供了必需的壓力梯度,促使DGR的發生。
2.膽汁反流性胃炎(BRG)的發病機制
胃手術如胃大部分切除一般在數月或數年後即由於膽汁的反流而發生殘胃炎或膽汁反流性胃炎(BRG),並產生上腹疼痛或嘔吐膽汁等症狀。大量動物實驗和臨床觀察證明,膽汁和十二指腸內容物反流到胃可引起胃炎,並發現胃炎的範圍和嚴重性與膽汁反流的程度有線性關係,並與反流成分有關。膽酸和溶血卵磷脂是損害胃黏膜的主要成分,膽鹽可以溶解來自胃黏膜的磷脂和膽固醇,並干擾胃黏膜上皮細胞的能量代謝和使溶酶體膜破裂,同時對胃黏膜表面的黏液有清除作用,損害胃黏膜屏障,使H+反向彌散增加,從而引起肥大細胞釋放組胺,導致胃炎發生。大量的DGR不僅直接損害胃黏膜發生胃炎,而且和胃潰瘍的發生有關,RhodesJ等(1972)發現胃潰瘍的病人DGR高於正常人,其機制可能是通過細胞毒性膽鹽和胰蛋白酶的過量首先損傷胃黏膜,繼而發生增生性改變,腸化並形成潰瘍。此外,DGR可同時反流入食管,在反流食管炎和Barrett食管發生機制中起重要作用,稱為十二指腸胃食管反流(DGER)。有的研究報告DGR與食管癌和殘胃癌發生也有關。
診斷
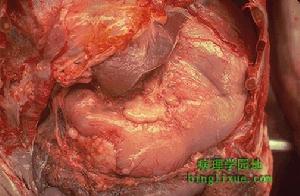 十二指腸胃反流
十二指腸胃反流2.胃液Na+測定十二指腸液Na+濃度較高,並穩定在146mmol/L左右,比腸液中膽汁的濃度還穩定(膽汁是間斷的從膽道排入腸道),同時反流入胃中的Na+不被胃酸破壞和失活,並具備檢測方便的特點,可作為DGR的一個診斷指標。有人研究,在胃腔pH值監測同時抽取胃液定時測定其Na+和膽酸含量,發現三者之間有良好的線性關係,Na+濃度的檢測不失為判斷DGR的一種簡單易行的方法。本院曾對DGR(+)胃炎組(28例)和DGR(-)胃炎組(24例)測定空腹胃液Na+濃度,DGR(+)組為(62.87±8.31)mmol/L,DGR(-)組為(32.18±4.67)mmol/L,2組Na+含量相差顯著(P<0.01)。
3.空腹胃液膽酸測定膽酸常見於有DGR的胃內,且不被胃酸破壞,可作為十二指腸液的“標記物”。測定其在胃液內的濃度對了解反流程度有重要意義,但是插管過程的刺激易造成人為反流,即使抽取空腹胃液,其膽酸含量將受影響,可出現假陽性結果;另一方面,十二指腸液中出現膽汁依賴於膽囊的排空,膽汁若不排泄入十二指腸,會造成假陰性結果。套用99mTc-EHIDA掃描顯示膽囊收縮平均間隔時間為70min。因而持續收集胃液,測定其膽酸含量可提高DGR診斷的陽性率。有作者採用持續抽吸胃液90min,以總膽汁酸量≥100μmol/h或膽酸濃度≥1000μmol/L為診斷DGR的標準,與放射性核素相比較,前者符合率為80%,後者為70%。
4.微量膽紅素測定24h膽汁反流監測儀(24-hourbilerefluxmonitoring)DGR物中的主要成分是鹼性腸液、膽汁及胰酶等。用膽紅素的存在來評估是否有DGR發生,生理性抑病理性。晚近套用光纖維感測技術設計的微量膽紅素檢測儀(fideroptictechniquefor24-hourbilerefluxmonitoring)(Bilitec,2000)問世。膽紅素的特徵吸收光譜峰值在450nm。套用此技術,不僅可以定性DGR,同時也可定量膽汁反流的多少,通過多項參數的分析,對評估膽汁反流有重要意義,同時也可監測胃食管膽汁反流的情況,常用於Barrett食管,酸性反流藥物治療無效的食管炎,胃切除後殘胃炎的評價等。檢查時需空腹6h以上,從鼻腔插管,將感測器置於下食管括約肌下5cm處,進標準餐(限制酒精,飲料和酸性食物以及色素等)固定導管,佩帶式記錄儀進行24h可移動式監測、結果經微機軟體處理分析包括24h膽汁反流總次數,反流超過5min的次數,最長反流時間以及反流總時間的百分比等。該技術所檢測的是膽汁反流,因此受MMC時相的影響。在某些肝病如先天體質性黃疸(Gilbert病和DubinJohnson綜合徵)時則不適用。另外,在酸性環境中,由於膽紅素轉化為二聚體,光吸收峰值由453nm變為400nm,其檢測值將降低。
檢查
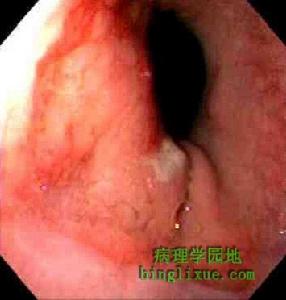 十二指腸胃反流
十二指腸胃反流2.放射學檢查早期診斷DGR是採用插管法,將導管插入十二指腸,注入硫酸鋇溶液,在X線透視下觀察鋇劑反流入胃的情況,由於插管導致的患者不適感和對幽門生理功能的影響,且在判斷常常時有主觀色彩,因此假陽性率較高。現今此法基本被廢除。
3.胃腸壓力測定用壓力感測器或灌注式導管測定胃竇、幽門及十二指腸壺腹部的壓力。DGR患者大多數有胃竇、幽門壓力降低、十二指腸壺腹部壓力上升。
4.胃內鹼灌注激惹試驗當胃內灌注鹼性溶液(0.1NNaOH20ml/次)後出現上腹痛、伴有或不伴有噁心者均列為灌注陽性。此試驗敏感,簡單易行並具有特異性。
5.核素檢查採用通過肝由膽汁排泄的核素閃爍圖,非侵入地測定反流,無機械刺激且在近似生理條件下進行,能較精確的測定有無反流及反流量。目前國內外學者一致認為99mTcEHIDA放射性核素掃描技術是DGR定量的“金指標”,優於胃鏡檢查及空腹膽酸測定。本方法敏感性較高,當胃內放射性與靜脈注入總量比率>1%時即呈陽性,且重複性好(75%),已成為十分有價值的研究工具和臨床診斷手段。但放射性核素檢查也有一定缺陷,因胃的解剖位置難以準確定位而降低了此技術的準確性,以致影響DGR的定量結果。胃的核素集中區常常難以代表胃的真實輪廓,特別是胃竇部更難以描繪,肝、十二指腸-腸襻的覆蓋也將影響其準確性,雖然可以限定範圍,但這些區域的活性常不恆定。患者臥位或立位時身體活動加大核素集中區判定的難度。以上諸因素,可造成診斷偏差。
6.超聲檢查KingPM等(1984)首先採用實時超聲法檢測DGR,隨後HauskenT等(1991)用彩色都卜勒超聲技術觀察胃內容物的流動和反流,此法代表DGR評估技術的飛躍,非侵入性,可重複性好,並能量化DGR。具體步驟如下:禁食1夜取坐位,在2min內攝入1份液體試驗餐(400ml肉湯或牛奶),將探頭置於幽門平面水平,觀察胃竇,幽門及十二指腸近端。根據彩色信號(液體流向遠端呈藍色,反流為紅色)判斷是否反流,其DGR的嚴重程度可根據其頻率和強度進行評估。該技術不足之處是目前只能用液體試餐測定DGR,同時由於腸脹氣或腹壁脂肪層厚等因素影響,常常帶來一些技術的困難。
鑑別
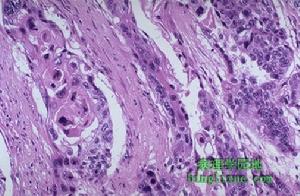 十二指腸胃反流
十二指腸胃反流2.嗜酸性胃炎是以胃壁任何一層或各層都有顯著的嗜酸性細胞浸潤為特點的慢性胃炎。本病好發於有過敏性狀態或外周性嗜酸細胞增多症患者,也可能是嗜酸性胃腸炎的一部分。病變最易侵犯胃竇部黏膜,兒童患者胃竇部受累幾乎達100%。黏膜浸潤可引起糜爛,黏膜活組織檢查時可見嗜酸細胞侵入上皮細胞層內,並可見上皮細胞壞死、再生,活化的嗜酸細胞脫顆粒,提示組織損傷系由嗜酸細胞釋放毒性物質所致。嗜酸性胃炎也可侵入胃竇肌層,引起胃竇局部僵硬、狹窄及排空障礙。
治療
 十二指腸胃反流
十二指腸胃反流①考來烯胺(消膽胺)是一種陰離子交換樹脂,與膽汁酸有親和力,服用後可與膽酸結合,減少可溶性膽酸的濃度,防止胃炎的發生,用藥時間超過3個月,並要求補充脂溶性維生素。
②多潘立酮是胃多巴胺受體阻滯藥,加強胃腸蠕動,促進胃排空,減少膽鹽和黏膜接觸時間。
③新一代全胃腸道促動劑西沙必利(普瑞博思)是5-HT4受體激動劑,通過興奮膽鹼能受體而增加腸肌間神經叢乙醯膽鹼的釋放,協調胃竇、幽門十二指腸運動增加胃排空,對控制DGR的發生有較好的療效。
④由於膽酸需要在H2的介導下才構成對胃黏膜的損傷,因此抗分泌藥對保護胃黏膜有一定的作用。
⑤熊去氧膽酸(UDCA)可抑制膽酸的合成,服用後膽汁中有大量的熊去氧膽酸排出,使去氧膽酸和石膽酸的濃度相對減少,故有較好療效。
⑥鋁碳酸鎂(胃達喜,Talcid)是層狀晶格結構體,能迅速中和胃酸,可逆性失活胃蛋白酶,持續阻止膽酸和溶血卵磷脂對胃黏膜的損傷,增強胃黏膜保護因子作用,治療膽汁反流性胃炎總有效率可達90%。此外,雙八面體蒙脫石(思密達)、複方谷氨醯胺(麥滋林-S)、複方三矽酸鎂(蓋胃平)、甘珀酸鈉(生胃酮)和支鏈澱粉等均可選用。
