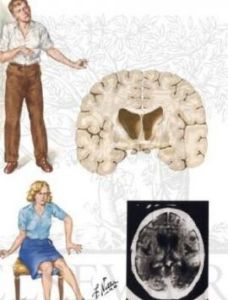
概述
 亨廷頓舞蹈病
亨廷頓舞蹈病歷史
1872年首先由G.·亨廷頓予以描述。該病的首發症狀常可見面部抽搐,其後逐漸波及其他部位,可見震顫及隨意運動失去控制;從初起時的動作笨拙、不能完成精細動作,逐漸發展成周身不自主的舞蹈樣動作或舞蹈手足徐動症;言語、吞咽功能亦日漸受損,最終甚至無法完成此類動作;情緒變得壓抑;痴呆多在不自主動作出現數年後發生,但亦可先由智慧型減退起病。此外幻覺、妄想和其他一些常見的症狀與精神分裂症極為相似。許多亨廷頓病患者,特別在病程早期,可被誤診為精神分裂症,但晚期患者的智力、記憶力和運動障礙較精神分裂症患者更為嚴重。發病年齡通常在30~40歲間,某些病例亦可早在20歲或晚至60歲發病,起病於兒童期的患者雖較罕見,但症狀略有不同,且病情惡化更為迅速。本病病程呈進行性,預計發病後15年左右死亡。死亡原因常為心力衰竭,呼吸困難或肺炎等並發病所致。病因
亨廷頓舞蹈病是一種全外顯性的常染色體顯性遺傳病。在確認基因位點後,又經過多年研究才找到它的致病基因Htt(Huntingtin)。這個基因編碼Htt蛋白(Huntingtinprotein),在它的第一個外顯子中,包含了重複的CAG三聯密碼子。在HD中,這個三聯密碼子的重複次數會出現異常增加。擁有多36次CAG重複三聯子的個體會患病。但如果重複次數為36~39個,則全外顯性較低。三聯子重複次數不穩定,在遺傳到下一代時次數可發生改變。在大腦中表達的變異Htt蛋白通過不同分子機制導致神經功能退化。變異蛋白不僅促使該蛋白的異常功能增加而且導致正常功能的喪失。正常Htt蛋白本身具有多種細胞功能,Htt蛋白變異則導致這些功能障礙。蛋白變異常常首先表現為相關基因的表達異常,已有研究顯示HD紋狀體中有關神經傳導的基因出現表達異常。另外,CAG的異常重複可以大規模影響分子間的相互作用,導致細胞內蛋白運輸紊亂。Htt蛋白變異不僅打亂線粒體功能相關蛋白的基因調節,而且還和線粒體膜表面的蛋白反應,損傷呼吸鏈功能,妨礙線粒體固定到微管,影響線粒體動態融合與分裂並使鈣傳輸增加。變異蛋白也可抑制自噬功能,促進凋亡,改變神經營養供能及細胞胞漿內的生物和信號合成。HD的患病率在不同人群中變異很大,西方人口的患病率是十萬人中有4~8例。最近研究顯示中國/日本HD患病率為0.40,而歐洲/北美以及大洋洲患病率為5.7。在中國文獻中以前只有少數的個案報導,但隨著對此病的認識,病例報導會逐漸增多。
表現
1、病因主要是家族遺傳或者基因受到外部刺激而發生突變。只要自雙親任一方遺傳缺陷的基因,皆會表現出病徵。2、病徵主要表現為情緒異常,變得冷漠、易怒或憂鬱。
3、手指、腿部、臉部或身體出現不自主動作。
4、智力衰減,判斷力、記憶力、認知能力減退。
5、一般來說,導致患者死亡的原因是因為突然跌倒或者感染其他併發症。目前藥物可以控制、減緩情緒波動和動作問題,但無法徹底根治該疾病。
6、這種精神病在人的幼年期和少年期就開始有表現,但病狀並不明顯,到了成年期各種症狀就會一齊出現:行為失常、身體各部分不自覺地動作、精神混亂、神經衰弱,甚至死亡。亨廷頓氏舞蹈症患者走路不穩,說話含糊,常被人誤認為喝醉了酒。研究人員懷疑—些塞勒姆的巫婆曾患有這種病。
7、這種疾病是由於維持生命體基本活動的腦神經節內神經的大量死亡引起的,這一區域正控制著人的行動和認識。
8、一般患者在中年發病,逐漸喪失說話、行動、思考和吞咽的能力,病情大約會持續發展15年到20年直到最後死亡,並最終導致患者死亡。這種病的遺傳幾率為50%。
檢查
本病主要累及基底節和大腦皮質,以尾狀核、殼核萎縮最明顯,出現神經細胞脫失及膠質細胞增生。大腦皮質(特別是額葉)萎縮,特別是III、V和VI層的錐體神經細胞和小神經元脫失,沒有膠質細胞增生。神經細胞脫失亦可累及丘腦腹外側核、下丘腦、黑質網狀結構、橄欖體、薄束核和楔束核、白質和間腦核等部位。早期影像學檢查多無特殊表現。隨病情進展,典型表現為對稱性尾狀核萎縮,側腦室前腳尾狀核區呈球形向外膨起,呈“蝴蝶征”。病情進一步發展可以出現不同程度的皮層和皮層下的萎縮。
診斷
根據陽性家族史、典型的舞蹈樣運動、精神障礙和進行性痴呆、以及基因檢測陽性結果而加以診斷。治療
現有的幾種HD療法可以歸類為對症治療或對因治療。對症治療的目的是根據醫生客觀診斷和患者主觀回饋信息,直接緩解患者病症。對症治療還可以進一步分類。根據針對運動、精神和認知方面的不同的主要症狀的治療,可分為HD特異和HD非特異對症治療。對因治療則包括直接的基因療法和其他間接的分子療法。前者把變異基因和它的轉錄產物作為唯一的病因,直接進行治療;後者的目的是更正導致疾病的複雜分子和神經相關通路。雖然對因治療目前還無法實現,但針對上述不同的分子通路,正在開展大量的研究,以期減緩疾病。除此之外,我們還必須重視HD患者的護理以支持其家人。由於針對患者的需要進行症狀治療非常重要,最好能通過多學科合作來實施。在發病前和疾病第一階段,這個多學科的團隊可以包括神經專科醫生、精神科醫生和遺傳諮詢師,隨著患者病情的變化,則需要理療師、語言和職業治療師、護理人員及其他專業醫療人員的加入。而臨終關懷和末期處理也越來越受到重視。治療的主要目的仍然是改善患者的生活質量。根據患者的需要,如果出現包括恥辱感、身體損傷,步態不穩,工作困難和睡眠不安等症狀,則表示需開始服用治療舞蹈症的藥物。當患者合併出現精神病或攻擊行為時則首選精神類藥物。丁苯喹嗪是美國食品藥品局(FDA)批准治療HD舞蹈動作的藥物之一。丁苯喹嗪的主要機制是抑制單胺囊泡轉運。其用藥量大時,可以顯著減輕舞蹈症狀,但如果停止用藥,舞蹈症狀會加重。使用此類藥物須注意其副作用,包括運動遲緩伴震顫。還需注意抑鬱症。精神類藥物還包括奧氮平,利培酮,或泰必利。注意用藥時需要根據患者反應調整劑量。對於一些特定的患者,有時可能需嘗試幾種不同的精神類藥物,從而找出最合適的。巴氯芬和苯二氮卓可對疾病末期的運動障礙治療有效。而化學神經阻滯劑如肉毒桿菌毒素可治療局部痙攣,如磨牙症或局灶性痙攣反射亢進。同時,物理治療也很重要。近期研究顯示,重點訓練姿勢和步態對HD患者有很大幫助。
由於對藥物治療HD認知障礙的研究很少,目前仍無藥物顯示有效。
對於強迫,和易激惹症狀,可以建議採取階梯性治療方法。在輕度認知障礙的患者中,可先採用五羥色胺再攝取抑制劑,並可同時結合行為治療。如果同時出現抑鬱,焦慮和強迫症行為,五羥色胺再攝取抑制劑也可為一線用藥。用藥調整到最適劑量後,就應合併用藥治療。也可採用行為治療。
吞咽困難一般出現在疾病的後期,目前已有指南對吞咽食物(應在認知障礙影響到學習能力前開始指導),包括正確的準備食物以及在監控環境下提供食物給出指引。用適當方法增加患者能量攝入非常重要。Huntington舞蹈病目前無特異有效的治療方法。一些藥物可以緩解症狀但不能阻止疾病的進展。病因治療通過基因水平或細胞水平進行,但均處於研究階段。
腦深部電刺激術因其獨特的優勢已開始套用於運動症狀相對進展較快的患者。電刺激的靶點主要位於雙側蒼白球內側部,而且有研究發現電刺激不僅能夠改善HD患者運動症狀,而且也能改善情緒、體力以及日常生活能力。因此,對於高級皮層功能受累較輕的患者,運動功能的改善能夠顯著提高生活質量,延長獨立生活的時間。
作為一種新興治療手段,基因治療,尤其是RNAi、神經營養因子基因導入等方法,在亨廷頓病動物模型實驗中已顯示出一定療效。但是,從動物實驗到人體試驗的轉化仍是一條漫長的道路。
HD患者及其親人同時還會面對不少社會及醫療問題,這都需要受過訓練的專業人士合理解決。
預防
HD目前已經有不少對症療法可用,綜合看護計畫也使患者及其家人受益。臨床研究及看護項目已非常到位,在世界範圍內建立起了包括診所、研究人員和醫療組織的大型網路。在研究人員、醫務工作者、患者、社會環境的相互協作下,相信HD患者能夠得到早期診斷和最優治療。現狀
 亨廷頓舞蹈病研究
亨廷頓舞蹈病研究研究人員說,他們現在已掌握了這種基因,可以著手研究這種由於神經系統衰退而引起的精神病了。這種病通常總是侵襲30到40歲左右的人。患者看似正常,實則身體已嚴重受損,在10年到20年間就會死去。亨廷頓氏舞蹈症折磨著3萬名左右的美國人,另有15萬美國人處於染病的險境。眾所周知的民間歌手烏迪·古斯里便是它的犧牲品之一。在20世紀80年代初,人們發現了引起亨廷頓氏舞蹈症的基因線索,當時正值新形態的分子遺傳學的起步階段,研究人員不久就遇到了一連串兒的麻煩,使這項研究變得更具有挑戰性和令人無法抗拒的魅力,也因此吸引了許多傑出的生物學家。
令科學家們感興趣的是,引起這種疾病的基因突變與他們不久前在引起其他疾病的基因中所見到的一樣。那是一種分子摺疊反應,其中一小段基因被反常地延長開來,並不斷地發生重複。研究人員說,在把這種突變作為一種準確預見疾病的方法前,還要做大量的工作。發現了致病基因,並不意味著就找到了治癒這種病的方法。但這一發現對破解亨廷頓氏舞蹈症之謎提供了實質性答案。這一研究成果被發表在《細胞》雜誌上,其成就是令人信服的,因為它的發現者是亨廷頓氏舞蹈症聯合研究組。這是一次罕見的持續性科學界合作行動,參與研究的6個實驗室分別設在美國、英格蘭和威爾斯,這些實驗室共同分享彼此的研究資料和構想。各地的生物學家,即使是那些曾與這個聯合研究組競爭過的,都不由自主地為這一發現感到高興和由衷的欣慰。
成果
日本理化研究所2010年3月1日宣布,該機構研究人員開發出一種針對亨廷頓舞蹈病等類型疾病的基因療法,並成功改善了患亨廷頓舞蹈病實驗鼠的症狀。日本理化研究所在新聞公報中介紹說,谷氨酸是按照基因中胞嘧啶、腺嘌呤和鳥嘌呤這3種鹼基的特定序列編碼合成的。在正常情況下,3種鹼基的序列會重複20次左右,而如果這種重複超過40次,就會形成異常延長的多聚谷氨醯胺。這種物質堆積在神經細胞中,引發神經細胞功能異常或死亡,最終導致多聚谷氨醯胺疾病,這類疾病的最典型代表就是亨廷頓舞蹈病。亨廷頓舞蹈病患者通常在30歲至50歲時發病,患者會出現不可控制的顫搐,並有可能發展成痴呆。理化研究所研究人員開發出的新基因療法,主要是促進異常堆積的多聚谷氨醯胺分解。具體做法是,令兩種肽——“QBP1”和“HSC70bm”融合形成另一種肽“HQ”。接著,令“HQ”在細胞中表達,它就會和多聚谷氨醯胺形成一個複合體。這個複合體會被搬運至分解廢棄蛋白質的溶酶體,從而被分解。對患亨廷頓舞蹈病實驗鼠進行的實驗中,研究人員令“HQ”在亨廷頓舞蹈病中最易受損的大腦紋狀體內表達,發現實驗鼠體內多聚谷氨醯胺的表達量減少。與此同時,實驗鼠運動機能的測試成績得到改善,壽命也延長了。阿爾茨海默氏症、帕金森氏症等都被認為與異常蛋白質在腦部的堆積相關。因此,這項新基因療法除了可以治療亨廷頓舞蹈病等多聚谷氨醯胺疾病外,也可套用於治療阿爾茨海默氏症等疾病。廣東科學家領銜的國際研究團隊經過四年努力,利用基因編輯技術(CRISPR-Cas9)和體細胞核移植技術,將人突變的亨廷頓基因敲入豬的內源性基因中,並進一步培育出患“亨廷頓舞蹈病”的豬。研究發現,“亨廷頓豬”模型不僅能模擬亨廷頓舞蹈症病人在大腦中特異神經元選擇性死亡的典型病理特徵,而且表現出類似亨廷頓舞蹈病“舞蹈樣”的異常行為。更重要的是,這些病理特徵及異常行為都可以穩定地遺傳給後代。2018年3月30日凌晨,這項研究成果在生物學頂尖學術期刊《細胞》線上發表,研究由暨南大學粵港澳中樞神經再生研究院教授李曉江、中國科學院廣州生物醫藥與健康研究院研究員賴良學、美國Emory大學教授李世華領銜的國際研究團隊共同完成。