病因
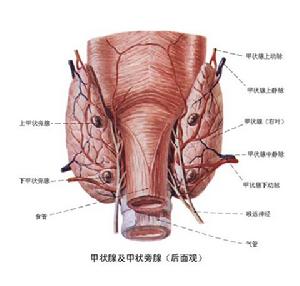 甲狀腺結構圖
甲狀腺結構圖文獻報導,PTML40%~85%可同時合併慢性淋巴細胞性甲狀腺炎(Hashimoto’s thyroiditis,HT)。認為,HT的發病因素,可能由於呼吸道病毒感染,導致機體免疫反應而發生。這間接證明PTML可能存在同樣的發病因素,但兩者的關係至今仍未闡明, 究竟是甲狀腺淋巴瘤中的淋巴細胞浸潤導致了HT的發生,還是由於甲狀腺炎中的淋巴細胞長期慢性刺激,誘導了PTML的發生?相信對兩者的關係的闡明, 必將有助於發現PTML的發病原因。
發病機制:
PTML絕大多數是B細胞來源的非霍奇金氏淋巴瘤,偶可見T
 原發性甲狀腺惡性淋巴瘤
原發性甲狀腺惡性淋巴瘤細胞來源。以往的甲狀腺小細胞癌已統一歸為PTML。PTML通常為中度惡性的瀰漫性大細胞淋巴瘤,已證實其中69%主要為黏膜相關性淋巴樣組織來源的淋巴瘤, 黏膜相關淋巴樣組織(mucosa associated lymphoid tissue,MALT)是指病理免疫學證實的一組具有相似分布特點及生物學行為的淋巴組織,主要位於胃腸道, 肺支氣管、咽黏膜層。與其相關的免疫活動主要位於黏膜,具有典型“淋巴細胞循環”現象。甲狀腺為循環淋巴細胞優先落戶的MALT器官,PTML多數具有MALT淋巴瘤的特點。
1.病理分類 沿用NHL組織病理學分類,Working Formulation分類如下:
(1)高度惡性(低分化):大細胞免疫母細胞性;淋巴母細胞性;無分葉小細胞性。
(2)中度惡性(中度分化):瀰漫性,分葉細胞;瀰漫性,混合大、小細胞;瀰漫性大細胞。
(3)低度惡性(高分化)。
2.臨床分期 沿用Ann Arbor分期。
流行病學
絕大多數為非霍奇金病, 既往認為發病率為0.6%~5%。Banfi報導在非霍奇金惡性淋巴瘤的病人中,表現為淋巴結外淋巴組織病變的占25%~30%,其中有10%的病人累及甲狀腺,甲狀腺惡性淋巴瘤是全身受累的部位之一。但在有甲狀腺惡性淋巴瘤表現的病人中,實際上原發於甲狀腺的惡性淋巴瘤<10%。Wright等報導,PTML的發病率近年有上升趨勢,原因可能是診斷水平的不斷提高和老年人群的不斷增多。 認為,PTML的發病率為2%~8%,占所有非霍奇金氏惡性淋巴瘤的2%~3%。
臨床表現
PTML的臨床表現常有:
1.常發生於中老年人,其中約23%亦可發生於小於40歲年輕人。患病人群平均年齡約59歲。
2.女性病人多於男性,男女比例為1∶2.7。
3.病人常表現為甲狀腺短期迅速增大,並可出現氣管、喉部受壓症狀, 文獻報導甚少有發熱、夜汗、體重明顯減輕等所謂“B”症狀。
4.多數病人就診時可觸及甲狀腺腫塊,腫塊大小不等、質地硬實,常固定,活動度差。可累及局部淋巴結及鄰近軟組織,40%可出現頸部淋巴結腫大。
5.30%的病人伴有言語不清。
6.20%病人出現聲嘶,10%出現呼吸困難,7%伴有甲狀腺功能低下表現。
7.遠處轉移多見於縱隔,可見骨、脾臟侵犯。
併發症:
部分病人可合併喬本甲狀腺炎(HT),伴有結節性甲狀腺腫約30%。起病至出現症狀的時間約為4個月,最長可達3年。
診斷
臨床診斷PTML 有一定困難。術前診斷率低於50%。近年隨著影像技術及診斷技術的進步,術前診斷率有較大的提高。
1.臨床上如出現下列情況應該高度懷疑本病:①甲狀腺腫塊短期迅速增大,同期伴頸部淋巴結腫大。②早期即出現聲嘶、呼吸困難。 ③體檢胸部X光片提示縱隔增寬, 氣管受壓。④病人既往有HT病史。⑤甲狀腺功能檢查提示TG、TM明顯升高。
2.輔助檢查 血常規、骨髓穿刺、全身骨掃描等可排除血液疾病;細針穿刺抽吸細胞學檢查(FNAC)、活組織病理檢查可明確診斷;X線檢查、CT掃描、B超等,有助於發現轉移病灶。
鑑別診斷:
治療前必須排除甲狀腺良性結節。 如腺瘤、結節性甲狀腺腫、常見類型的甲狀腺癌以及甲狀腺炎 ,必要時採取FNAC及相關的免疫學指標檢測,可基本上予以排除。
實驗室檢查:
1.血液檢查 血常規提示有無貧血及粒細胞減少等情況。
2.甲狀腺功能檢查 提示TG TM明顯升高。
3.骨髓穿刺 排除血液病。
4.細針穿刺抽吸細胞學檢查(FNAC) 可同時進行免疫學指標檢測和DNA流式細胞學檢查,進一步明確診斷。如免疫組織化學染色顯示CD20陽性,提示B細胞來源淋巴瘤。有時可見免疫球蛋白升高 特別是λ、κ輕鏈過度表達,免疫球蛋白基因重排檢測提示克隆聚集性。FNAC可滿足臨床診斷要求。若懷疑難以鑑別的HT,則必須輔以上述免疫指標檢測,必要時進行手術活檢。
其它輔助檢查:
1.X線胸片 可顯示縱隔增寬 氣管受壓等,並有助於了解有無胸腔轉移。
2.CT掃描 胸部及腹部CT,有助於了解有無縱隔、腹腔內外的淋巴組織病變。
3.B超檢查 肝脾B超檢查,排除肝、脾臟器侵犯。
4.淋巴管造影 若出現淋巴水腫,則需行核素淋巴管造影以了解梗阻位置。
治療
關於PTML的治療原則至今仍有爭議。早期許多學者主張手術切除。隨著對惡性淋巴瘤研究的深入,已證實淋巴瘤具有高度放射敏感性和化療敏感性。手術切除在PTML治療中的套用逐漸下降。甚至已降為僅作為活檢的手段 在1950~1960年放射治療興起的年代 多數學者主張實行單一的放射治療方案 隨著20世紀80年代化療藥物的興起,許多學者又主張化療。近年多個前瞻性研究指出,聯合治療可能是原發性甲狀腺惡性淋巴瘤的最適宜方案, Doria等分析11個系列共211例Ⅰ、Ⅱ期病人 發現總的復發率約30%;接受聯合放療化療者則降至5.1%~7.7%,而局部復發率則由12.6%降至2.6%。因此指出,聯合治療明顯有助於降低復發率而提高總的生存率。
關於PTML的治療比較統一的認識有如以下方面:
1.若ⅠΕ、ⅡΕ期,原則上採取外科手術切除, 方案為甲狀腺切除或加頸淋巴清掃,不主張擴大根治術。術後輔以放療或化療。
2.若ⅢΕ、ⅣΕ期,原則上採取放療聯合化療方案。當甲狀腺腫塊明顯增大,有壓迫症狀時,可採用手術姑息切除,以解除壓迫。必要時氣管切開。
3.當FNAC無法證實診斷而必須開放活檢時,可進行手術切除 術後根據分期 輔以放療或聯合放療、化療。
4.放療劑量 一般為30~50Gy 放射部位主要採取區域淋巴結區和縱隔區。
5.化療方案 一般選用CHOP(環磷醯胺、多柔比星、長春新鹼和Pred)加上博來黴素、或甲氨蝶呤,或多柔比星(阿黴素)方案,平均周期為6個療程。
6.治療後常見併發症。
(1)放射性食管炎 皮膚紅疹等,後期可發生心肌炎、限制性心包炎。
(2)化療引起的骨髓抑制,病毒性肺炎(博來黴素)。
預後:
業已證實,中度惡性的, 或低度惡性的PTML、或合併HT者預後較好。而腫瘤的生物行為狀態、治療方案和縱隔受累明顯影響預後。Ⅲ、Ⅳ期 縱隔有轉移者預後差。而年齡、性別、乳酸脫氫酶、腫瘤大小和呼吸道受壓等情況,以及有無“B”症狀對預後影響不明顯,但病人的病理分期 免疫狀態及腫物生物行為狀態是影響PTML,預後的重要因素。
PTML治療後總的生存率為50%~70%。臨床各期的5年生存率分別為Ⅰ期80%、Ⅱ期50%、Ⅲ期和Ⅳ期低於36% 治療後復發大多數在4年內,死因多為惡性淋巴瘤進展性急變以及腹腔實質臟器轉移。
案例分析
例1.女,62歲。因頸前漸大腫塊9 a 伴明顯增大、消瘦 0.5 a入院。曾在當地醫院診斷為“甲亢”。查體:一般情況可,淺表淋巴結不腫大,心肺腹正常,雙側甲狀腺腫大(Ⅱ度),雙側均可捫及多個結節,大者約2.5 cm×3 cm,質硬,與氣管粘連。T3,T4,TSH正常。甲狀腺B超:雙側甲狀腺及峽部實性占位性病變;核素掃描:冷結節。入院診斷:雙側結節性甲狀腺腫。行雙側甲狀腺次全切除術。病理報告:①慢性甲狀腺炎,②間質淋巴細胞顯著增生,以幼稚淋巴母細胞為主,並有間變性,符合惡性變淋巴瘤——瀰漫性非霍奇金B細胞型,中度惡性,LCA(+),L26(+),VCHL(-)。術後化療(CHOP方案),至今1 a余健在。
例2.女,56歲。頸前腫塊1a,明顯增大1月余入院。查體:一般情況好,淺表淋巴結不腫大,心肺腹正常,右側甲狀腺可及一4cm×3cm腫塊。T3,T4,TSH正常。核素掃描:冷結節。入院診斷:右側甲狀腺瘤惡性變?行右側甲狀腺腺葉切除術,術中腫塊未累及腺體外。病理報告:低度惡性B細胞型淋巴瘤,慢性甲狀腺炎。術後化療至今2 a余健在。
原發性甲狀腺惡性淋巴瘤(PMLT)是結外淋巴瘤的一種,占結外淋巴瘤的2.2%~6.5%,占所有甲狀腺癌的1.3%~2.5%。一般認為PMLT好發於女性,以老年人多見。發生原因可能與慢性淋巴細胞性甲狀腺炎有關,其發生可能是由於淋巴外套B細胞遷居於甲狀腺組織,早期表現為橋本病,由於抗原不斷刺激而轉化為惡性淋巴瘤。本組2例均為老年女性,B淋巴細胞型淋巴瘤合併慢性甲狀腺炎。
PMLT術前診斷難,容易誤診,病理診斷是唯一的確診方法。結合文獻及的資料,其臨床表現及病理有如下特點:①老年女性多見;②迅速增大的頸部腫塊或原甲狀腺瀰漫性腫大,短期內生長迅速;③可伴有頸部壓迫症狀如吞咽困難、聲音嘶啞或氣管壓迫症狀。④否認既往有淋巴系統疾病,無全身淺表淋巴結腫大;⑤核素掃描示“冷結節”;⑥大多甲狀腺功能正常或低於正常範圍;⑦組織學顯示甲狀腺的正常結構基本消失,為瀰漫浸潤的淋巴樣瘤細胞所代替,瘤細胞不僅侵入甲狀腺實質而且侵犯被膜,侵入甲狀腺濾泡的瘤細胞可取代濾泡,並能除外不典型淋巴性甲狀腺腫或小細胞甲狀腺癌者。
大多數作者認為手術是重要的,並主張應儘可能多的切除腫瘤,包括全甲狀腺切除、次全切除及開放性活檢,同時鑒於淋巴瘤對放療及化療較敏感,術後應結合化療和(或)放療。本組術後化療方案為CHOP,至今無復發,療效滿意。近年PMLT的5 a生存率已有不斷提高,1966年的報告為44%,1977年54%,1986年報告達74%,這與治療方法的改進有關。過去報告的病例中約10%~50%為單用手術治療,手術切除或活檢後加放療和(或)聯合化療,可能是提高療效的重要因素。
