12歲男孩患兒童早衰症 臉如80歲老人(圖)
http://news.tom.com 2005年12月29日13時22分來源:華商報
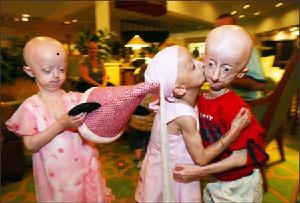
12歲的早衰人塞斯·庫克 |
據美國廣播公司28日報導,美國華盛頓州達令頓地區男孩塞斯·庫克儘管只有12歲,但他的模樣看上去卻像一名頭髮掉光、滿臉皺紋的八十老翁。據悉,庫克患有一種罕見的兒童早衰症,儘管他的心仍是一顆孩子的心,但他的血管卻都已硬化,並飽受關節炎的折磨。由於沒有完整發育,他只有1米高,25磅重。12歲的庫克目前最大的夢想,就是能活到“青少年時代”。全世界的早衰症患者目前約有42人,但科學家至今沒找到治癒早衰症的方法。
兒童早衰症是一種特別稀少的兒童基因病變,可導致兒童戲劇性的早衰和老化。全球每800萬新生兒中就有1個。此病症最嚴重的一種就是何奇森-吉爾福德兒童早衰症,這是由喬納森·何奇森博士和黑斯廷斯·吉爾福德博士共同發現的。何奇森博士於1886年首次描述了這種病症,吉爾福德博士於1904年發現這一病症。
 兒童早衰症
兒童早衰症兒童早衰症
作為一名得兒童早衰症的新生兒,出生時通常都很正常。然而,一年之內,他們的成長速度減緩,不久之後,他們個子比其它正常孩子要矮,體重好要輕。雖然具備正常的智力,但頭髮斑禿、皮膚褶皺而松馳、牙齒脫落,鼻子扁縮,臉與下巴偏小,與腦袋大小極不相稱,眼睛凹陷,在面頰和手臂的皮膚上分布著若隱若現的老年斑,整個的像一位80歲的老人。他們還患有老年人才有的多種老年疾病,如關節僵硬、髖部脫臼和嚴重的心臟血管疾病。然而,與正常老年人有關的其它疾病如白內障和骨關節炎,在兒童早衰症患者身上就沒有出現。
患有兒童早衰症的一些兒童會做冠狀動脈繞道手術或血管重建術以減輕由動脈硬化導致的威脅生命的心臟血管病變。然而,這種手術並不能改變這些可憐孩子的命運。甚至至今還沒有有效辦法能治癒這種疾病。患早衰病兒童的衰老速度是正常兒童的10倍,他們通常在13歲就會因心臟病發作而死亡。
 兒童早衰症
兒童早衰症基因變異導致此怪病
2003年,美國國立人類基因組研究所(NHGRI) 、兒童早衰症研究基金會、紐約州學院和美國密西根州大學的研究人員發現了何奇森-吉爾福德兒童早衰症是由單個基因的微小變異導致的。他們發現,兒童早衰症並非遺傳所至,而是人體內一種名叫LMNA(Lamin A)的蛋白基因發生突變導致。LMNA主要負責細胞核之間的相互連結,一但它發生突變,將會使細胞核處於不穩定狀態,加快人體的發育和衰老,其速度相當於正常速度的8倍,從而導致早衰。
研究小組負責人弗朗西斯·柯林斯博士:“我現在要宣布的是,這段獨立的基因(LMNA)現在能被複製成7種不同的基因,通常基因的突變結果取決於發生基因突變的位置。也就是說基因發生突變位置的不同,將會導致人們患上不同的疾病,比如肌肉營養失調、脂肪代謝障礙、原發性心肌病、以及神經病等疾病,所有這些都可能因為基因突變而產生,我們現在關注的這段引起兒童早衰症的基因十分特殊,因為它(LMNA)直接影響基因的連結,(它的突變)會對整個人體造成重大的影響。"
LMNA 基因為lamin A和lamin C 二種蛋白編碼,何奇森-吉爾福德兒童早衰症的突變導致LMNA 產生異常的lamin A 蛋白,從而導致細胞核膜不穩定,容易讓組織器官因強大身體力量而受傷,如心血管和肌骨骼系統。
兒童早衰症是一種十分罕見的兒童身體機能嚴重失調的疾病。究竟是什麼原因導致兒童早衰症的發生,一直以來這個問題長期困擾著醫學界,目前還沒有針對兒童早衰症的有效治療。兒童早衰症患者約翰·塔科特:“他們找到了我們的致病基因這個訊息,的確令人激動,因為我們將有可能被治癒,死於心血管疾病或動脈硬化的兒童早衰症患者,其平均年齡通常在13周歲。兒童早衰症致病基因的發現,不僅有助於科學家儘早找到兒童早衰症的治療方法,還將有助於科學家深入研究人體衰老的過程和心血管疾病方面的諸多問題
美國科學家近日為兒童早衰症(HGPS)的病因找到了新的線索,他們研究發現,一種名為progerin的蛋白能夠“誘惑”幹細胞誤入歧途,成長為錯誤類型的細胞。這一研究同時也可為理解正常的老化提供幫助。相關論文3月2日線上發表於《自然—細胞生物學》(NatureCellBiology)上。
患有早衰症的兒童易發骨質疏鬆症和動脈硬化症等疾病,並且通常在十幾歲時就會因心臟病而死亡。2003年,科學家確定蛋白progerin與此病有關。Progerin是laminA蛋白的錯誤版本,通常情況下,laminA幫助鞏固細胞核,但是progerin卻會導致畸形的細胞核和高於正常水平的DNA損傷。不幸的是,幾年來科學家對於progerin的了解僅限於此。
在最新的研究中,美國國立癌症研究所的細胞生物學家PaolaScaffidi和TomMisteli利用遺傳技術使培養的皮膚細胞製造progerin蛋白,他們隨後測量了基因活性的變化。結果發現,在1000多個因progerin而改變活性水平的基因中,有一些屬於能幫助促進幹細胞特化為多種類型細胞的Notch生化路徑。
進一步的研究發現,progerin會破壞間質幹細胞(mesenchymalstemcells)的形成,誘使幹細胞形成血管細胞,而不是骨細胞、肌細胞及脂肪細胞。而那些確實轉變成骨細胞的幹細胞活性會異常活躍。
研究人員還發現,由progerin產生的幹細胞很難轉化為脂肪細胞,這也解釋了為什麼早衰症兒童皮下脂層缺失,導致皮膚變薄。另外,那些含有過分活躍Notch路徑的細胞表現出與progerin相似的干擾效果,表明progerin可能正是通過“點燃”Notch路徑起作用的。
此次研究結果還有助於更深入地理解正常的老化。Scaffidi和Misteli曾於2006年發現,即使正常細胞也會產生少量的progerin,新的研究表明,這少量的progerin可能破壞了幹細胞替換損傷和死亡細胞的能力,從而促進了老化。
美國緬因州傑克遜實驗室的發育生物學家ThomasGridley認為,“這一研究結果具有很重要的意義。”
目前,第一個意在減輕兒童早衰症症狀的藥物試驗已經開始。不過新加坡醫學生物學研究所的發育生物學家ColinStewart表示,這些藥物主要標靶progerin,而此次發現則表明能幹擾Notch路徑的化合物同樣值得研究。
