誘導效應指數
正文
表示分子中某一基團或原子對於一個鄰近鍵上通過σ 鍵體系,以靜電誘導方式所引起的電子移動數量的常數。由經驗公式來確定。化學上對於誘導效應的認識已有長遠的歷史。化學家根據化合物的物理化學性質、反應平衡常數和速率常數等提出了多種誘導效應定性次序,例如英戈爾德-卡拉施定性序列等。在定量關係方面也提出多種基團特性常數,如塔夫脫極性取代基常數σ*值等。但這些基團常數都是在某種實驗數據的基礎上,依照推算的需要,就各個基團逐一指定數值的。為了從基團結構的基礎上系統地推導出各種基團誘導效應的大小,1962年蔣明謙和戴萃辰提出誘導效應指數。
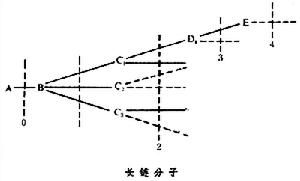
誘導效應指數的計算方法是以組分原子的電負性及其共價半徑為基礎,計算各單位鍵長上的極性強度δ/r(δ表示一個化學鍵的極性狀態, r為鍵長)。誘導效應在一個 σ鍵的體系中傳遞時,每經過一個鏈上原子,降低為原來的1/3,其遞降率以1/α表示。在一個長鏈分子中,B原子上所帶各基團對A─B鍵的誘導效應,可用式(1)或(2)計算。
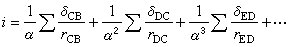 (1)
(1)
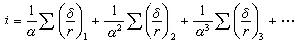 (2)
(2)
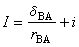
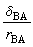 可以寫成
可以寫成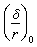 或i0,則可得:
或i0,則可得: I=i0+i (3)
I即以B開始的整個基團對於基準原子A(一般為H原子)的誘導效應指數,I的定性次序完全與各種已知的基團電負性系列符合, 其數值與σ*成直線關係,並且與化合物的電離勢、偶極矩等成良好的線性關係;在同一系列非共軛化合物中,同一反應的平衡常數的對數與速率常數的對數,都與誘導效應指數形成良好的線性關係。這充分表明它可以作為代表基團誘導效應的結構參數。誘導效應指數除了能建立統一的定量的誘導效應序列,和直接表達分子結構與化學活性間的定量關係外,主要還可作為驗證分子結構式,區別分子中不同位置上同種基團的活性,以及推斷反應機理的一種結構參數。誘導效應指數在國內外得到廣泛套用,曾用於萃取劑和反腐蝕劑的選擇,以及某些致癌藥物的藥理作用的研究。
參考書目
蔣明謙、戴萃辰著:《誘導效應指數及其在分子結構與化學活性間定量關係中的套用》,科學出版社,北京,1963。
