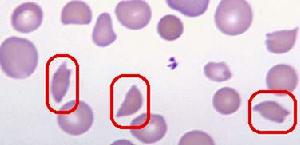
疾病簡介
血栓性血小板減少性紫癜(Thrombotic Thrombocytopenic Purpura,TTP)是一種嚴重的彌散性血栓性微血管病,以微血管病性溶血性貧血、血小板聚集消耗性減少,以及微血栓形成造成器官損害(如腎臟、中樞神經系統等)為特徵。該病最早由Moschowitz在1924年描述。1958年Amorosi和Vltman總結了該病臨床的五大特徵,即血小板減少性紫癜、微血管病性溶血、中樞神經系統症狀、發熱以及腎臟損害,並稱之為TTP五聯征,僅有前三大特徵的稱為三聯征。多數TTP患者起病急驟,病情兇險,如不治療死亡率高達90%。
流行病學
國外報導發病率為1/100萬,國內尚無這方面資料,近年來隨著對該病認識進一步深入,診斷率提高,繼發於其他疾病和藥物的患者增多,發病率呈上升趨勢,大約在2~8/100萬。發病情況通常與種族差異無關,女性稍多,且好發於育齡期。
發病機制
絕大多數患者是由於vWF蛋白裂解酶(vWFCP)異常所致。vWFCP 是正常止血過程中必須成在高剪下力血流狀態時內皮細胞表現、血小板表面受體和vWF多聚體三者之間相互作用,導致血小板與內皮細胞粘附。vWF水平過高會造成慢性內皮細胞損傷,可導致血栓性疾病。1982年Joel Moake等最先從在TTP患者的血清中發現並證實了存在一種超大分子的vWF因子 (ultralarge multimers of von Willebrand factor, UL-vWF)。1996年,Furlan等學者從血清中分離出一種可以剪下vWF的金屬蛋白酶,在臨床的研究中也發現TTP患者缺乏這種蛋白酶。2001年,Geririseten等分別套用不同的方法純化得到該酶,確定了該蛋白酶是屬於ADAMTS (A Disintegrin And Metalloprotease with ThromboSpondin 1 repeats)金屬蛋白酶家族成員,並命名為血管性血友病因子裂解酶(ADAMTS13),並將其基因定位於9q34位點。通過這一系列的研究,深刻地揭示了TTP的發病與ADAMTS13有密切的關係,對於TTP發病機制的認識也得到了更進一步的明確。vWFCP(ADAMTSl3)在TTP發病中起病因學作用,而其活性降低只是表現,本質的因素是其質、量或抗體存在。ADAMTSl3缺陷,活性下降,形成過多超大的vWF多聚體,可觸發病理性血小板聚集,導致TTP。
根據病因可將TTP分為遺傳性TTP和獲得性TTP,後者又可根據病因是否明確分為特發性TTP和繼發性TTP。遺傳性TTP的基本原因為ADAMTSl3突變。
遺傳性TTP患者大部分是複合雜合子,也有個別純合子的報導,還有部分血緣相關家族病例。大約10%的病例發生ADAMTS13基因突變,引起遺傳性的蛋白酶缺乏,導致家族性隱性TTP。
臨床上70%-80%的TTP患者其ADAMTS13缺乏是獲得性的,是由一種短暫的隨疾病緩解而消失的循環型自身抗體所抑制,97%-100%的患者可檢測出ADAMTS13自身抗體,該抑制性抗ADAMTS13自身抗體主要是IgG,部分是IgG1和IgG4亞型,也可以是IgM和IgA型。最近的研究表明,獲得性TTP的抑制性自身抗體主要的作用位點在ADAMTS13的半胱氨酸富集區和間隔區,但也有僅僅直接攻擊抗原表位的,主要是前導肽、凝血酶敏感區和補體結合區,這些研究結果提示,獲得性ADAMTS13的缺失是一個多克隆的自身抗體反應。
在獲得性TTP中,分為特發性以及繼發性,如可繼發於感染、藥物、自身免疫性疾病、腫瘤、骨髓移植和妊娠等多種疾病和病理生理過程。特發性TTP發病分子機制基本闡明,
病因及分類
1、遺傳性TTP 是一種在新生兒和兒童極其罕見(其發生率約為百萬分之一)的常常但非僅僅與常染色體隱性遺傳相關的疾病,由9號染色體q34編碼的金屬蛋白酶ADAMTSl3基因的缺陷(突變或缺失)導致其合成或分泌異常,致使其活性嚴重缺乏,一般低於正常活性的5%~lO%,無法降解高黏附性的超大分子量vWF,從而引起血小板性微血管血栓的形成而發病。
2、獲得性TTP可根據誘發因素是否明確分為原發性(特發性)TTP和繼發性TTP。獲得性TTP患者中有很大一部分,尤其是特發性TTP,可以檢測到抗ADAMTSl3自身抗體的存在。這種自身抗體中和或抑制了AMADTSl3的活性,同樣有ADAMTSl3活性的降低,從而導致發病。
1) 原發性(特發性)TTP:原發性TTP發病率為33~57%,90%的原發性TTP患者發病時可以檢測到抗ADAMTSl3自身抗體
2) 繼發性TTP:繼發性TTP發病率約為43~66%,可繼發於感染、藥物、自身免疫性疾病、腫瘤、骨髓移植和妊娠等多種疾病和病理生理過程。國外有報導在部分繼發性TTP患者體內也能檢測到ADAMTSl3自身抗體,如部分藥物(噻氯匹啶、氯吡格雷等)相關性TTP、妊娠相關性TTP、胰腺炎誘發的TTP、SLE相關性TTP、移植相關性TTP等患者體內均發現有自身抗體,但部分繼發性TTP患者體內確實沒有檢測到抗ADAMTSl3自身抗體。
臨床表現
本病在任何年齡都可發病,新生兒和90歲以上老年人均可發病,但發病高峰年齡是20~60歲,中位年齡35歲。本病起病多急驟,少數起病緩慢,以急性爆發型常見,10%-20%表現為慢性反覆發作型。根據患者的表現而在臨床上分為:同時具有血小板減少、微血管病性溶血性貧血、中樞神經系統症狀的三聯症和三聯症同時伴有腎臟損傷和發熱的五聯症。
1、發熱:90%以上患者有發熱,在不同病期均可發熱,多屬中等程度。其原因不明,可能與下列因素有關:①繼發感染,但血培養結果陰性;②下丘腦體溫調節功能紊亂;③組織壞死;④溶血產物的釋放;⑤抗原抗體反應使巨噬細胞及粒細胞受損,並釋放出內源性致熱原。
2、神經系統改變:包括頭痛、精神改變、局部運動或感覺缺陷、視覺模糊甚至昏迷,其特點為症狀變化不定,初期為一過性,部分患者可改善,可以反覆發作。神經系統表現的多變性為血栓性血小板減少性紫癜的特點之一,其嚴重程度常決定血栓性血小板減少性紫癜的預後。
3、血小板減少引起的出血:以皮膚黏膜為主,表現為淤點、淤斑或紫癜、鼻出血、視網膜出血、生殖泌尿道和胃腸出血,嚴重者顱內出血,其程度視血小板減少程度而不一。
4、微血管病性溶血性貧血:不同程度的貧血。約有1/2的病例出現黃疸、20%有肝脾腫大,少數情況下有Raynaud現象。
5、腎臟損害:肉眼血尿不常見。重者因腎皮質壞死最終發生急性腎功能衰竭 。
診斷依據
本病的診斷標準如下。
1. 主要診斷依據
(1) 血小板減少
1)血小板計數明顯降低,學片中可見巨大血小板
2)皮膚和(或)其他部位出血。
3)骨髓中巨核細胞數量正常或增多,可伴成熟障礙。
4)血小板壽命縮短。
(2)微血管病性溶血貧血:
1)正細胞正色素性中、重度貧血。
2)血片中可見較多的畸形紅細胞(>2%)與紅細胞碎片。
3)網織紅細胞計數升高。
4)骨髓代償性增生,以紅係為主,粒/紅比值下降。
5) 黃疸、血膽紅素升高,以間接膽紅素為主。
6)可有血漿游離血紅蛋白升高,結合珠蛋白、血紅素結合蛋白減少,乳酸脫氫酶升高。
7)與深色尿,偶可見血紅蛋白尿。
以上(1)、(2)兩項合稱TTP二聯征。
(3)無明顯原因可以解釋上述二聯征。
具備以上(1)~(3)三項即可初步診斷TTP。
2、其他診斷依據
(1)神經精神異常:精神異常與血小板減少、MAHA同時存在成為TTP三聯征(Triad)
(2)腎臟損害:蛋白尿,鏡下血尿。
(3)發熱:多為低、中度發熱,如有寒戰、高熱常不支持特發性TTP-HUS的診斷
腎臟損害、發熱與三聯征同時存在稱為TTP五聯征。
(4)消化系統症狀:由於胰腺及胃腸道微血栓可導致腹痛,25%-50%的患者有肝、脾腫大。
(5)軟弱無力
(6)輔助檢查:
1)ADAMTS13測定:重度減低者具有診斷價值 。
2)組織病理學檢查:可作為診斷輔助條件,無特異性。典型病理表現為小動脈、毛細血管中有均一性“透明樣”血小板血栓,PAS染色陽性,並含有vWF因子,纖維蛋白/纖維蛋白原含量極低。此外,還有血管內皮增生、內皮下“透明樣”物質沉積、小動脈周圍同心性纖維化等,栓塞局部可有壞死,一般無炎性反應。目前已很少套用,除非為尋找原發性疾病。
3)凝血象檢查:有條件應爭取檢查以輔助診斷。本病時PT、纖維蛋白原等基本正常,D-二聚體、纖維蛋白降解產物、凝血酶-抗凝血酶複合體、纖溶酶原活化因子抑制物(PAI-1)、血栓調節素(thrombomodulin)等均可輕度增高。
4)直接Coombs′試驗:本病時絕大多數應為陰性,。
5)其他:血漿中vWF因子升高,可發現抗血小板抗體,抗CD36抗體、UL-vWF等,肝轉氨酶也可增高。如果懷疑HUS時,應進行大腸桿菌的細菌學檢查。
鑑別診斷
1、瀰漫性血管內凝血(DIC):TTP首先需要鑑別的疾病是DIC。鑑別要點見下表
1、溶血性尿毒症綜合徵(Hemolytic Uremia Syndrome,HUS)
有關HUS與TTP的關係,目前認為是分立的但又不是獨立的綜合徵。TTP與HUS的鑑別目前可以通過ADAMTSl3的活性檢測區分,即TTP患者的ADAMTSl3活性多有嚴重缺乏,而HUS患者其活性均只是輕度或中度減少。但有學者主張不必細分二者,因為這兩種疾病目前治療上都採用血漿置換療法,故常被合稱為TTP—HUS綜合徵 。
表1.TTP與其他疾病鑑別
| TTP | HUS | HELLP | DIC | |
| 神經精神症狀 | +++ | +/- | +/- | +/- |
| 腎損害 | +/- | +++ | + | +/- |
| 發熱 | +/- | -/+ | - | +/- |
| 肝損害 | +/- | +/- | +++ | +/- |
| 高血壓 | -/+ | +/- | +/- | - |
| 溶血 | +++ | ++ | ++ | + |
| 血小板減少 | +++ | ++ | ++ | +++ |
| 凝血異常 | - | - | +/- | +++ |
3、Evans綜合徵 自身免疫性溶血性貧血伴免疫性血小板減少性紫癜。可有腎功能損害的表現 ,Coombs試驗陽性,無畸形和破碎紅細胞,無神經症狀。
4、HELLP(Hemolysis,Elevated/Liver function,Low Platelets)綜合徵:是一種與妊娠期高血壓相關的嚴重併發症,病理表現為血栓性微血管性改變,臨床上表現為溶血、肝功能異常和血小板減少,與ADAMTS13缺乏無關,可能與自身免疫機制有關。但是在遺傳性或獲得性ADAMTS13缺乏的婦女,妊娠本身可以誘發急性TTP。
治療
1、血漿置換:自從引進血漿置換療法後,原發性TTP的死亡率由90%降至10%左右。血漿置換機理是糾正酶的缺乏,去除導致內皮細胞損傷和血小板聚集的不利因子和自身抗體。血漿置換原則是:早期、足量、優質、聯合,只要患者有明顯的血小板減少與微血管病性溶血性貧血,不能用其他的疾病解釋時,即開始使用。 國外文獻推薦血漿置換的量為40-80ml/(kg/d),每日一次,直至血小板減少和神經系統症狀緩解,血紅蛋白穩定,血清乳酸脫氫酶水平正常,然後在1~2周內逐漸減少置換量直至停止。 血漿替代品多選用冷沉澱上清或新鮮冰凍血漿。雖然患者有嚴重的血小板減少,但避免輸注血小板仍是非常關鍵的。血漿置換對慢性反覆發作的家族性TTP患者療效欠佳。
2、血漿輸註:對於遺傳性TTP患者,血漿輸注是首選治療措施。也作為無條件進行血漿置換時的替代治療,但療效不如血漿置換。多與糖皮質激素、靜脈免疫球蛋白、環孢菌素A等聯合使用。
3、糖皮質激素 能夠穩定血小板和內皮細胞膜,抑制IgG產生。通常與血漿置換同時套用,一直持續到病情緩解,再逐漸減量。潑尼松1-2mg/(kg··d) 或地塞米松20mg/d,也可用大劑量甲基強的松龍1000mg/d,靜脈滴注。
4、免疫抑制劑 有報導認為硫唑嘌呤和環磷醯胺對於難治性TTP可以通過抑制自身抗體產生達到治療目的。抗CD20單抗--利妥昔單抗可以通過清除B細胞克隆產生的ADAMTS13抑制性抗體,導致疾病緩解,具體用法為375mg/m²/每周,平均約4個療程。環胞素A可以通過抑制calcineurin介導的去磷酸化作用而抑制輔助性T細胞的功能,從而抑制B細胞的分化和產生效益型抗體,通常與血漿置換聯用。大劑量免疫球蛋白可以通過抑制血小板聚集和脾臟對血小板和紅細胞的破壞對部分血漿置換無效患者起一定療效。。
5、脾切除
脾臟在TTP的發病機制中的確切作用並不清楚,作為網狀內皮系統,脾臟是自身抗體產生和抗原抗體複合物清除的主要場所,因此,通過脾切除術可以去除抗體產生部位。由於療效不十分肯定,目前較少採用,多用於其他療法無效或多次復發者。
6、補充ADAMTS13蛋白
血漿純化ADAMTS13蛋白。克隆ADAMTS13基因,獲得功能性的 ADAMTS13重組蛋白,仍處於實驗研究階段,為目前最具前景的TTP治療方法。理論上講,採用rh—ADAMTSl3對遺傳性TTP患者行替代治療將是一種有著良好前景的治療手段。.
預後和轉歸
之前TTP預後差,病程短,不及時治療病死率80~90%,隨著血漿置換的臨床套用,預後大大改觀,病死率降至10~20%。研究表明,TTP患者其ADAMTS13活性是一個比較理想預後指標。ADAMTS13嚴重缺乏的TTP患者其復發率要比非嚴重缺乏者高,分別為60%和19%。