疾病分類
根據中華醫學會神經病學分會帕金森病及運動障礙學組《肝豆狀核變性的診斷與治療指南》,臨床分型如下:
肝型
①持續性血清轉氨酶增高;②急性或慢性肝炎;③肝硬化(代償或失代償);④暴發性肝功能衰竭(伴或不伴溶血性貧血)。腦型
①帕金森綜合徵;②運動障礙:扭轉痙攣、手足徐動、舞蹈症狀、步態異常、共濟失調等;③口-下頜肌張力障礙:流涎、講話困難、聲音低沉、吞咽障礙等;④精神症狀。其他類型
以腎損害、骨關節肌肉損害或溶血性貧血為主。混合型
以上各型的組合。發病原因
 肝豆狀核變性
肝豆狀核變性發病機制
正常人每日自腸道攝取少量的銅,銅在血中先與白蛋白疏鬆結合,在肝細胞中銅與α2-球蛋白牢固結合成具有氧化酶活性的銅藍蛋白。循環中90%的銅與銅藍蛋白結合,銅作為輔基參與多種重要生物酶的合成。銅在各臟器中形成各種特異的銅-蛋白組合體,剩餘的銅通過膽汁、尿和汗液排出。疾病狀態時,血清中過多的游離銅大量沉積於肝臟內,造成小葉性肝硬化。當肝細胞溶酶體無法容納時,銅即通過血液向各個器官散布和沉積。基底節的神經元和其正常酶的轉運對無機銅的毒性特別敏感,大腦皮質和小腦齒狀核對銅的沉積也產生症狀。銅對腎臟近端小管的損害可引起胺基酸、蛋白以及鈣和磷酸鹽的丟失。銅在眼角膜彈力層的沉積產生K-F環。與此同時,肝硬化可產生門靜脈高壓的一系列變化。
病理生理
病理改變主要累及肝腦腎角膜等。肝臟表面和切片均可見大小不等的結節或假小葉,逐漸發展為肝硬化,肝小葉由於銅沉積而呈棕黃色。腦的損害以殼核最明顯,蒼白球、尾狀核、大腦皮質、小腦齒狀核也可受累,顯示軟化、萎縮、色素沉著甚至腔洞形成。光鏡下可見神經元脫失和星形膠質細胞增生。角膜邊緣後彈力層及內皮細胞漿內有棕黃色的細小銅顆粒沉積。臨床表現
本病通常發生於兒童和青少年期,少數成年期發病。發病年齡多在5~35歲,男性稍多於女性。病情緩慢發展,可有階段性緩解或加重,亦有進展迅速者。神經精神症狀
神經症狀以錐體外系損害為突出表現,以舞蹈樣動作、手足徐動和肌張力障礙為主,並有面部怪容、張口流涎、吞咽困難、構音障礙、運動遲緩、震顫、肌強直等。震顫可以表現為靜止或姿勢性的,但不像帕金森病的震顫那樣緩慢而有節律性。疾病進展還可有廣泛的神經系統損害,出現小腦性共濟失調、病理征、腱反射亢進、假性球麻痹、癲癇發作,以及大腦皮質、下丘腦損害體徵。精神症狀表現為注意力和記憶力減退、智慧型障礙、反應遲鈍、情緒不穩,常伴有強笑、傻笑,也可伴有衝動行為或人格改變。肝臟異常
肝臟受累時一部分病例發生急性、亞急性或慢性肝炎,大部分病例肝臟損害症狀隱匿、進展緩慢,就診時才發現肝硬化、脾腫大甚至腹水。重症肝損害可發生急性肝功能衰竭,死亡率高。脾腫大可引起溶血性貧血和血小板減少。角膜K-F環
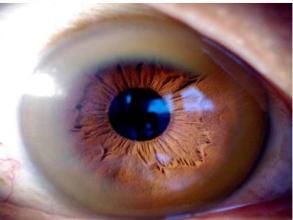 肝豆狀核變性疾病
肝豆狀核變性疾病其他
腎臟受損時可出現腎功能改變如腎性糖尿、微量蛋白尿和胺基酸尿。鈣、磷代謝異常易引起骨折、骨質疏鬆。銅在皮下的沉積可致皮膚色素沉著、變黑。診斷鑑別診斷
輔助檢查
(1)銅代謝相關的生化檢查:①血清銅藍蛋白降低:正常為200—500mg/L,患者<200mg/L,<80mg/L是診斷WD的強烈證據。②尿銅增加:24h尿銅排泄量正常<100μg,患者≥100μg;③肝銅量:正常<40一55μg/g(肝乾重),患者>250μg/g(肝乾重)。(2)血尿常規:wD患者有肝硬化伴脾功能亢進時其血常規可出現血小板、白細胞和(或)紅細胞減少;尿常規鏡下可見血尿、微量蛋白尿等。
(3)肝腎功能:患者可有不同程度的肝功能改變,如血清總蛋白降低、球蛋白增高,晚期發生肝硬化。肝穿刺活檢測定顯示大量銅過剩,可能超過正常人的5倍以上。發生腎小管損害時,可表現胺基酸尿症,或有血尿素氮和肌酐增高及蛋白尿等。
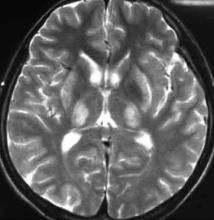
(4)腦影像學檢查:CT可顯示雙側豆狀核對稱性低密度影。MRI比CT特異性更高,表現為豆狀核(尤其殼核)、尾狀核、中腦和腦橋、丘腦、小腦及額葉皮質T1加權像低信號和T2加權像高信號,或殼核和尾狀核在T2加權像顯示高低混雜信號,還可有不同程度的腦溝增寬、腦室擴大等。
(5)基因診斷:WD具有高度的遺傳異質性,致病基因突變位點和突變方式複雜,故尚不能取代常規篩查手段。利用常規手段不能確診的病例,或對症狀前期患者、基因攜帶者篩選時,可考慮基因檢測。
診斷
根據青少年起病、典型的錐體外系症狀、肝病體徵、角膜K-F環和陽性家族史等診斷不難。如果CT及MRI有雙側豆狀核區對稱性影像改變,血清銅藍蛋白顯著降低和尿銅排出量增高則更支持本病。對於診斷困難者,應爭取肝臟穿刺做肝銅檢測。鑑別診斷
本病臨床表現複雜,應注意和小舞蹈病、青少年性Huntingtou舞蹈病、肌張力障礙、原發性震盪、帕金森病和精神病等鑑別;此外,還應與急、慢性肝炎和肝硬化、血小板減少性紫癜、溶血性貧血、類風濕性關節炎、腎炎及甲狀腺功能亢進等相鑑別。疾病治療
飲食治療
避免進食含銅高的食物如小米、蕎麥麵、糙米、豆類、堅果類、薯類、菠菜、茄子、南瓜、蕈類、菌藻類、乾菜類、乾果類、軟體動物、貝類、螺類、蝦蟹類、動物的肝臟和血、朱古力、可可。某些中藥,如龍骨、牡蠣、蜈蚣、全蠍等。藥物治療
以驅銅藥物為主,驅銅及阻止銅吸收的藥物主要有兩大類藥物,一是絡合劑,能強力促進體內銅離子排出,如青黴胺、二巰丙磺酸鈉、三乙烯-羥化四甲胺、二巰丁二酸等;二是阻止腸道對外源性銅的吸收,如鋅劑、四硫鉬酸鹽。(1)D-青黴胺(D-penicillamine,PCA):是本病的首選藥物,為強效金屬螯合劑,在肝臟中可與銅形成無毒複合物,促使其在組織沉積部位被清除,減輕游離狀態銅的毒性。青黴胺與組織中的同類子絡合成銅-青黴胺複合物,從尿中排出。本要口服易吸收。藥物副作用有噁心、過敏反應、重症肌無力、關節病、無皰瘡,少數可以引起白細胞減少和再生障礙性貧血。視神經炎、狼瘡綜合症。剝脫性皮炎、腎病綜合徵等較嚴重的毒副作用。另外,當患者首次用藥時應做青黴胺皮試,陰性者才能使用。本病需長期甚或終生服藥,應注意補充足量維生素B。
(2)二巰基丙磺酸(DMPS):DMPS5mg/kg溶於5%葡萄糖溶液500ml中緩慢靜滴,每日1次,6天為1療程,2個療程之間休息1-2天,連續注射6-10個療程。不良反應主要是食慾減退及輕度噁心、嘔吐。可用於有輕、中、重度肝損害和神經精神症狀的肝豆狀核病患者。
(3)三乙烯-羥化四甲胺(TETA):藥理作用與D-青黴胺相似,是用於不能耐受青黴胺治療時的主要藥物。副作用小,但藥源困難、價格不菲。
(4)鋅製劑(zincpreparations):常用有硫酸鋅、醋酸鋅、葡萄糖酸鋅、甘草鋅等。在餐後1h服藥以避免食物影響其吸收,儘量少食粗纖維以及含大量植物酸的食物。鋅劑副反應較小,主要有胃腸道刺激、口唇及四肢麻木感、免疫功能降低、血清膽固醇紊亂等。對胎兒無致畸作用。鋅劑的缺點是起效慢(4~6個月),嚴重病例不宜首選。
(5)四硫鉬酸鹽(tetl.athiomolybdate,TM):能促進體內的金屬銅較快排出,改善WD的症狀與PCA相當,副作用則比PcA少得多。本藥在國外仍未商品化,至今國內未有使用的經驗。
(6)中藥治療:大黃、黃連、薑黃、金錢草、澤瀉、三七等由於具有利尿及排銅作用而對wD有效,少數患者服藥後早期出現腹瀉、腹痛。使用中藥治療WD,效果常不滿意,中西醫結合治療效果會更好。推薦用於症狀前患者、早期或輕症患者、兒童患者以及長期維持治療。
對症治療
有震顫和肌強直時可用苯海索口服,對粗大震顫者首選氯硝西泮。肌張力障礙可用苯海索、複方左鏇多巴製劑、多巴胺受體激動劑,還可服用氯硝西泮、硝西泮、巴氯芬,局限性肌張力障礙藥物治療。無效者可試用局部注射A型肉毒毒素。有舞蹈樣動作和手足徐動症時,可選用氯硝西泮、硝西泮、氟哌啶醇,合用苯海索。對於精神症狀明顯者可服用抗精神病藥奮乃靜、利培酮、氟哌啶醇、氯氮平,抑鬱患者可用抗抑鬱藥物。護肝治療藥物也應長期套用。手術治療
對於有嚴重脾功能亢進者可行脾切除術,嚴重肝功能障礙時也可以考慮肝移植治療。[3]疾病預後
本病若早發現早診斷早治療,一般較少影響生活質量和生存期。晚期治療基本無效,少數病情進展迅速或未經治療出現嚴重肝臟和神經系統損害者預後不良,會致殘甚至死亡。。肝豆狀核變性患者的主要死因是肝衰竭、自殺和腫瘤。儘管20年來早期診斷和治療水平有了較大的進步,但肝豆狀核變性患者的死亡率還是較高,預後不佳。疾病預防
對WD患者的家族成員測定血清銅藍蛋白、血清銅、尿銅及體外培養皮膚成纖維細胞的含銅量有助於發現WD症狀前純合子及雜合子,發現症狀前純合子可以及早治療。雜合子應禁忌與雜合子結婚以免其子代發生純合子。產前檢查如發現為純合子,應終止妊娠,以杜絕患者的來源。疾病護理
注意飲食①避免進食含銅量高的食物:小米、養麥面、糙米、豆類、堅果類、薯類、菠菜、茄子、南瓜、蕈類、菌藻類、乾菜類、乾果類、軟體動物、貝類、螺類、蝦蟹類、動物的肝和血、朱古力、可可。某些中藥(龍骨、牡蠣、蜈蚣、全蠍)等。
②適宜的低銅食物:精白米、精面、新鮮青菜、蘋果、桃子、梨、魚類、豬牛肉、雞鴨鵝肉、牛奶等。
③高胺基酸或高蛋白飲食。
④勿用銅製的食具及用具。
藥物治療的監測
開始用藥後應檢查肝腎功能、24h尿銅、血尿常規等,前3個月每月複查1次,病情穩定後3個月查1次。肝脾B超3—6個月檢查1次。同時必須密切觀察藥物的副反應。
康復及心理治療
有研究發現抑鬱症在WD患者中非常常見,已有的調查發現約30-60%患者存在抑鬱。因此要加強對WD患者的心理疏導。
①加強公共宣傳與教育,減少對患者的歧視。
②不斷提高醫護人員的業務和綜合素質,學習心理學、溝通技巧,與患者建立良好的關係。
③加強生活護理。通過對患者進行文娛體療和各種技能訓練,有利於改善睡眠與精力、進食、運動與感覺等軀體功能狀況,創造寬鬆舒適的住院環境和豐富的訓練活動,有利於緩解精神緊張,減輕焦慮、抑鬱等負性情感。
④加強對患者進行心理輔導和干預。心理健康狀況和生活質量相關,心理干預,對改善患者生活質量有幫助。
⑤患者的預後與家庭支持有密切關係,患者家庭作為其最主要的支持系統,對患者心理及身體的康復起著至關重要的作用。