疾病描述
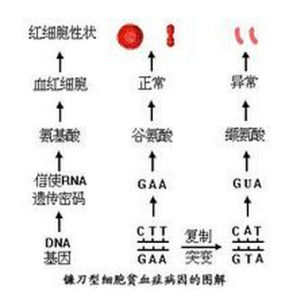
1928年,人們就已經了解到鐮刀型細胞貧血症是一種遺傳病。後來證實,它是一種常染色體隱性遺傳病。1949年,一位曾經兩次獲得諾貝爾獎金的美國著名化學家鮑林(Li.C.Pauling,1901—),在美國的《科學》雜誌上發表了題為《鐮刀型細胞貧血症cc一種分子病》的研究報告。他在文章中寫道:“在我們的研究開始之時,有證據表明(紅細胞)鐮變的過程可能是與紅細胞內血紅蛋白的狀態和性質密切相關的。
鮑林將正常人、鐮刀型細胞貧血症患者和鐮刀型細胞貧血症基因攜帶者的血紅蛋白,分別放在一定的緩衝溶液中電泳,發現正常人和患者的血紅蛋白的電泳圖譜明顯不同,而攜帶者的血紅蛋白的電泳圖譜,與由正常人的和患者的血紅蛋白以1:1的比例配成的混合物的電泳圖譜非常相似。鮑林推測鐮刀型細胞貧血症是由於血紅蛋白分子的缺陷造成的。
疾病概述
 基因
基因 流行病學:
鐮刀型細胞貧血症系常染色體隱性遺傳性疾病。主要見於非洲黑人,雜合子狀態者占非洲黑人的20%美國黑人群的8%,此外也見於中東、希臘、土籍印第安人及與上述民族長期通婚的人群。雜合子之間通婚其1/4子女為純合子導致鐮刀型細胞貧血症。
疾病病理
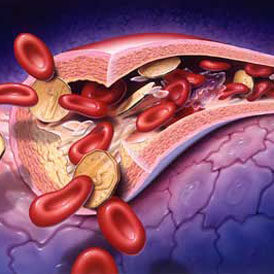 血液
血液 這是β鏈N末端的一段肽鏈。也就是說,HbS和HbA的α鏈是完全相同的,所不同的只是"鏈上從N末端開始的第6位的胺基酸殘基,在正常的HbA分子中是谷氨酸,在病態的HbS分子中卻被纈氨酸所代替。
在HbS中,由於帶負電的極性親水谷氨酸被不帶電的非極性疏水纈氨酸所代替,致使血紅蛋白的溶解度下降。在氧張力低的毛細血管區,HbS形成管狀凝膠結構(如棒狀結構),導致紅細胞扭曲成鐮刀狀(即鐮變)。這種僵硬的鐮狀紅細胞不能通過毛細血管,加上HbS的凝膠化使血液的黏滯度增大,阻塞毛細血管,引起局部組織器官缺血缺氧,產生脾腫大、胸腹疼痛(又叫做“鐮形細胞痛性危象”)等臨床表現。
臨床表現
 腎病綜合徵
腎病綜合徵 併發症:本病在病情穩定時,患者可耐受貧血及其他臨床症狀;但當病情突然加重時,稱“鐮狀細胞危象”,則有嚴重臨床表現,甚至導致死亡。感染、代謝性酸中毒、低氧條件可能誘發危象,但有時難以發現明顯誘因。根據臨床表現特徵的不同,可將鐮狀細胞危象分為5型:梗死型(疼痛型)再生障礙型,巨幼細胞型,脾滯留型,溶血型。
1.梗死型危象系最常見的一種危象,鐮變的僵硬紅細胞阻塞小血管;組織缺氧,重者導致組織壞死血管梗死可發生於任何部位,但梗死引起疼痛的部位最常見於四肢骨骼,尤以膝部及膝部以下多見其次是胸背部及腹部疼痛常為發作性疼痛可伴有發熱,輕者1~2天自行緩解,重者持續時間較長發作頻度不一;可為數天1次,也可為數年1次。脾梗死是引起腹痛的常見原因多次脾梗死形成大量瘢痕組織可使脾臟變小,稱自身脾切除。部分病人腹痛與慢性溶血引起的膽石症有關,此時血清膽紅素會升高。此型危象發作時貧血常常並不加重。
2.再生障礙型危象貧血突然加重,網織紅細胞顯著減少甚或消失,骨髓增生低下。感染尤其是微小病毒(parvovirus)感染是常見誘發因素。
3.巨幼細胞型危象妊娠患者易發生此型危象,葉酸缺乏是主要原因。嚴重貧血伴有巨幼細胞貧血特徵是本型的主要臨床表現。
4.脾滯留型危象此型危象多見於兒童患者,也可見於脾顯著增大的成年患者。主要臨床表現是血紅蛋白的濃度陡然下降。在幼年患兒可成為致死原因。
5.溶血型危象此型危象不常見。當本病患者合併其他疾患(如G6PD缺乏)時,易發生溶血危象。臨床表現為貧血加重黃疸、網織紅細胞數增多常發生溶血者易有膽石症。
疾病診斷
本病的診斷並不困難重要的是要考慮到本病的可能性而不遺漏本病。根據種族和家族史鐮變試驗陽性血紅蛋白電泳顯示主要成分為HbS,再結合臨床表現,即可明確診斷。
疾病檢查
 網織紅細胞計數器
網織紅細胞計數器 1. 外周血血紅蛋白為50~100g/L,危象時進一步降低。 網織紅細胞計數常在10%以上。紅細胞大小不均,多染性、嗜鹼性點彩細胞增多可見有核紅細胞、靶形 紅細胞異形紅細胞、Howell-Jolly小體。鐮狀紅細胞並不多見,若發現則有助於診斷通常採用“鐮變試驗”檢查有無鐮狀細胞。紅細胞滲透脆性顯著降低白細胞和血小板計數一般正常。
2. 骨髓象示紅系顯著增生,但在 再生障礙危象時增生低下,在巨幼細胞危象時有巨幼細胞變
3.血清膽紅素輕~中度增高,溶血危象時顯著增高。本病的溶血雖以血管外溶血為主,但也存在著血管內溶血。
4. 血漿結合珠蛋白降低,血漿游離血紅蛋白可能增高。
5. 紅細胞半衰期測定顯示紅細胞生存時間明顯縮短至5~15天[正常為(28±5)天]
6. 血紅蛋白電泳顯示HbS占80%以上HbF增多至2%~15%,HbA2正常,而HbA缺如。
其它輔助檢查:
根據病情、臨床表現、症狀、體徵選擇做心電圖、X線、CTMRI、B超、生化等檢查。
治療思路
 治療儀器
治療儀器 鐮刀型細胞貧血是一種遺傳的慢性貧血症,表現為紅血球形態失常,劇烈疼痛,未成年夭折。這是由於病人體內製造血紅蛋白的基因的一個編碼錯誤造成的,血紅蛋白是紅血球攜帶氧氣在體內運輸的主要成分。錯誤的基因編碼一個異常的血紅蛋白,導致紅血球形態失常成鐮刀型,往往會阻塞毛細血管,進一步導致疼痛、中風、心臟病發作、腎功能喪失、甚至早夭。
儘管鐮刀型貧血無法治癒,但還是有治療方法的,包括抗癌藥物hydroxyurea,輸血,骨髓移植等。Hydroxyurea廣泛用於重新激活gamma球蛋白的產生,替代血紅蛋白中的失活組分――beta球蛋白。雖然這種方法不能治癒這種疾病,卻可以幫助減輕疾病的症狀。
 研究人員
研究人員 研究人員在攜帶鐮刀型細胞的轉基因小鼠中表達一種人類胚胎形式的血紅蛋白alpha鏈――zeta球蛋白。和患鐮刀型細胞的小鼠不同的是,改造後的轉基因小鼠血液中不再出現鐮刀型紅細胞,腎功能正常,有正常的血細胞計數,而不再是貧血,而且其紅細胞的壽命是正常紅細胞的5倍。這個工作證實一種全新的治療方法能夠逆轉患鐮刀型細胞貧血的小鼠的疾病進程。雖然這個實驗離套用到人還有相當遙遠的距離,不過可以預期,這種方法和其他現有的方法一起,將為飽受疾病折磨的病人提供更加有效而靈活的治療方案。
全世界有數以百萬計的人遭受鐮刀型貧血的困擾。這也是美國最常見的遺傳病,病人數大約在7.2萬左右,每500個非裔美國人中就有一個患者,每1000―1400西班牙裔美國人中就有一個患者,此外美國還有大約2百萬健康的鐮刀型貧血基因攜帶者,由於有潛在可能將疾病基因遺傳給子女而在接受治療。
預後預防
預後:
鐮刀型細胞貧血症是一種嚴重疾病若無良好的醫療條件,患者多於幼年死亡。如有較好的醫療條件患者可能生存至成年。妊娠使心力衰竭、梗死、貧血加重並易發生流產和死胎。感染、心力衰竭、梗死危象引起的休克、中樞神經系統併發症可成為死因。
預防:
本病預後不佳且缺乏有效療法,故應注重預防,提倡優生,進行婚前和產前檢查。採用聚合酶鏈反應(PCR)和寡核苷酸探針(ASO)方法或採用PCR和限制性內切酶片段長度多態性(RFLP)方法,在妊娠早期即可作產前診斷,防止純合子患兒的出生。