歷史
 偉哥
偉哥西地那非由美國輝瑞製藥公司研發,最早是作為一個用於治療心血管疾病的5-磷酸二酯酶抑制藥而進入臨床研究的。研究者希望西地那非能夠通過釋放生物活性物質一氧化氮舒張心血管平滑肌,達到擴張血管緩解心血管疾病的目的。但是臨床研究顯示,西地那非對心血管的作用並不能達到研究人員的預期,作為一個心血管藥物,西地那非的表現是令人失望的,無法成長成為一個成功的治療藥物。
1991年4月,西地那非的臨床研究正式宣告失敗,但受試者報告的一項副作用引起了研究人員的注意。研究員發現,治療者在領過試藥之後都不願意交出餘下的藥物。追查之下,發現這一種藥對病者的性生活有改善。在經輝瑞高層許可後,研究人員就西地那非對陰莖海綿體平滑肌的作用展開了研究,並於1998年3月27日獲得美國聯邦食品和藥品管理局的上市許可,成為令輝瑞公司名聲大噪的一個產品。
1998年,美國和歐洲的食品藥品監管部門(FDA和EFSA)批准了西地那非(Viagra)上市治療ED,在全球範圍內引起了轟動。西地那非臨床研究結果發表於頂級醫學雜誌《新英格蘭醫學雜誌》,NewEnglandJournalofMedicine
1999年,“Viagra”一詞被英國牛津大詞典收錄,同時,臨床研究證實了其心血管方面的安全性。
2000年,研究進一步證實了西地那非在血壓方面的安全性,以及與降壓藥物合用的安全性。文章發表於《高血壓雜誌》,JournalofHypertension
2001年,Viagra已經在全球超過100個國家獲得批准上市,平均每秒處方6片。
2002年,臨床人體研究進一步證實了西地那非對精子功能無影響,文章發表於《英國臨床藥理學雜誌》,BritishJournalofClinicalPharmacology
2003年,120項對照研究證實西地那非不增加心梗/心血管死亡風險,文章發表於《國際臨床實踐雜誌》,InternationalJournalofClinicalPractice
2004年,研究證實,西地那非通過改善勃起,改善患者的自信心、自尊心、與性伴侶的關係以及整體生活質量(SEAR和QoL)
2005年,Viagra已有超過75萬醫生處方,超過2300萬男性使用
2006年,研究進一步證實Viagra幫助男性達到第4級勃起硬度(最佳勃起硬度),文章發表於JournalofSexualMedicine
2007年,4年長期研究證實Viagra的長期安全性和長期療效,文章發表於TherapeuticsandClinicalRiskManagement
2008年,研究證實,勃起硬度是ED患者的重要治療期待,SCORED研究發表於InternationalJournalofImpotenceResearch
2009年,彩超研究證實,100mgViagra治療顯著改善陰莖血流,文章發表於JournalofSexualMedicine
2010年,薈萃分析進一步驗證其安全性(67項雙盲安慰劑對照研究),文章發表於InternationalJournalofClinicalPractice
2011年,西地那非在Pubmed資料庫收錄的文獻已超過4800篇,有超過3800萬男性使用Viagra
2012年,萬艾可10粒裝在中國上市
2013年,萬艾可新品包裝上市
2014年,萬艾可在華專利到期。
2014年,白雲山醫藥集團獲得“偉哥”商標使用授權,生產白雲山偉哥——金戈。商標使用許可備案號:20150000019385。
規格
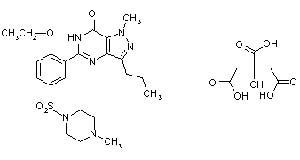 分子式
分子式國內1粒/盒(100mg/粒)128元;5粒/盒(100mg/粒)495元;10粒/盒(100mg/粒)965元
國外30粒/瓶(100mg/粒)240美元;4粒/盒(100mg/粒)60美元。
執行標準
WS1-(X-010)-2010Z
批准文號
25mg:國藥準字H20020526
50mg:國藥準字H20020527
100mg:國藥準字H20020528
成分與作用
偉哥所包含的成分及使用的藥物相互作用:
1、成分
枸櫞酸西地那非的化學名為1-[4-乙氧基-3-(6,7-二氫-1-甲基-7-氧代-3-丙基-1-氫-吡唑並[4,3d]嘧啶-5-基)苯磺醯]-4-甲基哌嗪枸櫞酸鹽。分子式為C22H30N6O4S·C6H8O7,分子量為666.67。本品為淺藍色菱形薄膜衣片。
2、其他藥物對西地那非的作用
體外實驗:本品代謝主要通過細胞色素P4503A4(主要途徑)和2C9(次要途徑),故這些同功酶的抑制劑會降低西地那非的清除。
體內實驗:健康志願者同時服用本品50mg和西咪替丁(一種非特異性細胞色素P450抑制劑)800mg,導致血漿內西地那非濃度增高56%。
單劑西地那非100mg與細胞色素P4503A4的特異性抑制劑紅黴素(500mg,一日兩次,共5天達到穩態)合用時,西地那非的藥時曲線下面積(AUC)升高182%;單劑西地那非100mg與另一種CYP4503A4抑制劑HIV蛋白酶抑制劑saquinavir合用,達到穩態時(1200mg,一日三次),則後者的Cmax提高140%,AUC增加210%,西地那非不影響後者的藥代動力學;酮康唑、伊曲康唑等更強效的CYP4503A4抑制劑,上述作用可能更大;當與CYP4503A4抑制劑(如酮康唑、紅黴素、西咪替丁)合用時,西地那非的清除率降低。可預測同時服用CYP4503A4的誘導劑(如利福平)將降低血漿西地那非水平。
單劑抗酸藥(氫氧化鋁/氫氧化鎂)對本品生物利用度沒有影響;CYP4502C9抑制劑(如甲苯磺丁脲、華法令)、CYP4502D6抑制劑(如選擇性5-羥色胺再攝取抑制劑、>三環抗抑鬱藥)、噻嗪類藥物及噻嗪類利尿劑、血管緊張素轉換酶抑制劑、鈣通道阻滯劑等,對西地那非的藥代動力學沒有影響。
襻利尿劑和保鉀利尿劑可使西地那非活性代謝產物(N-去甲基西地那非)的AUC增加62%,而非選擇性?-受體阻滯劑使其增加102%。這些對西地那非代謝產物的影響不會引起臨床變化。
3、西地那非對其他藥物的作用
體外實驗:本品是一種細胞色素P4501A2、2C9、2C19、2D6、2E1和3A4(IC50>150μM)的弱抑制劑。由於服用推薦劑量西地那非後其血漿峰濃度約為1μM,故西地那非不會改變這些同功酶作用底物的清除。
體內試驗:高血壓患者同時服用西地那非(100MG)和氨氯地平5MG或10MG,仰臥位收縮壓平均進一步降低8mmHg,舒張壓平均進一步降低7mmHg。未發現經CYP4502C9代謝的甲苯磺丁脲(250MG)和華法令(40mg)與西地那非有明顯的相互作用。西地那非(50MG)不增加阿司匹林(150MG)所致的出血時間延長。健康志願者平均最大血漿酒精濃度為0.08%時,西地那非(50MG)不增強酒精的降壓作用。西地那非(100mg)不影響HIV蛋白酶抑制劑saquinavir、ritonavir穩態時的藥代動力學,後二者都是CYP4503A4的底物。
鑑別:(1)本品含量測定項下所附的色譜圖中,供試品溶液主成分的保留時間應與對照品溶液主成分峰的保留時間一致。
(2)取本品一片,加入25ml甲醇-水-氨水(75:25:1)混合溶劑,振搖使崩解,超聲2分鐘,鏇轉混合1分鐘,以每分鐘3000轉離心15分鐘,取5ml上清液,以混合溶劑稀釋至10ml,搖勻,作為供試品溶液。另取枸櫞酸西地那非對照品,以混合溶劑製成每1ml中約含西地那非0.5mg的溶液,作為對照品溶液,照薄層色譜法(中國藥典1995年版二部附錄VB)試驗,取上述兩種溶液各5(l,分別點於同一矽膠GF254薄層板上,以正己烷-乙醇-氨水(30:70:1)為展開劑,層析缸預先以展開劑飽和至少20分鐘。展開後晾乾,在碘蒸汽中薰5分鐘後,置254nm紫外燈下檢視,供試品溶液所顯主斑點的顏色和位置中華人民共和國國家藥品監督管理局發布中國藥品生物製品檢定所審核國家藥品監督管理局藥品審評審員會審訂輝瑞製藥有限公司(中國(大連)提出本標準自2000年2月19日起試行,試行期3年保護期12年,保護期內,其它單位不得仿製應與對照品溶液的主斑點相同。
(3)本品顯枸櫞酸鹽的鑑別反應(2)(中國藥典1995年版二部附錄III)。
性狀
 萬艾可
萬艾可作用機理
5型磷酸二酯酶(PDE5)是西地那非的作用靶點,磷酸二酯酶是NO-cGMP通路的負調節因子,它通過催化cGMP的分解而調低一氧化氮的作用,一般認為體內的一氧化氮是一個調節血管平滑肌擴張的因子,因而磷酸二酯酶作用的結果是促進血管平滑肌的收縮。
西地那非可以高選擇性的抑制人體內PDE5活性,PDE5在陰莖海綿體內表達水平極高,而在人體其他組織和器官中則表達較低。服用西地那非後,陰莖海綿體血管平滑肌在藥物的作用下舒張,血液流量增加,海綿體充血,陰莖勃起,從而產生對陰莖勃起功能障礙的治療作用。
臨床實驗顯示,在歐美人中,約有78%的受試者服用西地那非後有明顯作用,其作用程度隨藥物在血液中濃度的升高而提升。其作用時間持續約4小時。
適應症
西地那非的主要適應症為陰莖勃起功能障礙,以及肺高壓與高山症預防等。
在實際套用中,一些保健品生產廠商在其產品中加入西地那非成分以期令使用者獲得更加明顯的效果,但由於在保健品中使用西地那非的用量沒有嚴格的控制,因而可能會對使用者產生不良影響。
不良反應
萬艾可®能引起嚴重的副作用。很少報告的副作用包括:持續勃起(異常勃起)。如果你持續勃起超過4個小時,立即尋求醫療幫助。如果不即刻處理,異常勃起能對你的陰莖產生永久性損害。單眼或雙眼突然視力喪失。單眼或雙眼突然的視力喪失是一種嚴重的眼病徵兆,這種眼病被稱為非動脈性前部缺血性視神經病變(NAION)。如果你出現單眼或雙眼突然的視力喪失,停止服用萬艾可®,並立即通知你的醫護人員。突發聽力減退或聽力喪失。某些人可能會出現耳朵嗡嗡響(耳鳴)或頭暈。如果你出現這些症狀,立即停止服用萬艾可®並聯繫醫生。
心臟病發作、中風、心律不齊和死亡很少發生在服用萬艾可®的男性中。這些人的絕大多數(雖非全部)在服用萬艾可®之前原已存在心臟問題。尚不清楚是否由萬艾可®引起這些問題。
主要表現
1、頭痛:臨床試驗中發現,約有1%的人服藥後出現頭痛,且服用劑量越大愈烈。
2、眼花:約有0.3%的服藥者可發生短暫的視力模糊,有的還會出現看見藍光的幻覺。
3、昏暈:可能造成血壓驟降,如同時服用硝酸甘油等藥物,常會立即頭昏甚至暈倒。
4、掩蓋心血管疾病:陽痿可能是心臟疾病、糖尿病或癌症的先兆,服用該藥可能掩蓋真正的病情。
5、血壓降低:偉哥可引起血壓降低,而含三硝酸甘油或硝酸鹽等心臟病藥物也會降低血壓,故偉哥與這些藥混用時血壓會大大降低,有時可能危及生命。
7、青光眼:眼科專家警告,服用偉哥可導致血壓下降,但青光眼患者眼壓較高,有3%~5%的人可能出現急性青光眼,可使人一夜失明,即使治好也不能恢復原來視力。
8、暫時性耳聾:FDA報導,偉哥可致聾,約1/3為暫時性耳聾。
9、加重睡眠呼吸暫停:梗阻性睡眠呼吸暫停是由於在睡眠中喉部軟組織塌陷,阻塞氣道導致短時間的呼吸停止而產生的常見病症。
上市前的經驗
在全球範圍的臨床試驗中,三千七百多名患者(年齡19-87歲)服用了西地那非。其中五百五十多名患者的治療時間在一年以上。
在安慰劑對照臨床試驗中,試驗組因不良事件停藥率(2.5%)較安慰劑組(2.3%)無顯著差異。不良事件一般是短暫的、性質多為輕到中度。
在各種形式的臨床試驗中,試驗組患者報告的不良事件通常相似。固定劑量試驗中,某些不良事件的發生隨劑量增加而增加。通常,靈活劑量試驗更能反映藥物的推薦劑量用法,試驗中所見不良事件的性質與固定劑量試驗相似。
在靈活劑量、安慰劑對照臨床試驗中,按推薦方法服用西地那非(按需服藥),患者報告了以下不良事件:
以下不良事件雖然發生率2%,但試驗組與安慰劑組發生率相同。它們是:呼吸道感染、背痛、流感症狀和關節痛。
在固定劑量試驗中,消化不良(17%)和視覺異常(11%)在100毫克劑量組比低劑量組常見。超過推薦劑量範圍時,不良事件的表現與前相似,但報告頻度增加。
以下為對照臨床試驗中,發生率2%的不良事件。尚不能肯定其發生是否由西地那非所致。在此包括了那些可能與用藥相關的事件,但省略了輕微事件和不準確的報告。
全身反應:面部水腫、光敏反應、休克、乏力、疼痛、寒戰、意外跌倒、腹痛、過敏反應、胸痛、意外損傷。
心血管系統:心絞痛、房室傳導阻滯、偏頭痛、暈厥、心動過速、心悸、低血壓、體位性低血壓、心肌缺血、腦血栓形成、心臟驟停、心力衰竭、心電圖異常、心肌病。
消化系統:嘔吐、舌炎、結腸炎、吞咽困難、胃炎、胃腸炎、食道炎、口腔炎、口乾、肝功能異常、直腸出血、齒齦炎。
血液和淋巴系統:貧血和白細胞減少症。
代謝和營養:口渴、水腫、痛風、不穩定性糖尿病、高血糖、外周性水腫、高尿酸血症、低血糖反應、高鈉血症。
骨骼肌肉系統:關節炎、關節病、肌肉痛、肌腱斷裂、腱鞘炎、骨痛、肌無力、滑膜炎。
神經系統:共濟失調、肌張力過高、神經痛、神經病變、感覺異常、震顫、眩暈、抑鬱、失眠、嗜睡、多夢、反射遲緩、感覺遲鈍。
呼吸系統:哮喘、呼吸困難、喉炎、咽炎、鼻竇炎、支氣管炎、痰多、咳嗽。
皮膚及其附屬器:蕁麻疹、單純性皰疹、瘙癢、出汗、皮膚潰瘍、接觸性皮炎、剝脫性皮炎。
特殊感覺:瞳孔擴大、結膜炎、畏光、耳鳴、眼痛、耳聾、耳痛、眼出血、白內障、眼乾。
泌尿生殖系統:膀胱炎、夜尿、尿頻、乳腺增大、尿失禁、異常射精、生殖器水腫和缺乏性高潮。
上市後的經驗
心血管系統
上市後曾報告下列與套用西地那非有時間聯繫的嚴重心血管不良事件:心肌梗死、心原性猝死、室性心律失常、腦出血、一過性腦缺血和高血壓。上述患者絕大多數(雖非全部)原已存在心血管危險因素。所報告的事件許多發生於性活動過程中或剛剛結束後;個別發生在服用西地那非後不久尚未進行性活動時。還有一些報告的事件發生在服藥或性活動後幾小時甚至幾天。對於這些事件,尚無法確定它們是否直接與西地那非相關,還是與性活動、已存在的心血管疾病、上述因素的共同作用或其它因素有關。
特殊感覺:
上市後有突發聽力減退或喪失的個別病例報導,與使用PDE5抑制劑(包括本品)有時間相關性。其中一些患者,可能存在引起耳科相關不良事件的基礎疾病或其它因素。很多病例的隨訪信息有限。不能確定突發聽力減退或喪失是否與使用本品直接相關,是否與患者已存在聽力喪失的危險因素相關,也無法判斷是否為以上兩個因素的共同作用或是否存在其它原因。
其它事件
上市後報告的其它與服用西地那非有時間聯繫、但未在上市前研究中出現的不良事件有:
神經系統:癲癇發作和焦慮。
泌尿生殖系統:勃起時間延長、異常勃起和血尿。
特殊感覺:復視、短暫視覺喪失或視力下降、紅眼或眼部充血、眼部燒灼感、眼部腫脹和壓迫感、眼內壓增高、視網膜血管病變或出血、玻璃體剝離、黃斑周圍水腫及鼻衄等。
在PDE5抑制劑包括萬艾可的上市後套用中,均有與用藥時間相關的非動脈性前部缺血性視神經病(NAION)的罕見報告。NAION是一種可引起視力下降包括永久性喪失的疾病,在大多數但非所有情況下,這些患者均具有潛在的患NAION的解剖或血管方面的基礎或危險因素,包括但不限於:低杯盤比,年齡超過50歲,糖尿病,高血壓,冠狀動脈疾病,高脂血症和吸菸。
不能確定這些事件與套用PDE5抑制劑直接相關;或與患者的基礎血管危險因素或解剖缺陷有關;或是二者的共同作用;抑或是其他因素所致。
血液淋巴系統:血管阻塞危象與接受萬艾可治療的ED男性的臨床相關性尚不清楚。
用法用量
對大多數患者,推薦劑量為50mg,在性活動前約1小時服用;但在性活動前0.5~4小時內的任何時候服用均可。基於藥效和耐受性,劑量可增加至100毫克(最大推薦劑量)或降低至25毫克。每日最多服用1次。下列因素與血漿西地那非水平(AUC)增加有關:年齡65歲以上(增加40%)、肝臟受損(如肝硬化,增加80%)、重度腎損害(肌酐清除率﹤30ml/分,增加100%)、同時服用強效細胞色素P4503A4抑制劑(酮康唑、伊曲康唑增加200%)、紅黴素增加182%、saquinavir增加210%。由於血漿水平較高可能同時增加藥效和不良事件發生率,故這些患者的起始劑量以25mg為宜。研究表明,HIV蛋白酶抑制劑Ritonavir可使西地那非血藥水平顯著增高(AUC增加了11倍)。有鑒於此,建議服用Ritonavir的患者,每48小時內用藥劑量最多不超過25mg。
老年患者用藥
健康老年志願者(≧65歲)的西地那非清除率降低。血藥濃度較高,可能同時增加不良事件的發生,故起始劑量以25MG為宜。禁忌
服用任何劑型硝酸酯類藥物的患者,無論是規律或間斷服用,均為禁忌症。對西地那非(萬艾可)中任何成分過敏的患者禁用。
硝酸酯類藥物主要有:硝酸甘油硝酸甘油(片劑、噴霧劑、軟膏、貼膜、針劑)耐絞寧,貼保寧,永保心靈,硝酸異山梨醇酯消心痛,長效消心痛,異舒吉氣霧劑/針劑,雙硝酸異山梨醇酯安基倫緩釋,易順脈(膠囊/噴霧劑),5-單硝山梨醇酯安心脈,臣功再佳、單硝酸異山梨醇酯、德明麗珠欣樂、莫諾美地、莫諾確特、依姆多異樂定、異樂定長效、益辛保、德脈寧,三硝酸甘油酯療通脈緩釋膠囊(長效療通脈)、尼采貼,戊四硝酯長效硝酸甘油、四硝季戊醇,硝乙醇胺片四硝赤醇片。
質量標準
檢查
有關物質取本品5片,放入250ml量瓶中,加入25ml乙腈-水(9:1V/V),振搖使崩解。超聲5分鐘,以流動相稀釋至刻度,再超聲5分鐘,磁攪拌30分鐘,以每分鐘6000轉離心10分鐘,取上清液作為供試品溶液。量取供試品溶液適量,加流動相製成相當供試品溶液濃度0.1%的溶液作為預試溶液。按含量測定項下的方法,取預試溶液20(l注入液相色譜儀,調節檢測靈敏度,使主成分色譜峰面積滿足準確測量要求。另取供試品溶液進樣,記錄色譜圖至主成分峰保留時間的二倍。供試品溶液色譜圖中顯示的各雜質峰扣除輔料峰外超過主峰面積的0.1%的不得多於1個,其面積不得超過主峰面積的0.3%,雜質峰面積總和不得超過主峰面積的0.5%。含量均勻度取本品1片,置250ml量瓶中,加入5ml乙腈-水(9:1V/V)振搖使崩解,做5分鐘超聲,用流動相稀釋至刻度,再次5分鐘超聲,30分鐘磁攪拌,以每分鐘6000轉離心10分鐘。取5ml上清溶液,以流動相稀釋至25ml作為供試品溶液。照含量測定項下的方法測定含量,應符合規定(中國藥典1995年版二部附錄XE)。溶出度取本品,照溶出度測定法(中國藥典1995年版二部附錄XC,第一法),以0.01M鹽酸溶液900ml為溶劑,轉速為每分鐘100轉,依法操作。經15分鐘時,取溶液濾過,取續濾液作為供試品溶液。另取枸櫞酸西地那非對照品適量,精密稱定,用0.01M鹽酸溶解並稀釋成每1ml約含西地那非22(g的溶液,作為對照品溶液。取上述兩種溶液,照分光光度法(中國藥典1995年版二部附錄IVA),在290nm處分別測定吸收度,計算出每片的溶出量。限度為標示量的80%,應符合規定。水分取本品細粉,照水分測定法(中國藥典1995年版二部附錄VIIIM,第一法)測定,含水分不得過6.0%。含量測定
照高效液相色譜法(中國藥典1995年版二部附錄VD)測定。色譜條件與系統適用性試驗以十八烷基矽烷鍵合矽膠為填充劑,0.05M磷酸三乙胺(取7ml三乙胺用水稀釋至1000ml,用磷酸調至pH至3.0)-甲醇-乙腈(58:25:17)為流動相,檢測波長為290nm。理論板數按西地那非計應不低於3000。另取枸櫞酸西地那非對照品約70mg於250ml量瓶中,加1ml甲酸-過氧化氫(1:2V/V)溶液,以流動相稀釋至刻度,此溶液中含有西地那非及其降解產物N-氧化物,進樣20(l,西地那非與降解產物的分離度應大於2.5。外標溶液的製備精密稱取枸櫞酸西地那非對照品適量,以流動相溶解製成每1ml約含西地那非20(g的溶液,即得。測定法精密量取有關物質檢查項下供試品溶液10ml於250ml量瓶中,以流動相稀釋至刻度,搖勻,作為供試品溶液,取外標溶液及供試品溶液各20(l,分別注入液相色譜儀。記錄色譜圖,按外標法以峰面積計算,即得。辨別方法
真假萬艾可
 萬艾可
萬艾可 1.正品包裝精緻,光滑,效果顯著;假冒商品包裝粗燥,極不規範,每粒大小不一、粗燥。
2.顏色為藍色,正品表面色澤好,光滑發亮。假冒顏色成深藍,表面粗糙,無光澤。
3.表面都刻有文字,正面有“vgr100”字樣,背面有“pfizer”字樣。
4.性狀為白色結晶粉末,藥片為藍色薄膜衣、圓菱型,除去薄膜衣後仍為白色結晶粉末,每片劑量為100mg。
5.採用新變色防偽標識;直視標籤上的橢圓形“pfizer”標識與轉換角度斜看“pfizer”標識時顯示不同的顏色;用手觸摸橢圓形“pfizer”標識,有的凹凸感。
6.瓶裝偉哥採用的是壓力防偽瓶蓋;需要輕輕用力壓住瓶蓋,逆時針鏇轉才能打開瓶蓋。
外觀辨別
正品體積比仿造的略小,表面和周邊都比較光滑。正品表面為啞光。
正品偉哥是易溶於水的,在水中快速溶解為粉末狀,但不在水中擴散。假偉哥在水中擴散,並呈顆粒狀。這點就非常容易區別了。
瓶裝辨別
瓶裝的均為真貨。
專利權之爭
雖然輝瑞在全世界絕大多數國家享有西地那非的專利權,但是在一些國家,他們失去了這一特權,這些國家包括南美洲的玻利維亞、哥倫比亞、秘魯,歐洲的英國等,中華人民共和國國家知識產權局也曾在2004年否決了輝瑞公司提出的西地那非用於治療陰莖勃起障礙的用途專利申請。2006年6月2日,北京市第一中級人民法院判決美國輝瑞製藥公司贏得了專利訴求的勝利。2014年5月萬艾可在中國的專利保護到期。同年9月18日,廣藥白雲山率先發布了首箇中國產“偉哥”——金戈。
造假偉哥
2014年9月1日,歐洲多個國家展開“打擊假冒偉哥藥品”的突擊行動。警方繳獲大量從中國和印度走私的假冒偉哥,並逮捕12名嫌犯。歐洲檢察官組織1日在一份聲明中稱,奧地利、比利時、賽普勒斯、匈牙利和英國參加了此次打擊假冒偉哥的行動。警方共繳獲數百萬顆藥丸,價值超過1000萬歐元,以及大量現鈔和數輛汽車,其中包括豪華轎車。超過750萬歐元的銀行存款被凍結。報導稱,這些假藥在中國和印度生產,主要通過海運和郵寄走私到歐洲。,