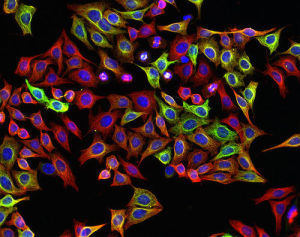
名稱由來
Hela細胞源自一位名叫HenriettaLacks美國婦女的子宮頸癌細胞的細胞系。這名美國婦女在1951年死於該癌症。為了讓拉克斯保持匿名,此細胞株原宣稱是依“HelenLane”命名。特點
1、可以連續傳代。
2、細胞株不會衰老致死,並可以無限分裂下去。
3、此細胞系跟其它癌細胞相比,增殖異常迅速。
4、感染性極強。
細胞之母
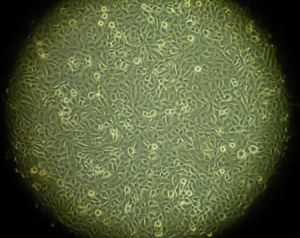 hela細胞
hela細胞已證實Hela細胞系難以控制。此細胞系有時會污染同一實驗室的其他細胞培養物(cellculture),干擾生物學的研究。污染程度難以估計,因為研究人員很少檢定已確立細胞系的本質和純度。據說有相當數目的體外細胞系(invitrocelllines)其實就是HeLa細胞系,因為原先的細胞株已被快速增殖的HeLa細胞系污染物取代了。
有學者認為此細胞系是一新的物種,因為此細胞株能自行繁殖和散布。在1991年此細胞株被命名為Helacytongartleri。 Hela細胞生長奇快,甚至超越一般癌細胞。Hela細胞經歷細胞分裂時可維持端粒酶活性以維持端粒長度,一般細胞的端粒會隨著老化而變短,終至細胞死亡。海樂細胞利用此機制避開海佛烈克極限(Hayflicklimit)。
傳代步驟
1、觀察培養基是否正常,細胞狀態如何,細胞密度如何,決定是否傳代。觀察時擰緊蓋子。2、加熱PBS、versene、培養基,(提前做好)瓶子不要倒著放,不要讓液體接觸到瓶塞。
3、打開超淨台(先開風機,後開照明),用75%乙醇清潔台面,點燃酒精燈。不要把廢液缸拿出去倒,如果廢液太多,可以用其他容器先裝廢液。取小離心管一個,置於架子上。
4、取尖吸管、吸量管各一支,放置在專用的架上。放置的方式,注意吸管、吸量管前端都不要與架子接觸。
5、取待傳代的細胞。打開versene,用酒精燈外焰燒。燒吸管時距離酒精燈心遠些,不要把渣滓帶進去。把試劑拿入台子的時候,儘量平穩,不要讓試劑碰到瓶口。
6、用吸量管吸取舊的培養基,置離心管中,吸量管加入versene,然後將versene瓶收起來。(加versene主要是為了將舊培養基洗去)。在離心管中間部分將液體加入。吸液體和加液體時都不要對著細胞。
7、打開胰酶,然後將versene棄掉。換新管,用尖吸管吸取適量胰酶加入。加胰酶後,儘快放平,使細胞消化時間一致。
8、將細胞放入37度孵箱。放孵箱2min,收胰酶,打開PBS.之後拿出來鏡下隨時觀察。使用二次消化法,去除容器中殘餘的細胞。別忘了用舊培養基中和。
9、取細胞,鏡下觀察消化情況。消化程度合適之後(細胞變圓,但不漂起),用尖吸管棄去胰酶,取離心管中的培養基加入細胞,吹打,至所有細胞從培養皿底部脫落下來。用PBS洗細胞,versene對細胞有毒性,且不能被血清中和。然後吸取至離心管中,800rpm離心5分鐘。
10、吸量管吸取適量培養基加入新的培養皿中。
11、細胞離心畢,用吸新培養基的管棄去上清,先把泡沫吸走。換吸量管吸取培養皿中培養基適量,加入離心管,小體積混勻,將細胞重懸,尖吸管吹勻。
12、擦計數板,用槍吸10ul的液體,計數。不要把槍伸到離心管內。
13、吸量管吸取細胞懸液,加入新的培養皿中。鏡下觀察,搖勻,放入37度孵育。收超淨台。
與遺傳學關係
得益於Hela細胞,基因檢測的原理才被發現。1953年,一位用Hela細胞進行實驗的研究人員發現,一種名為蘇木蘇的著色劑能夠讓細胞核的染色體清晰可見,利用這一發現,科學家成功找出了唐氏綜合症等疾病的遺傳聯繫,並逐漸掌握遺傳性疾病的診斷方法。
1954年,Hela細胞幫助科學家實現了細胞克隆。科學家利用其具有頑強生命力的特徵,發明了一種分離單一細胞的方法,並讓其存活足夠長的時間來複製和創造一個自身的完美拷貝。這一重大突破為動物克隆、基因療法、試管受精和幹細胞分離等尖端生物醫學奠定的基礎。
1965年,Hela細胞幫助實現了基因混合。通過將海拉細胞和小鼠細胞融合,人類首次創造了跨物種混合體。基因泥合技術不僅讓人們成功繪製人類基因圖譜、進行血型鑑定,也帶動了抗癌藥物赫塞汀的發明。另外,小鼠和人的Hela細胞中的氯黴素抗性的遺傳屬於染色體處遺傳,該抗性和線粒體有關。
1973年,科學家利用Hela細胞模型沙門氏菌的擴散,測定基傳染性,產研究其在人體細胞中的活動。
1993年,研究人員讓Hela細胞感染結核桿菌DNA,明白了細菌如何侵襲人類細胞。
套用
 Hela細胞
Hela細胞 Hela細胞系被GeorgeGey分送給眾研究單位(並未通知拉克斯本人也未得到她的許可),並用作癌症模式細胞(modelcancercells)研究。HeLa細胞系也被用作研究細胞信號傳導(cellularsignaltransduction)。
1952年研究人員用各種從腮腺炎、麻疹到皰疹疾病組織分離來的病毒感染Hela細胞,由此現代病毒學產生。
1956年,Hela細胞先於人類,隨一顆前蘇聯衛星進入太空,開始被用於太空生物學研究。美國宇航局後來還在首次載入太空梭中攜帶了海拉細胞,並發現癌細胞在太空中繁殖更快。
1984年,一名德國病毒學家利用Hela細胞證明了人乳頭狀病毒(HPV)會導致癌症,這項發現後來讓這名德國人獲得了諾貝爾獎,也向HPV疫苗的成功研製邁出了第一步。
1986年,科學家發現如何讓Hela細胞感染人體免疫缺陷病毒(HTV)。通過它找到了一個關鍵受體,揭示了這種病毒的感染機制。
1989年,一位Yale大學的研究人員公布了一項科學發現,Hela、癌細胞含有一種叫做端拉酶的物質,能使細胞不死。這讓控制生物衰老的神秘物質——端粒酶走進了人們的視線。
爭議
 海拉
海拉Steinmetz與他的團隊在位於德國海德堡的歐洲分子生物學實驗室工作。他們認為,Hela細胞基因組有助於檢驗基因變異如何對基本的生物功能產生影響,並且他們願意將研究成果與眾多其他致力於研究海拉細胞系的科學家分享。
但是HenriettaLacks的後代(海拉細胞源自她的子宮頸癌細胞),以及其他科學家和生物倫理學家卻不這樣認為。他們批判將基因序列公開發布這一行為,認為Hela細胞系的提取並未獲得Lacks本人的同意(於1951年她死後獲取),並且Steinmetz與他的團隊發布的研究成果可能會泄露依然健在的Lacks後代的基因特徵。
作為回應,Steinmetz與他的團隊將基因組數據從公共資料庫中移除。Steinmetz說:“我們感到很驚訝,根本沒想到會導致這樣的後果。我們尊重Lacks家人的意願,絕對不是蓄意發布研究成果使他們焦慮。”