鋼的脫磷反應
正文
減少鋼液中含磷量的化學反應。磷是鋼中有害雜質之一。含磷較多的鋼,在室溫或更低的溫度下使用時,容易脆裂,稱為“冷脆”。鋼中含碳越高,磷引起的脆性越嚴重。一般普通鋼中規定含磷量不超過 0.045%,優質鋼要求含磷更少。生鐵中的磷,主要來自鐵礦石中的磷酸鹽。氧化磷和氧化鐵的熱力學穩定性相近。在高爐的還原條件下,爐料中的磷幾乎全部被還原並溶入鐵水。如選礦不能除去磷的化合物,脫磷就只能在(高)爐外或鹼性煉鋼爐中進行。鐵中脫磷問題的認識和解決,在鋼鐵生產發展史上具有特殊的重要意義。鋼的大規模工業生產開始於1856年貝塞麥(H.Bessemer)發明的酸性轉爐煉鋼法。但酸性轉爐煉鋼不能脫磷;而含磷低的鐵礦石又很少,嚴重地阻礙了鋼生產的發展。1879年托馬斯(S.Thomas)發明了能處理高磷鐵水的鹼性轉爐煉鋼法,鹼性爐渣的脫磷原理接著被推廣到平爐煉鋼中去,使大量含磷鐵礦石得以用於生產鋼鐵,對現代鋼鐵工業的發展作出了重大的貢獻。
鹼性渣的脫磷作用 脫磷反應是在爐渣與含磷鐵水的界面上進行的。鋼液中的磷 【P】和氧 【O】結合成氣態P2O5的反應:
2【P】+5【O】─→P2O5
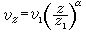 (1)
(1)1600℃時的平衡常數非常小(K1=4.4×10-10),要靠生成P2O5氣體逸出而使鋼液脫磷,顯然是不行的。但如果鋼液和鹼性渣接觸,P2O5就會與渣中的氧化鈣(CaO)結合成穩定的3CaO·P2O5或4CaO·P2O5,總反應是:
2【P】+5【O】+3(CaO)─→(3CaO·P2O5) (2)
1600℃時,K2=1.7×108或 2【P】+5【O】+4(CaO)─→(4CaO·P2O5) (3)
1600℃時,K3=3.5×108平衡常數如此大,說明鹼性渣的脫磷能力是很強的。熔渣離子理論認為:鹼性渣中含有自由的氧離子O2-,它能與P2O5結合成穩定的PO婯離子,脫磷反應是:
2【P】+5【O】+3(O2-)─→2(PO婯) (4)
不管是分子理論或離子理論,但是有一個重要的事實是:3CaO·P2O5、4CaO·P2O5和PO婯都有很高的熱力學穩定性。根據熔渣陰離子聚合模型(見馬松模型),PO婯還能與渣中的矽-氧鏈結構形成SiPO叅、Si2PO喒、Si3PO喐等穩定的複合陰離子。
渣量、FeO含量、溫度對脫磷的影響 增大渣量,或將含磷多的爐渣放出,另造新的鹼性渣,都是使鋼液有效脫磷的措施。渣中含有足夠量的 FeO不僅可以向鋼液傳送氧,還能使加入爐內的固體石灰更快地溶入渣中,使渣中自由的O2-離子增多,從而提高熔渣的脫磷能力。脫磷是放熱反應,溫度較低有利於反應的進行。
各種煉鋼方法脫磷的特點 在平爐煉鋼及電弧爐煉鋼氧化期中,渣中含有足夠數量的 FeO;在氧氣頂吹轉爐煉鋼中,調節氧槍位置高低也可保持渣中含有一定量的 FeO,在脫碳的同時也可以脫磷。但在空氣底吹轉爐煉鋼(托馬斯法)時,脫磷與脫碳不能同步進行。其主要原因是:空氣穿過鋼水時,其中的氧被矽、錳、碳的氧化所消耗殆盡,渣中缺乏足夠量的FeO,加入的固體石灰也很少溶入渣內,渣的脫磷能力很差。只有待吹煉後期,鋼中碳降到很低時,渣中FeO含量增大,使固體石灰迅速溶解入渣後,才能有效地脫磷。這稱為“後吹”去磷。氧氣底吹轉爐煉鋼也有類似的情況,主要靠後吹去磷。為避免後吹,可用吹入石灰粉或人造合成渣的辦法以加速石灰的溶解,提早去磷。
回磷及防止方法 脫磷反應速度甚快,容易接近平衡。在鋼水脫氧時,溫度較高,如果渣中CaO含量不夠高,加入脫氧劑後,鋼中溶解的氧減少,這些不利於脫磷的條件湊在一起,會使去磷反應的平衡向反方向轉移,鋼中含磷回升。這種現象稱為“回磷”。在氧氣頂吹轉爐煉鋼中,如果槍位過低、渣中FeO少,也會使渣趨於回磷。為減少回磷,應儘可能在出鋼時使渣量減少,並在渣中加入石灰,使渣變稠。電爐煉鋼在氧化期結束時,要儘可能地將含磷的氧化性渣排出爐外,以防止還原期回磷。
脫磷的定量計算 可以採用下式:
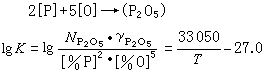
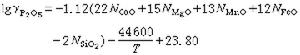
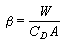
參考書目
R.G.Ward,An.Introduction to Physical Chemistry of Iron and Steelmaking,E.Arnold,London,1962.
C.Bodsworth & H.B.Bell,Physical Chemistry of Iron and Steel Manufacture,2nd ed.,Longman,London,1972.
