簡述
執行轉座功能的酶,通常由轉座子編碼,識別轉座子兩端的特異序列,能把轉座子從相鄰序列
 轉座酶
轉座酶TnsABC*轉座酶
TnsABC*轉座酶可用在GPSTM系列系統中(GPS-1基因組測序系統,GPS-M突變系統和GPS-LS蛋白質結構分析系統)將PGPS質粒中的Transprimer轉座元件體外隨機插入到任何期望的靶DNA內(1-3)。
來源:三個組成蛋白分別從含有編碼TnsA、TnsB和TnsC*的質粒的E.coliK-12中純化獲得。
套用:用於GPS系統中所用到的Tn7源轉座子的轉位。
反應緩衝液:1×GPSBuffer25mMTris-HCl,2mMATP,2mMDTT(pH8.0@25°C)。補充15mM鏈轉移反應起始溶液。37°C溫育。
單位定義:在用0.08µg2.8kb對照質粒的標準對照反應體系中,能使至少1%的靶分子獲得轉座子插入所需要的酶量定義為一個單位。
熱失活:75°C10分鐘。
原核生物轉座因子的類型
(一)插入序列(IS)
IS1是基因組中可移動的遺傳因子家族中的成員之一,它可以整合到宿主非同源位點上,這就是轉座(tronsposition),若IS插入到某基因內,通常這個基因就會失活。這種精確的作用取決於IS有關的狀況。例如IS2因子以同一方向插入到染色體中,則會減少基因的表達,但以相反方向整合,則會增加基因表達。相比這下IS1因子不論以什麼方向插入都會降低基因的表達。
IS原來分為IS1~4,後面的數字反應它們被分離的先後次序和轉座因子的總數無關。
正常的細菌染色體和質粒都含有IS。E.coli的標準品系似乎含有各種拷貝數(<10)的IS因子。在原核生物中IS家族有很多成員,它們的結構相似,兩端都有短的正向重複序列(directrepeats,DR)(靶序列),略長的反向重複序列(invertedrepeats,IR)以及1kb左右的編碼區,它僅編碼和轉座有關的轉座酶。對靶的選擇有三種形式:隨機選擇,熱點選擇和特異位點的選擇。
由於IS中有反向重複序列的存在,因此如果質粒上有IS,那么經變性和復性後,在電鏡下可以觀察到莖環結構的存在(圖23-30)。
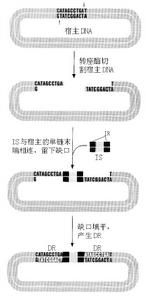
IS的轉座是由轉座酶(transposase)催化的,它由IS編碼。首先轉座酶交錯切開宿主靶位點,然後IS插入,與宿主的單鏈末端相連線,餘下的缺口由DNA聚合酶和連線酶加以填補,結果使插入的IS兩端形成了DR或靶重複。
(二)類插入序列(IS-likeelements)是指IS10R,IR50R和IS903,它們的結構和IS相似,但不獨立存在。而是作為複合轉座子(compositetransposons)兩臂的組件。
(三)複合轉座子。複合轉座子要比IS長得多,中心區域編碼抗性標記。不同的複合轉座子的抗性標記不同。複合轉座子兩端的組件由IS和類IS組成。有的二側組件相同(如Tn903),有的不同(如Tn10)。有的方向相同(如Tn9),有的方向相反(如Tn903,10,5)。有的皆有功能(如Tn903,10),有的僅右側組件有功能。
據推測當兩個獨立的組件與中心區域連線時發展成複合轉座子。這個結構可能由IS因子轉座到緊靠供體位點的受體位點上。這兩個組件可能相同或存在差異。單個組件轉座整個複合轉座子的能力解釋了兩個組件保持活性不受選擇壓力的影響。
在複合轉座中是什麼替代單個組件而擔負起座的作用呢?特別是在兩個組件都有功能的情況下。在Tn9例子中,它的組件是IS1因子,推測它們都有功能。為什麼轉座是整個複合轉座,而不是IS的本身呢?
兩個IS因子能使夾在其中的任何序列轉座。如一個環狀複製子上的Tn10它的兩個組件IS10L和IS10R,也可以看成是複製子序列兩端的組件,因此在進一步轉座時它不僅可以使Tn10轉座,也可心使複製子序列轉座,但兩側面組件的序列與在Tn10中不同。
(四)TnA家族
轉座子(transposon,Tn)另一家族是TnA,長約5kb左右,兩端具有IR,而不是IS,中部的編碼區不僅編碼抗性標記,還編碼轉座酶和解離酶。
TnA是複製轉座的轉座子。在此家族中Tn3和Tn1000(γδ)研究得最深入。通常末端有38bp左右的IR,在兩個IR中任一個順式作用缺失都會阻止轉座。5bp的正向重複是靶位點產生的。它們都帶有抗性標記(圖23-33)。
TnpA介導轉座分為兩步,分別由tnpA,、tnpR編碼的轉座酶(transposase)和解離酶(resolvase)來完成的。這兩個酶是通過實變鑑別出來的。此類轉座和末端的IR有關。解離順序(res)是內部的特殊位點,只有TnA家族才具有這一位點。
tnpA突變體是不能轉座的,這個基因的產物是一種轉座酶。它可以結合在末端38bpIR中的25bp的序列上。E.coliIHF的結合位點就在轉座酶結合位點附近(在靶位點附近)。而轉座酶結合和IHF的結合是協同性的。轉座酶識別末端重複序列,並可以使靶DNA產生5bp的交錯切割使轉座子插入。IHF是一種DNA結合蛋,常在E.coli中組裝成一個大分子,它在轉座反應中並不起作用。
tnpR的產物具有雙重功能,一是作為基因表達的阻遏物,另一個作用是具有解離酶的功能。tnpR突變將增加轉座預率,這是由於TnpR阻遏了tnpA和它自己的基因轉錄,TnpR蛋白失活就使TnpA合成增多,結果增加了轉座的頻率。這表明TnpA轉錄酶的數量一定是轉座的限制因子。
tnpA和tnpR基因之間有一個富含A-T的內部順式控制區,TnpR的兩種功能就是通過和此區的結合來實現的。
採用經修飾的TN5轉座酶的體外轉座系統
一種體外轉座系統,該系統包含包括側接一對細菌轉座子Tn5外末端重複序列的可轉座元件的DNA供體分子、可轉座元件能夠轉座到其中的DNA靶分子以及一種經修飾的Tn5轉座酶,該轉座酶與外末端重複序列結合的親合力高於野生型Tn5轉座酶,呈失活多聚體形式的可能性低於野生型Tn5轉座酶。
一種對可轉座DNA序列進行體外轉座的系統,該系統包含:相對於野生型Tn5轉座酶進行過修飾的Tn5轉座酶,該經修飾的轉座酶包含:一個相對於野生型Tn5轉座酶的變化,該變化使經修飾的轉座酶與Tn5外末端重複序列結合的親合力高於野生型Tn5轉座酶;另一個相對於野生型Tn5轉座酶的變化是,該變化使經修飾的轉座酶呈失活多聚體形式的可能性低於野生型轉座酶;DNA供體分子,該分子包含可轉座的DNA序列,DNA序列的5′和3′端側接了Tn5外末端重複序列;和可轉座元件能轉座到其中的DNA靶分子。
設計動物變容易了
一種蠅類DNA的環狀片段可能會使進行了遺傳修飾的動物迅速增加,如同涓涓溪流變成滔天洪水一樣。舊金山的Tosk生物技術公司聲稱它可以藉助能跳入和跳出染色體的果蠅DNA以前所未有的效率將基因添加到哺乳動物細胞中。該公司的聲明受到了其他生物學家們夾雜著熱誠與懷疑的複雜成分的歡迎,他們警告說它的結果尚未被完全確定。來自紐約斯托尼布魯克大學的TomRosenquist說:“如果它的結果如同他們所聲稱的那樣,它將是革命性的。”目前,將外源基因導入哺乳動物體內的技術僅停留在實驗室階段並且代價昂貴,因此該項技術僅用於研究和製造能產生高價值醫藥產品的動物。但是,如果製造GM動物(遺傳修飾動物)變得便宜而且容易了的話,各個公司很快就可以對每種動物都進行修飾,包括從提供我們食物的農場動物到我們的寵物。Tosk的方法甚至可以用來改正人們的遺傳缺陷。現在,GM哺乳動物通常採用在卵細胞中直接插入裸露DNA的方法。但是其成功率十分低:為了得到一個GM動物,一個熟練的技術人員也不得不進行若干次插入試驗,然後將其中成功的胚胎移植培養。而另一種方法是從普通細胞開始,然後盡力去克隆整合了外源DNA的少數細胞。但是該方法的效率也不高。據《新科學家》雜誌報導,Tosk的方法排除了上述繁雜的操作,外源DNA被簡單地插入動物的血液中。據Tosk執行長PatrickFogarty聲稱,外源DNA將在兩周之內以一個高比例整合到許多不同組織的細胞之中。由於一些精細胞和卵細胞也被改變了,通過正常的繁殖就能產生出每個細胞都攜帶外源基因的動物。Fogarty聲稱當小鼠通過尾部插入DNA而被修飾後,在其後代中約有平均40%的小鼠攜帶外源DNA——這是一個令人震驚的高比例。Tosk的秘密就在於使用跳動基因或轉座子,它們已經在很多生物體中被發現。它們是遺傳的寄生元件:沒有功能的DNA環狀片段,其僅有的獨特能力就是在一種名叫轉座酶的“剪下和貼上”酶的幫助下通過跳入和跳出DNA來向四處傳播。典型的轉座子由編碼轉座子酶的基因所組成,其兩側帶有獨特的標記序列。當轉座酶產生後,它以標記序列為目標導向將整個轉座子剪下下來,並將它貼上到細胞基因組別的位置上。最具活性的轉座子之一就是在果蠅中發現的P-元件。數十年來,科學家們已經利用該轉座子,通過將他們想轉移的基因與轉座酶基因相替換而製造出了轉基因蠅類。但是沒有人能在哺乳動物中很好地利用它。
現在,從史丹福大學來到Tosk的Fogary說,通過對P-元件結構的調整,他的研究人員可以將該元件整合到超過80%的培養的人和鼠細胞中。這一基因運送系統由兩組DNA環狀片段構成:一個包含了待導入基因,其兩側帶有標記序列;另一個則包含了P-元件轉座酶基因。大量的上述DNA環狀片段對被包裹在能幫助它們進入細胞的脂肪球中,然後插入一個動物體內。隨後,該動物的細胞開始產生轉座酶,轉座酶將外源基因剪下下來並將其貼上到細胞基因組的隨機位點上。
轉座酶基因本身不會被整合到細胞DNA上,而是在兩周后分解掉。一旦轉座酶分解掉,插入的DNA環狀片段就固定下來了。
Tosk剛開始對外開展了一項服務即製造轉基因動物,而且已有幾位科學家開始訂購了。來自倫敦帝國大學的生物學家LaurenceBugeon剛從Tosk得到了一批小鼠,他說:“如果它是真的話,它將是神奇的。”Fogarty說他們也開始與若干公司進行合作,在山羊、牛和豬中檢測這項技術。然而,到目前為止,該公司的有關實驗細節還沒有公開發表,其聲明被完全確認可能還要花上幾個月時間。其他的科學家認為該公司需要做更多的實驗來證明通過轉座子進行的基因整合確確實實發生了。
Tosk並不僅僅研究開發轉座子在基因運送方面的用途,已發表的著作中提到的對其他轉座子的套用說明該技術也許可以成為改正人們遺傳缺陷的有價值的工具。
目前,基因療法研究的主要方法是將裸露DNA注入細胞或利用病毒將DNA加到基因組上。但是,裸露DNA只能在短時間內起作用,而利用病毒則存在著明顯的安全問題。轉座子在這兩方面都有著無與倫比的優勢:穩定的整合而沒有病毒的危險。一個從魚身上提取的名叫“睡美人”的轉座子已經成功地用於與嗜血桿菌一起將基因運送到小鼠肺中。但是即使是在培養物中,“睡美人”的整合率也很低——僅僅5%-6%的細胞。Tosk聲稱它的轉座子的效率比“睡美人”高10倍,這真是一種巨大的差異。當然,需要確定的主要問題是轉座子能否成為基因療法的工具。哈佛醫學院的RichardMulligan說:“但是如果你看一看遺傳法則,就會知道它是一個神奇的系統,時間會證明這一切。”