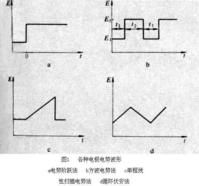
計時電流法
正文
一種研究電極過程動力學的電化學分析法和技術。在電解池上突然施加一個恆電位,足夠使溶液中某種電活性物質(或稱去極劑)發生氧化或還原反應,記錄電流與時間的變化,得到電流-時間曲線,故稱計時電流法(見圖)。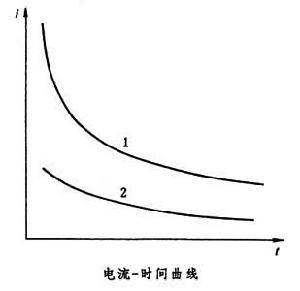 計時電流法
計時電流法1902年美國F.G.科特雷耳根據擴散定律和拉普拉斯變換,對一個平面電極上的線性擴散作了數學推導,得到科特雷耳方程:
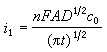
當時間趨向於無窮大,電流就趨近於零,這是因為電極表面活性物的濃度由於電解而逐漸減小的結果。利用i1或i1t1/2與c0成正比的關係,可用於定量分析,但由於此法不如極譜法準確和重現性好,所以實際上很少套用。因為
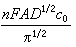 是一個常數,所以i1t1/2對t作圖得一不隨t變化的直線。
是一個常數,所以i1t1/2對t作圖得一不隨t變化的直線。 科特雷耳方程適用於擴散過程(圖中曲線1),如果電極反應不可逆或伴隨化學反應時,則動力電流ik隨時間的變化見圖中曲線2,它受反應速率常數的控制。
計時電流法常用於電化學研究,即電子轉移動力學研究。近年來還有採用兩次電位突躍的方法,稱為雙電位階的計時電流法。第一次突然加一電位,使發生電極反應,經很短時間的電解,又躍回到原來的電位或另一電位處,此時原先的電極反應產物又轉變為它的原始狀態,從而可以在i-t曲線上更好地觀察動力學的反應過程;並從科特雷耳方程出發,考慮反應速率,進行數學推導和作圖,求出反應速率常數。