簡介
胰十二指腸切除術是一種複雜且創傷很大的腹部手術,切除範圍包括部分胰腺、鄰近的十二指腸、膽管下端、部分胃及空腸上端,並且需作膽總管、胰管、胃與空腸的吻合。手術方式包括胰頭十二指腸切除術、擴大胰頭十二指腸切除術、保留幽門的胰十二指腸切除術、全胰腺切除術等。療效發展
胰腺癌的發病率正在增高,據報導在美國最常見的因癌症死亡的病例中胰腺癌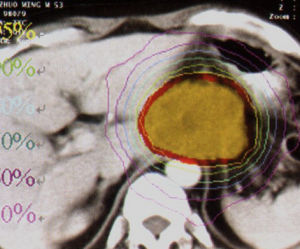 胰十二指腸切除術
胰十二指腸切除術除術是治療這類腫瘤比較有效的療法,但其療效仍不能使人滿意。胰頭癌最差,其他幾種類型癌略好些,但總的手術切除率僅30%,手術死亡率和切除術後五年治癒率均僅10%左右。
胰頭部包括下部膽管與十二指腸,從胚胎髮生學和解剖學來看關係密切,行胰頭切除時合併十二指腸切除曾被認為是不可避免的。胰十二指腸切除術(PD)及保留幽門的胰十二指腸切除術(PPPD)被認為是慢性胰腺炎胰頭部腫塊和良性腫瘤的經典術式。但手術創傷大,破壞了消化道的連續性。Beger等於1972年倡導保留十二指腸的胰頭切除術(duodenum2preservingpancreaticheadresection,DP2PHR)治療慢性胰腺炎胰頭部腫塊。其後有許多學者在Beger手術的基礎作了改進[1]。1990年文獻[2]報告Imai2zimi等對胰頭部低度惡性腫瘤及良性病變採用保留十二指腸的胰頭全切除術(duodenum2preservingtotalpancreaticheadresection,DPTPHR)以降低胰漏的發生率。但當前,DPPHR在國內尚未普遍開展。
符合條件
1.胰頭部癌、乏特壺腹癌、膽總管下段癌、壺腹周圍的十二指腸癌。其中,胰頭癌療效較差,對壺腹周圍癌的療效較好。
2.其他如十二指腸平滑肌肉瘤、類癌、胰腺囊腺癌等疾病,必要時可選用此術。
3.不適行此手術的情況是:肝已發生轉移;膽總管和肝管轉移;肝門、膽總管周圍和胰上方淋巴結廣泛轉移;腫瘤已侵及門靜脈和腸系膜上靜脈;胰頭或壺腹周圍已與下腔靜脈或主動脈緊密粘連。
4.對長期嚴重黃疸,條件極差的病人,可先行膽囊空腸近段端側吻合或先行ptcd、ercp引流後,待病情好轉後再行二期或擇期根治切除。二期手術一般爭取在第1期手術後10日左右施行,最遲不得超過2周。二期手術常因粘連造成困難,故原則上應儘量爭取一期根治手術。
術前準備
1.糾正全身情況,進高熱量、高蛋白飲食,輔以膽鹽和胰酶,以助消化吸收。術前反覆多次少量輸血,能提高血紅蛋白和血壓。2.治療黃疸,主要是保護和改善肝、腎功能。術前幾日每日靜脈滴注10%葡萄糖1000ml。採用茵陳、白朮、梔子、木香、鬱金、青蒿等中草藥治療,很有補益。有條件時先行ptcd或ercp引流是最好的減黃措施。
3.改善凝血功能,除反覆輸新鮮血外,應給足量的鈣和維生素k1、k3、c。術前3日肌肉注射止血劑。
4.膽道梗阻後常引起肝內感染,術前應常規套用抗生素、滅滴靈等,以預防感染。
手術詳細
改進歷程
胰頭十二指腸切除術是治療胰腺癌的主要術式。第1例壺腹周圍癌切除術是德國外科醫生Kausch於1909年分兩期進行的。1935年,Whipple用相似的方式進行了此手術,並在1942年改進為一期切除手術,切除後吻合順序為膽、胰、胃與空腸吻合,即形成今天的胰頭十二指腸切除術。1944年Child將空腸斷端和胰腺斷端吻合,然後行膽總管空腸端側吻合及胃空腸端側吻合,即胰、膽、胃與空腸吻合,稱之為Child法。Child法和Whipple法是目前較常用的手術方式。目前國內外該手術的死亡率最低的為≤2%。麻醉要求
連續硬膜外麻醉維持的時間長,反應較小,腹肌鬆弛良好,便於顯露。主要過程
A.常規探查:檢查腹腔有無遠處轉移和癌瘤侵犯,初步判定能否切除。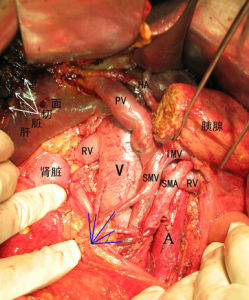 胰十二指腸切除術
胰十二指腸切除術B.分離探查:剪開十二指腸降部外側腹膜,切開肝胃韌帶及肝十二指腸韌帶,延至十二指腸水平部乃至橫結腸系膜根部,鈍性分離胰腺後疏鬆組織,向左側翻起十二指腸及胰頭部,將十二指腸和胰頭部從腹膜後充分地游離,檢查癌瘤和腔靜脈、腸系膜上動脈和靜脈、腹腔動脈和肝動脈之間有無侵犯,尤其是門靜脈的侵犯。應在胰腺後面無明顯阻力分離出門靜脈和腸系膜上靜脈,此步是最終決定能否行根治手術的關鍵,但有時雖然已能完全分離,但切斷胰腺後發現癌浸潤部分門靜脈,如右後側壁,此時,常要準備行部分門靜脈血管切除和人工血管吻合。
C.切除病變及周圍組織:切除膽囊、切斷肝總管或膽總管,如為胰頭癌,則必須在肝總管下段離斷膽管;切除遠端胃,其範圍取決於病人年齡及有無胃酸過多等,最多可達胃遠端1/2,大網膜應按胃癌根治術要求處理;切斷胰腺,其範圍一般在腹腔動脈左緣,而壺腹癌或一些良性病變則可在胰腺頸部作為切除線。在切斷胰腺時,先在胰腺邊緣四點縫扎,預防胰腺橫行血管的出血,應邊切開胰腺,邊剝離胰管並仔細保護,插入與原胰腺管管徑相適宜的矽膠管,並用可吸收線在胰腺管縫合1~2針來固定矽膠管,注意結紮胰腺背面的一些靜脈血管。在腸系膜左側根部確認出Treitz韌帶,觸摸清楚腸系膜上動脈,結紮空腸動脈第一支和第二支,在Treitz韌帶下10cm處切斷空腸,近端關閉,遠端備與胰腺做套入式吻合。最後處理胰腺鉤突,主要注意此處有多條小靜脈匯入到腸系膜上靜脈,必須仔細逐一結紮後切斷,以免損傷腸系膜上靜脈,發生大出血。應將胰頭鉤突全部切除,同時廓清腸系膜上動靜脈周圍的淋巴結。
D.重建消化道:主要有以胰腸、膽腸和胃腸吻合順序的Child法和以膽腸、胰腸及胃腸吻合的Whipple法。目前較流行的是Child法,其胰腸吻合採用胰腺與空腸端端嵌入吻合法,均行全層加漿肌層縫合。有時胰腺斷面較空腸腔寬厚,為防止硬性套入造成腸壁血液循環障礙,影響吻合口癒合,須將胰腺上、下緣楔行切除或只做下緣楔行切除,以將胰腺楔行套入。常規方法行膽腸吻合,仍然需要放置T形管,其尺寸應大小適宜;不能太大,也不能太小。還有人用放置導尿管來起支撐作用。最後行胃空腸吻合,一般距胰腸吻合口下40~50cm,於結腸前胃斷端與空腸吻合。如需腸內營養,還需腸造瘺,其營養管應送入吻合口下輸出段空腸內,胃管也要深入到輸入段。Whipple法是將空腸遠側斷端閉合後拉至結腸後先行膽腸吻合。胰腸吻合則分兩種:一種是胰管空腸端側吻合,適用於胰管明顯粗大擴張者;另一種是胰管空腸內移植法,此法需將胰腺管內插入一矽膠管與胰腺管固定。不管Child法還是Whipple法,為防止胰瘺的發生,主張均在主胰腺管內放置導管引流胰液。
技術改良
A.保留幽門的胰頭十二指腸切除術:由於標準的胰頭十二指腸切除術常有體重丟失和營養障礙,許多外科醫師尋求對其改良,保留幽門的胰頭十二指腸切除術就是如此。該術式保留了胃貯存和消化功能,促進消化,預防傾倒綜合徵,有利於改善手術後的營養。雖然手術的程度減輕了,但並沒有降低手術後的存活率,並適應於近來對手術後生存質量提高的要求,所以自20世紀70年代以來得到了一定的推廣。然而人們最關注的是這一改良是否影響惡性腫瘤的根治程度和遠期生存率。對於手術後病人的營養狀態和根治程度與標準的胰十二指腸切除術相比較,雖然有不少的文獻報導,但迄今仍然無令人信服的資料來對此問題做出結論。因為有一個關鍵問題是不能隨機地選擇病人來做這兩種手術,常常是根據病人的具體情況決定術式。一般認為胰頭周圍的良性病變、壺腹癌、惡性程度較低的胰頭部腫瘤、癌腫尚未浸潤幽門及十二指腸等,可採用此術式。惡性病變需要切斷胃右動脈以利於淋巴結廓清,可能對胃幽門及十二指腸球部的血供有影響,術後有部分病人發生胃排空延遲,故術中應加行胃造瘺,以減輕病人因手術後長時間留置鼻飼管帶來的痛苦。B.擴大的胰頭十二指腸切除術:胰腺癌多為胰管上皮發生的腺癌,淋巴結轉移是胰腺癌轉移的重要途徑。胰腺癌的轉移和擴散除淋巴結轉移和癌向周圍組織浸潤外,沿神經束擴散是胰腺癌轉移的另一種方式,因此,所謂擴大的根治切除術除廓清淋巴結外,還應廓清腹腔動脈、腸系膜上動脈及腹主動脈旁的神經叢。腸系膜上周圍神經叢完全切除可導致頑固性腹瀉。此外還需切除胰腺周圍的軟組織,所以全部的手術包括切除門靜脈、肝動脈和腸系膜上動脈在內的全部或大部胰腺及其周圍軟組織和淋巴結、肝門以下膽道、十二指腸、部分空腸、胃和整塊橫結腸系膜。由於擴大手術早期併發症發生率高,手術死亡率高,遠期生存率不理想,故在歐美及我國並沒有得到廣泛套用,即使在多數學者主張此擴大手術的日本,仍有不少學者對此持有異議。
術後防治
胰瘺
常是胰腺切除術後致命和最常見的併發症。多發生於術後5~7天。病人出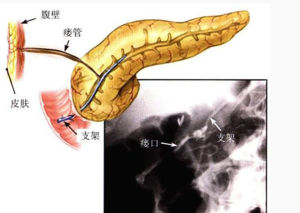 胰十二指腸切除術
胰十二指腸切除術現腹脹、腹痛、高熱,腹腔引流液增加,如腹腔引流液澱粉酶升高,可確定為胰瘺。一般採用非手術療法,因手術難以修復。不同的消化道重建方法對預防胰瘺的發生有重要意義。中國醫科大學附屬醫院總結胰頭十二指腸切除術118例,採用Whipple法的42例中10例發生胰瘺,其中6例死亡;而採用Child法75例中2例發生胰瘺,1例死亡。Child法胰瘺發生率明顯低於Whipple法。目前國內較少採用Whipple法重建消化道。手術中注意胰腸吻合的嚴密,特別是主胰管內導管的放置及引流,腹腔引流要充分,最好採用潘式引流管,必要時加雙腔引流管引流。早期持續套用抑制胰液分泌的藥物,如生長抑素及其衍生物。
腹腔出血
分原發性和繼發性兩種。原發性出血常在手術早期,多為鮮血自引流管流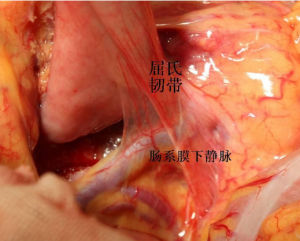 胰十二指腸切除術
胰十二指腸切除術胃腸道出血
術後早期出血可考慮胃黏膜下止血不徹底或凝血功能障礙。術後1周左右出血多認為是應激性潰瘍出血,可按應激性潰瘍出血處理,手術後早期常規套用抗酸藥。腹腔內感染
是一種嚴重併發症,多由胰瘺、膽瘺或腹腔滲血合併感染所致。可有腹痛高熱,身體消耗,發生貧血、低蛋白血症等。加強全身支持治療,套用高效廣譜抗生素。膽瘺
較少發生,一旦發生主要靠通暢引流,一般可以治癒,引流不暢及有腹膜刺激征者應手術探查。手術步驟
切口
上腹正中切口或右上腹正中旁切口,便於上、下、延伸,顯露充分。探查
探查的目的主要是了解病變性質,以決定是否需要切除;了解周圍組織情況,以決定是否能夠切除。⑴決定病變性質:進入腹腔後,需檢查以下情況,以決定病變的性質。
膽囊大小:肝內梗阻或膽石病時,膽囊不大或中等大小,膽石病還可觸到結石,而胰頭癌則膽囊明顯腫大,且不能排空。
胰頭部腫塊:胰頭癌及壺腹周圍癌的腫塊均在十二指腸降部內側,前者一般較大、很硬,在胰頭內,而後者較小、較軟,在十二指腸腔內。慢性胰腺炎時,胰腺呈瀰漫性腫硬,質地較癌腫相對為軟。
x線造影:對於難區別的膽石病,可行術中膽道x線造影診斷,或行術中b超探查鑑別。
活組織檢查:當確診不能鑑別病變性質時,可考慮行胰頭部腫塊活組織檢查。先切開
 胰十二指腸切除術
胰十二指腸切除術為了減少活組織檢查引起出血和增加癌細胞擴散的危險,也可使用肝穿刺針取胰頭部硬塊活組織作切片檢查但準確性較差。
切開十二指腸檢查:可鑑別胰頭癌或壺腹周圍癌和十二指腸良性腫瘤,但此操作有一定危險性,且易使腫瘤擴散或腸內細菌播入腹腔,在非特殊必要時應儘量避免。
⑵決定能否切除:能否行根治性切除,需檢查以下各種情況後才能決定。
癌的局部情況:檢查癌腫本身是否越出腺體和侵及門靜脈、腸系膜上動靜脈、腹主動脈、下腔靜脈等重要血管。如被侵及,則不能進行根治性手術。
檢查方法可分3步進行:
第1步探查外側:切開十二指腸外側的後腹膜,將十二指腸及胰頭部向內翻轉,用左手示指探查胰頭部背側及主動脈和下腔靜脈腹側的間隙,如容易將手指伸入此間隙,說明癌腫尚局限於胰內[圖3⑴]。如不能分開伸入,則說明癌已侵及主動脈或下腔靜脈。
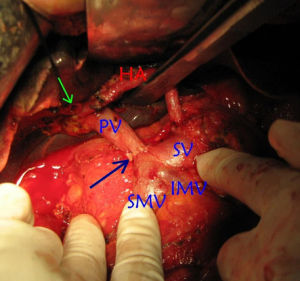
第2步探查下側:將胃、橫結腸及大網膜提向上方,顯露橫結腸系膜,在儘量遠離十二指腸懸韌帶處切開,顯露腸系膜上動脈靜脈、結腸中動脈和胰十二指腸下動脈。用右手示指伸入胰腺背側,由內側向外側將胰腺與腸系膜上動、靜脈分開[圖3⑵]。如已固定,說明腫瘤已侵及血管,勿再勉強分離,以防大出血。此步驟也可經切開胃結腸韌帶,在胰頸部下緣切開後腹膜,在腸系膜上靜脈和門靜脈前,胰頸後之間用手指探測胰塊與門脈的關係。
第3步探查上側:將膽總管和胃小彎中點之間的胃十二指腸韌帶切開,顯露肝動脈,結紮、切斷胃右動脈,將左手示指伸入胰腺上緣的背側,沿門靜脈腹側向下分離[圖3⑶]。如腫瘤未侵及重要血管,此手指可與下側伸上的右手示指相遇;否則表示腫瘤已侵及重要血管。
經仔細探查,如判斷腫瘤不能切除,應即終止手術。
切除
如經仔細探查,判斷腫瘤能夠切除,即可將胰頭部、胃竇部分,十二指腸全部、空腸一部分和膽總管一併切除。⑴充分分離準備切除的臟器:將探查時的胰頭上、下、外側3處作的後腹膜切口連線,充分顯露準備切除的臟器。
分離外側:分離橫結腸肝曲,並向內下推移,直至胰腺頸體連線部,再將十二指腸降部和胰頭向內側分離至下腔靜脈及主動脈附近。繼續將大網膜沿胃下緣切斷,進一步顯露腸系膜上動、靜脈,並將分出的胰十二指腸下動、靜脈的胰頭小分支結紮、切斷,並清除腸系膜根部淋巴結。然後,將十二指腸橫部向上翻起,顯出其後方的主動脈和下腔靜脈,並清除胰頭後及主動脈周圍淋巴結。
分離上側:結紮切斷胃十二指腸動脈及幽門上區的各小血管分支、並清除肝十二指腸韌帶內及幽門上淋巴結,顯露膽總管下段及膽囊管。將膽總管向上外側拉開,用手指進一步分離胰頭後部與門靜脈之間的疏鬆組織。邊分離邊將胰頭向下牽拉,顯露門靜脈下段的脾靜脈與腸系膜上靜脈分支,充分分離出準備切除的臟器。
⑵切斷膽總管:在十二指腸上緣切斷膽總管,遠端暫時鉗夾或結紮,近端用止血鉗鉗夾,備以後吻合用。此時進一步清除肝總動脈乾、胃左動脈乾及腹腔動脈周圍淋巴結。
⑶切斷胃:為了便於徹底切除胰頭和防止術後吻合口潰瘍,需將胃竇部切除。切斷處兩端均以直鉗夾緊,遠端隨胰頭癌一併切除,近端留待修復時吻合用。還可根據具體情況採用選擇性迷走神經切斷術,以防止吻合口潰瘍。
⑷切斷胰體:以左手示、中指伸入胰腺後壁作為支持固定,再用拇指仔細檢查胰頭癌大小範圍,在距腫瘤最少3cm處橫斷胰體。切斷前在切線兩側上、下緣各縫扎一針,以防切斷後出血。切斷後,頭端用粗絲線扎牢固定,體端以中號絲線間斷褥式縫合止血,備以後吻合用。胰管最好找出,如較粗,應多留0.3cm,在中間剪開向上、下外翻後縫合固定於胰腺組織上;如較細,可不予處理。胰腺切斷後沿胰體上緣向左繼續清除脾動脈乾及脾門淋巴結。
⑸切斷空腸:在十二指腸懸韌帶遠端6~8cm處切斷空腸,近端鉗夾或結紮,向上推過橫結腸系膜裂孔,準備切除,遠端暫用直止血鉗夾住,備吻合用。
⑹分離胰頭鉤突:將切斷的胰腺頭端外翻,仔細將其後壁與門靜脈和腸系膜上靜脈相聯繫的小血管一一結紮、切斷,將鉤突顯露。用左手示指放在胰頭和下腔靜脈之間,拇指在前,分離結締組織。分離出鉤突後即可將需要切除的臟器整塊切除,仔細止血。
消化道重建
切除後,胃腸道4個殘端需要作胰空腸吻合、膽總管空腸吻合和胃空腸吻合等手術修復[圖5]。⑴胰空腸吻合:胰頭部癌根治術的重要環節是將胰管再植入腸道。胰腺殘端的胰管與
 胰十二指腸切除術
胰十二指腸切除術行端端吻合時,先將空腸遠端經橫結腸系膜切口向上提出,在距空腸斷端1cm處,將空腸後壁漿肌層與胰腺距其殘端1cm處,將空腸後壁漿肌層與胰腺距其殘端1cm處的後壁包膜用1-0號絲線間斷縫合固定,再將腸壁全層與胰腺組織間斷縫合一圈。最後,將空腸前壁漿肌層與胰前壁包膜行間斷縫合,使胰腺套入空腸1cm左右即可。
⑵膽總管空腸吻合:因膽總管多已擴張,採取端側吻合,縫合操作不難。在距空腸斷端5~10cm處選定吻合部位,切除膽總管殘端鉗夾過的部分,用1-0號絲線先間斷縫合空腸後壁與膽總管殘端後壁的漿肌層,切開空腸,全層間斷內翻縫合吻合口一圈。最後,間斷縫合吻合口前壁漿肌層。單層間斷縫合,效果亦很滿意。
⑶胃空腸吻合:在距膽總管吻合口以遠約20cm處作結腸前空腸近端對胃小彎的胃空腸吻合。先將胃斷端與空腸行端側吻合(操作方法按畢羅Ⅱ式全口吻合)。最後,將結腸系膜裂孔閉合。