基本內容
化學
中文名稱:乙胺丁醇
中文別名:[2R,2[S-(R*,R*)]-R]-(+)2,2’-(1,2-乙二基二亞氨基)-雙-1-丁醇;
英文名稱:ethambutol
英文別名:(+)-2,2-ethylenediiminodibutan-1-ol; 2,2'-(ethane-1,2-diyldiimino)dibutan-1-ol; (2R,2'R)-2,
CAS號:74-55-5
EINECS號:200-810-6
分子式:C10H24N2O2
分子量:204.3098
InChI:InChI=1/C10H24N2O2/c1-3-9(7-13)11-5-6-12-10(4-2)8-14/h9-14H,3-8H2,1-2H3/t9-,10-/m1/s1
密度:0.987g/cm3
沸點:345.3°C at 760 mmHg
閃點:113.7°C
蒸汽壓:3.9E-06mmHg at 25°C
藥物
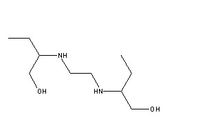 乙胺丁醇分子式
乙胺丁醇分子式藥物名稱: 乙胺丁醇
藥物別名: 暫無
英文名稱: Ethambutol
藥物說明: 片劑:每片0.25g。
主要成分:[2R,2[S-(R*, R*)]-R]-(+)2,2′-(1,2-乙二基二亞氨基)-雙-1-丁醇二鹽酸鹽
分子式: C10H24N2O2·2HCl
分子量:277.23
性狀特徵: 白色粉末
作用
藥理
本品為合成抑菌抗結核藥。其作用機理尚未完全闡明。本品可滲入分技桿菌體內干擾RNA的合成從而抑制細菌的繁殖,本品只對生長繁殖期的分技桿菌有效。
動力學
 鹽酸乙胺丁醇片
鹽酸乙胺丁醇片口服後經胃腸道的吸收75~80%。
廣泛分布於全身各組織和體液中(除腦脊液外)。紅細胞內藥濃度與血漿濃度相等或為其2倍,並可持續24小時;腎、肺、唾液和尿液內的藥濃度都很高;但胸水和腹水中的濃度則很低。本品不能滲入正常腦膜,但結核性腦膜炎患者腦脊液中可有微量。其分布容積為1.6L/kg。蛋白結合率約10~30%。口服2~4小時血藥濃度可達峰值,T1/2為3~4小時,腎功能減退者可延長至8小時。主要經肝臟代謝,約15%的給藥量代謝成為無活性代謝物。經腎小球濾過和腎小管分泌排出:給藥後約80%在24小時內排出,至少50%以原形排泄,約15%為無活性代謝物。在糞便中以原形排出約20%。在乳汁中的藥濃度約相當於母血藥濃度。相當量的乙胺丁醇可經血液透析和腹膜透析從體內清除。
功能主治
對結核桿菌和其他分支桿菌有較強的抑制作用。口服吸收約80%,血藥濃度達峰時間2~4小時,蛋白結契約40%,在體內僅有10%左右的藥物代謝成為非活性物。主要經腎排泄。與其他抗結核藥間無交叉耐藥性。但結核桿菌對本品也可緩慢產生耐藥性。 為二線抗結核藥,可用於經其他抗結核藥治療無效的病例,常與其他抗結核藥聯合套用。以增強療效並延緩細菌耐藥性的產生。對細胞內結核無效用法用量
1.成人常用量與其他抗結核藥合用,結核初治,按體重15mg/kg,每日一次頓服;結核復治,按體重25mg/kg每日一次頓服,連續60天,繼以按體重15mg/kg,每日一次頓服。非典型分技桿菌感染,每日15—25mg/kg,一次頓服,與其他抗結核藥合用。2,小兒常用量13歲以下不宜套用本品;13歲以上兒童用量與成人相同。如發生胃腸道刺激,乙胺丁醇可與食物同服。一日劑量分次服用可能達不到有效血藥濃度,因此本品宜一次頓服。乙胺丁醇單用時細菌可迅速產生耐藥性,因此本品必須與其他抗結核藥聯合套用。本品用於曾接受抗結核藥的患者時,應至少與一種二線藥物合用,例如乙硫異煙胺或環絲氨酸等。治療必須持續1一2年,有時甚至數年或無限期用藥。此外,乙胺丁醇與異煙肼聯合間歇療法曾獲滿意療效,劑量為按體重用乙胺丁醇50mg/kg與異煙肼15mg/kg,每周給藥2次。肝或腎功能減退的患者,本品血藥濃度可能增高,半衰期延長。有腎功能減退的患者套用本品時需減量。
使用須知
不良反應
 乙胺丁醇片
乙胺丁醇片(1)發生率較多者為視力模糊
、眼痛、紅綠色盲或任何視力減退(視神經炎:每日按體重劑量25mg/kg以上時易發生)。(2)發生率較少者為畏寒、關節腫痛(尤其大趾、髁、膝關節)、病變關節表麵皮膚發熱拉緊感(急性痛風、高尿酸血症)。(3)發生率極少者為麻木,針刺感、燒灼痛或手足軟弱無力(周圍神經炎)。可引起胃腸道反應:噁心,嘔吐,食欲不振,腹脹,腹瀉.個別病例有抑鬱、頭痛、皮疹、脫髮、關節痛、痤瘡,轉氨酶升高、肝損害、下肢發麻、關節痛及幻覺、不安、失眠等精神症狀.劑量過大,體位性低血壓、高尿酸血症、剝脫性皮炎、視物模糊、抽搐、甚至出現失明。
藥物禁忌
(1)乙胺丁醇可透過胎盤,胎兒血藥濃度約為母親血藥濃度的30%。本品在小鼠實驗中高劑量可引起膀裂、腦外露和脊柱畸形等;大鼠中本品高劑量可引致輕度頸椎畸形;在家兔中本品高劑量可引起獨眼畸形、短肢、兔唇和齶裂等畸形。雖然在人類中未證實有問題,孕婦套用仍須充分權衡利弊。本品和其他藥物合用時對胎兒的影響尚未闡明。(2)乙胺丁醇可分泌至乳汁,濃度與血藥濃度相近,雖然在人類中未證實有問題,哺乳期婦女用藥須權衡利弊。(3)下列情況應慎用:痛風、視神經炎、腎功能減退。(4)13歲以下兒童尚缺乏臨床資料,老年人往往伴有生理性腎功能減退,故應按腎功能調整用量。乙醇中毒者、乳幼兒禁用本品。糖尿病患者必須在控制糖尿病的基礎上方可使用本品。已發生糖尿病性眼底病變者慎用本品,以防眼底病變加重。
注意事項
1、視覺神經炎。主要在套用劑量較大的病人中出現,可以有視物模糊,視物時出現中心盲點,視野(視物範圍)縮小等。
2、胃腸道不適,食慾減退,肝功能出現異常,有的還可以有過敏性皮炎及肌肉酸痛和關節疼痛。
3、有時會影響腎臟功能,對於孕婦、嬰幼兒及有癲癇的病人要謹慎使用,用前最好作有關檢查,用時要嚴密觀察副反應的出現,對於嚴重的副反應,應該在醫師的指導下及時停藥。
相互作用
(1)與乙硫異煙胺合用可增加副作用。(2)與氫氧化鋁同用能降低乙胺丁醇的吸收。(3)與神經毒性藥物合用可增加本品神經毒性,如視神經炎或周圍神經炎。
其它相關
鹽酸膠囊
英文名EthambutolHydrochlorideCapsules
 鹽酸乙胺丁醇膠囊
鹽酸乙胺丁醇膠囊類別西醫藥物
藥理作用
1.藥理本品為人工合成抑菌性抗結核藥。對生長繁殖期細菌具較強活性,對靜止期細菌幾無作用。對各型分枝桿菌具高度抗菌活性。結核桿菌對本品與其他藥物之間無交叉耐藥現象。本品的作用機制尚未完全闡明,可能與抑制敏感細菌的代謝,抑制RNA的合成,干擾結核桿菌蛋白代謝,從而導致細菌死亡。2.毒理本品大劑量時在小鼠試驗中可引致齶裂、腦外露和脊柱畸形等;在大鼠試驗中可引致輕度頸椎畸形;在家兔試驗中可引致獨眼、短肢和齶裂等。本品為膠囊劑。
動力學
本品口服後經胃腸道吸收75%~80%,達峰時間2~4小時。在體內各組織中分布廣泛,可濃集在紅細胞(紅細胞內濃度可達血藥濃度的2~3倍)、腎、肺、唾液和尿液中,在胸水、腹水濃度極低。腦脊液中藥物濃度約為血藥濃度20%~80%,表觀分布容積(Vd)為1.6~3.9L/kg,蛋白結合率約10%~30%。血消除半衰期(T1/2a)為2.5~4小時,腎功能減退者可延長至7~15小時,故應進行劑量調整。約10%~20%的本品在肝臟代謝,本品經腎小球濾過和腎小管分泌排出,給藥後約50%~90%藥物以原型在24小時內經腎排出,約15%為無活性代謝物,腎清除率(ClR)為5.93~8.45ml/分/kg。在糞便中以原形排出約20%。乳汁中的藥物濃度約相當於母體血藥濃度。血液透析和腹膜透析可清除本品。
適應症
本品適用於與其他抗結核藥聯合治療結核分枝桿菌所致的肺結核和肺外結核,亦可用於非典型結核分枝桿菌感染的治療。
用法用量
需與其他抗結核藥物聯合使用。1.初治:口服,按體重15mg/kg,一日1次;或一次25~30mg/kg,最高2.5g,一周3次;或按體重50mg/kg,最高2.5g一周2次。2.復治:口服,按體重25mg/kg,一日1次,連續60天后,繼以按體重15mg/kg,一日1次。3.非典型結核分枝桿菌感染:按體重15~25mg/kg,一日1次。
不良反應
1.常見視神經損害,如球後視神經炎、視神經中心纖維損害。可能與本品同銅、鋅等金屬元素螯合後引起這些金屬元素含量下降有關。球後視神經炎發生率約0.8%,與劑量、療程有關,長期服藥、每日劑量大於25mg/kg時易於發生,每日劑量15mg/kg發生率為1%,25mg/kg為6%,35mg/kg增至15%。表現為視力模糊、眼痛、紅綠色盲或視力減退、視野縮小。上述反應早期發現和及時停藥則可於數周或數月內自行消失,永久性視覺功能喪失極少發生。2.少見畏寒、關節腫痛(尤其大趾、髁、膝關節)和病變關節表麵皮膚發熱拉緊感(急性痛風、高尿酸血症)。3.偶見胃腸道不適、噁心、嘔吐、腹瀉、肝功能損害、周圍神經炎(常表現為麻木、針刺感、燒灼痛或手足軟弱無力)和過敏反應(常表現為皮疹、瘙癢、頭痛、發熱、關節痛)等。
禁忌
對本品過敏者、已知視神經炎患者、乙醇中毒者、及年齡<13歲者應謹慎使用。
注意事項
1.痛風、視神經炎、糖尿病眼底病變、肝、腎功能減退患者慎用。腎功能減退的患者應減量。2.單用本品細菌可迅速產生耐藥性,因此必須與其他抗結核藥聯合套用。3.治療期間應檢查:(1)眼部,視野、視力、紅綠鑑別力等,在用藥前、療程中每月檢查一次,尤其是療程長、每日劑量超過15mg/kg的患者。(2)由於本品可使血中尿酸濃度增高,引起痛風發作,因此在療程中應定期測定血清尿酸。4.對診斷的干擾:服用本品可使血尿酸濃度測定值增高。5.如發生胃腸道刺激,本品可與食物同服。一日劑量分次服用可能達不到有效血藥濃度,因此本品一日劑量宜1次服用。13歲以下兒童尚缺乏臨床資料,由於在幼兒中不易監測視力變化,故本品不宜用於13歲以下小兒;13歲以上小兒用量與成人相同。1.由於本品可透過胎盤,胎兒血藥濃度約為母體血藥濃度的30%,動物實驗顯示本品可致畸形,雖然在人類中未證實有問題,但孕婦仍應禁用本品,如確有服用指征時須充分權衡利弊。2.本品可分泌至乳汁,濃度與母體血藥濃度相近,故哺乳期婦女禁用本品,如確有服用指征需暫停授乳。老年患者因生理性腎功能減退,故應按腎功能調整用量。
過量處理1.藥物過量主要表現為中所述症狀,重症者可發生永久性視神經萎縮。2.藥物過量的處理:(1)停藥。(2)對症處理:①球後視神經炎者可用維生素B6、複合維生素及鋅銅製劑等。②恢復視力,可選用地塞米松5mg,每日靜滴或球後注射;妥拉蘇林12.5mg,每日球後注射;氫化可的松200mg,每日靜滴。也可口服強的松20mg,每日2~3次。同時給予維生素等。恢復期可予針刺治療,口服地巴唑、煙酸等,或胎盤組織液每日肌內注射。③必要時進行血液透析和腹膜透析。
相互作用
1.鋁鹽,包括DDI緩衝液可減少本品的吸收。2.本品與維拉帕米合用可減少後者的吸收。3.與神經毒性藥物合用可增加本品的神經毒性,如視神經炎或周圍神經炎。4.與乙硫異煙胺合用可增加黃疸性肝炎、視神經炎等不良反應。
鹽酸片
 鹽酸乙胺丁醇片
鹽酸乙胺丁醇片類別西醫藥物
藥理作用
本品為合成抑菌抗結核藥。其作用機理尚未完全闡明。本品可滲入分枝桿菌體內干擾RNA的合成,從而抑制細菌的繁殖,本品只對生長繁殖期的分枝桿菌有效。迄今未發現本品與其他抗結核藥物有交叉耐藥性。本品為白色片。
動力學
口服後經胃腸道吸收75%~80%。廣泛分布於全身組織和體液中(除腦脊液外)。紅細胞內藥濃度與血漿濃度相等或為其2倍,並可持續24小時;腎、肺、唾液和尿內的藥濃度較高;但胸水和腹水中的濃度則較低。蛋白結合率約為20%~30%。口服2~4小時血藥濃度可達峰值,半衰期(T1/2)為3~4小時,腎功能減退者可延長至8小時。主要經肝臟代謝,約15%的給藥量代謝成為無活性代謝物。經腎小球濾過和腎小管分泌排出;給藥後約80%在24小時內排出,至少50%以原形排泄,約15%為無活性代謝物。在糞便中以原形排出約20%。乳汁中的藥濃度約相當於母血藥濃度。相當量的乙胺丁醇可經血液透析和腹膜透析從體內清除。
適應症
適用於與其他抗結核藥聯合治療結核桿菌所致的肺結核。亦可用於結核性腦膜炎及非典型分枝桿菌感染的治療。
用法用量
1.成人常用量與其他抗結核藥合用,結核初治,按體重15mg/kg,每日一次頓服;或每次口服25~30mg/kg,最高2.5g,每周3次;或50mg/kg,最高2.5g,每周2次。結核復治,按體重25mg/kg,每日一次頓服,連續60天,繼以按體重15mg/kg,每日一次頓服。非典型分枝桿菌感染,每日15~25mg/kg,一次頓服;2.小兒常用量13歲以下不宜套用本品;13歲以上兒童用量與成人相同。
不良反應
1.發生率較多者為視力模糊、眼痛、紅綠色盲或視力減退、視野縮小(視神經炎每日按體重劑量25mg/kg以上時易發生)。視力變化可為單側或雙側;2.發生率較少者為畏寒、關節腫痛(尤其大趾、髁、膝關節)、病變關節表麵皮膚發熱拉緊感(急性痛風、高尿酸血症);3.發生率極少者為皮疹、發熱、關節痛等過敏反應;或麻木,針刺感、燒灼痛或手足軟弱無力(周圍神經炎)。
注意事項
1.對診斷的干擾:服用本品可使血尿酸濃度測定值增高;2.下列情況應慎用:痛風、視神經炎、腎功能減退;3.治療期間應檢查:眼部,視野、視力、紅綠鑑別力等,在用藥前、療程中每日檢查一次,尤其是療程長,每日劑量超過15mg/kg的患者;血清尿酸測定,由於本品可使血清尿酸濃度增高,引起痛風發作。因此在療程中應定期測定;4.如發生胃腸道刺激,乙胺丁醇可與食物同服。一日劑量分次服用可能達不到有效血藥濃度,因此本品一日劑量宜一次頓服;5.乙胺丁醇單用時細菌可迅速產生耐藥性,因此必須與其他抗結核藥聯合套用。本品用於曾接受抗結核藥的患者時,應至少與一種以上藥物合用;6.鑒於2013年尚無切實可行的測定血藥濃度方法,劑量應根據患者體重計算。肝或腎功能減退的患者,本品血藥濃度可能增高,半衰期延長。有腎功能減退的患者套用時需減量。13歲以下兒童尚缺乏臨床資料。由於在幼兒中不易監測視力變化,故本品不推薦用於13歲以下兒童。1.乙胺丁醇可透過胎盤,胎兒血藥濃度約為母親血藥濃度的30%。本品在小鼠實驗中高劑量可引起齶裂、腦外露和脊柱畸形等;2.乙胺丁醇可分布至乳汁,濃度與血藥濃度相近,雖然在人類中未證實有問題,哺乳期婦女用藥須權衡利弊。老年人往往伴有生理性腎功能減退,故應按腎功能調整用量。
相互作用
1.與乙硫異煙胺合用可增加不良反應;2.與氫氧化鋁同用能減少本品的吸收;3.與神經毒性藥物合用可增加本品神經毒性,如視神經炎或周圍神經炎。
生產企業
麗珠醫藥集團股份有限公司、北京賽科藥業有限責任公司、廣東台城製藥有限公司、安徽豐原藥業股份有限公司、湖南張家界製藥廠、河南省新鄉同心製藥廠、西北合成藥廠、廣東江門環宇製藥有限公司、東北製藥總廠、廣東南國藥業有限公司、新疆華世丹藥業有限公司、合肥製藥廠、江西製藥有限責任公司、江蘇黃河藥業股份有限公司、江蘇省黃海藥業有限公司、甘肅省祁連山製藥廠、新疆優德製藥有限公司、陝西菊製藥有限責任公司、陝西省醫藥工業研究所、陝西大華製藥廠、西南藥業股份有限公司、四川合成製藥股份有限公司、重慶迪康長江製藥有限公司、貴州六枝大華集團製藥有限公司、廣東省中山市沙溪製藥廠、成都藥業有限責任公司、成都天台山製藥有限公司、成都錦華製藥廠、四川樂山製藥廠、廣州藥業公司廣州明興製藥廠、海南省金島製藥廠、麗珠集團利民製藥廠、麗珠集團利民製藥廠、廣州軍區君山製藥廠、河南省安陽市華安製藥廠、河南省南陽普康藥業集團公司、河南華利製藥廠、武漢中聯集團四藥藥業有限公司、美爾雅(集團)美升藥業有限公司、威海華新藥業有限公司、安徽三發製藥有限公司、安徽省蚌埠海洋製藥廠、安慶市海宜製藥廠、安徽仁濟堂藥業有限公司、江蘇太倉製藥廠、常州康普藥業有限公司、江蘇帝益藥業有限公司、鎮江市第三製藥廠、連雲港恆瑞製藥有限公司、上海五洲藥業股份有限公司、南京白敬宇製藥廠、上海赫司特五州製藥有限公司、鹽城生物化學製藥廠、無錫艾西恩製藥有限公司、吉林製藥股份有限公司、吉林集安華星製藥廠、黑龍江省佳木斯晨星藥業有限責任公司、鞍山第二製藥廠、朝陽製藥廠、東北製藥集團瀋陽紅旗製藥廠、瀋陽故宮製藥廠、內蒙古吉蘭泰鹽化集團、太原衛星製藥廠、大同市利群製藥廠、大同市星火製藥廠、大同衛華製藥廠、山西省大同第二製藥廠、大同市光明製藥廠、山西泰盛製藥有限公司、大同市光華製藥廠、天津市康誼藥業有限公司、天津市華新製藥廠、石家莊市第五製藥廠
物質毒性
| 編號 | 毒性類型 | 測試方法 | 測試對象 | 使用劑量 | 毒性作用 |
|---|---|---|---|---|---|
| 1 | 急性毒性 | 口服 | 成年男性 | 332 mg/kg/31D-I | 1.肺部、胸部或者呼吸毒性——肺間質纖維化、肺病(包括塵肺) 2.血液毒性——嗜酸性粒細胞增多 3.營養和代謝系統毒性——體溫升高 |
| 2 | 急性毒性 | 口服 | 人類 | 1410 mg/kg/11W-I | 1.眼毒性——視野發生變化 |
| 3 | 急性毒性 | 口服 | 成年女性 | 900 mg/kg/60D-I | 1.肝毒性——黃疸,膽汁淤積 |
| 4 | 急性毒性 | 口服 | 成年男性 | 600 mg/kg | 1.周圍神經毒性——神經或神經鞘結構發生變化 2.行為毒性——運動行為發生變化(具體情況具體分析) 3.腎、輸尿管和膀胱毒性——尿中成分發生變化 |
| 5 | 急性毒性 | 口服 | 成年男性 | 1200 mg/kg | 1.皮膚和附屬檔案毒性——皮炎 (全身暴露後) 2.免疫系統毒性——過敏性休克 |
| 6 | 急性毒性 | 口服 | 大鼠 | 998 mg/kg | 詳細作用沒有報告除致死劑量以外的其他值 |
| 7 | 急性毒性 | 口服 | 小鼠 | 8700 mg/kg | 1.行為毒性——驚厥或癲癇發作閾值受到影響 |
| 8 | 急性毒性 | 腹腔注射 | 小鼠 | 1075 mg/kg | 1.行為毒性——驚厥或癲癇發作閾值受到影響 |
| 9 | 急性毒性 | 靜脈注射 | 小鼠 | 240 mg/kg | 1.行為毒性——驚厥或癲癇發作閾值受到影響 |
| 10 | 急性毒性 | 皮下注射 | 哺乳動物 | 890 mg/kg | 1.肺部、胸部或者呼吸毒性——其他變化 |
| 11 | 急性毒性 | 靜脈注射 | 哺乳動物 | 350 mg/kg | 1.肺部、胸部或者呼吸毒性——其他變化 |
| 12 | 慢性毒性 | 口服 | 狗 | 52920 mg/kg/12W-I | 1.眼毒性——未報告 |

