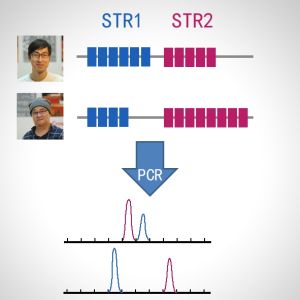
檢測
1.限制性片段長度多態性(RestrictionFragmentLengthPolymorphism):由DNA的多態性,致使DNA分子的限制酶切位點及數目發生改變,現在多採用PCR-RFLP法進行研究基因的限制性片段長度多態性。2.單鏈構象多態性(SSCP):是一種基於單鏈DNA構象差別的點突變檢測方法。相同長度的單鏈DNA如果順序不同,甚至單個鹼基不同,就會形成不同的構象。在電泳時泳動的速度不同。將PCR產物經變性後,進行單鏈DNA凝膠電泳時,靶DNA中若發生單個鹼基替換等改變時,就會出現泳動變位(mobilityshift),多用於鑑定是否存在突變及診斷未知突變。
3.PCR-ASO探針法(PCR-allelespecificoligonucleotide,ASO):即等位基因特異性寡核苷酸探針法。在PCR擴增DNA片段後,直接與相應的寡核苷酸探雜交,即可明確診斷是否有突變及突變是純合子還是雜合子。
其原理是:用PCR擴增後,產物進行斑點雜交或狹縫雜交,針對每種突變分別合成一對寡核苷酸片段作為探針,其中一個具有正常序列,另一個則具有突變鹼基。突變鹼基及對應的正常鹼基勻位於寡核苷酸片段的中央,嚴格控制雜交及洗脫條件,使只有與探針序列完全互補的等位基因片段才顯示雜交信號,而與探針中央鹼基不同的等位基因片段不顯示雜交信號,如果正常和突變探針都可雜交,說明突變基因是雜合子,如只有突變探針可以雜交,說明突變基因為純合子,若不能與含有突變序列的寡核苷探針雜交,但能與相應的正常的寡核苷探針雜交,則表示受檢者不存在這種突變基因。若與已知的突變基因的寡核苷探針勻不能雜交,提示可能為一種新的突變類型。
4.PCR-SSO法:SSO技術即是順序特異寡核苷酸法(SequenceSpecificOligonucleotide,SSO)。
原理是PCR基因片段擴增後利用序列特異性寡核苷酸探針,通過雜交的方法進行擴增片段的分析鑑定。探針與PCR產物在一定條件下雜交具有高度的特異性,嚴格遵循鹼基互補的原則。
探針可用放射性同位素標記,通過放射自顯影的方法檢測,也可以用非放射性標記如地高辛、生物素、過氧化物酶等進行相應的標記物檢測。
5.PCR-SSP法:序列特異性引物分析即根據各等位基因的核苷酸序列,設計出一套針對每一等位基因特異性的(allele-specific)、或組特異性(group-specific)的引物,此即為序列特異性引物(SSP)。SSP只能與某一等位基因特異性片段的鹼基序列互補性結合,通過PCR特異性地擴增該基因片段,從而達到分析基因多態性的目的。
6.PCR-螢光法:用螢光標記PCR引物的5’端,螢光染料FAM和JOE呈綠色螢光,TAMRA呈紅色螢光,COUM呈蘭色螢光,不同螢光標記的多種引物同時參加反應,PCR擴增待檢測的DNA,合成的產物分別帶有引物5’端的染料,很容易發現目的基因存在與否。
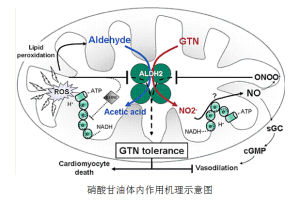 DNA的多態性
DNA的多態性常用方法有:Sanger雙脫氧末端終止法;Maxam-Gilbert化學裂解法;DNA測序的自動化。目前DNA順序全自動雷射測定法是最先進的方法。
8.PCR指紋圖法(PCR-fingerprints):實用於快速的同種異型DR/Dw配型。在DR/DW純合子及雜合子個體中,每種DR單倍型及每種單倍型組合所產生的單鏈環狀結構的大小、數目和位置各異,由於同質雙鏈和異質雙鏈之間的分子構象不同。
因此,在非變性聚丙烯醯胺凝膠電泳時,它們的遷移率各不相同,從而獲得單倍型特異的電泳帶格局即PCR指紋。也有人用人工合成的短寡核苷酸片段作為探針,同經過酶切的人體DNA作Southernblot,可以得出長度不等的雜交帶,雜交帶的數目和分子量的大小具有個體特異性,除非同卵雙生,幾乎沒有兩個人是完全相同的,就象人的指紋一樣,人們把這種雜交帶圖形稱為基因指紋(genefinger-printing)。
9.基因晶片法:又稱為DNA微探針陣列(Microarray)。它是集成了大量的密集排列的大量已知的序列探針,通過與被標記的若干靶核酸序列互補匹配,與晶片特定位點上的探針雜交,利用基因晶片雜交圖象,確定雜交探針的位置,便可根據鹼基互補匹配的原理確定靶基因的序列。這一技術已用於基因多態性的檢測。
對多態性和突變檢測型基因晶片採用多色螢光探針雜交技術可以大大提高晶片的準確性、定量及檢測範圍。套用高密度基因晶片檢測單鹼基多態性,為分析SNPs提供了便捷的方法。
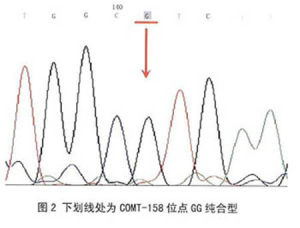 DNA的多態性
DNA的多態性限制性片段用二種酶切割產生,一種是罕見切割酶,一種是常用切割酶。它結合了RFLP和PCR技術特點,具有RFLP技術的可靠性和PCR技術的高效性。
由於AFLP擴增可使某一品種出現特定的DNA譜帶,而在另一品種中可能無此譜帶產生,因此,這種通過引物誘導及DNA擴增後得到的DNA多態性可做為一種分子標記。AFLP可在一次單個反應中檢測到大量的片段。以說AFLP技術是一種新的而且有很大功能的DNA指紋技術。
11.DGGE(denaturinggradinentelectrophoresis,DGGE)法,變性梯度凝膠電泳法DGGE法分析PCR產物,如果突變發生在最先解鏈的DNA區域,檢出率可達100%,檢測片段可達1kb,最適圍為100bp-500bp。
基本原理基於當雙鏈DNA在變性梯度凝膠中進行到與DNA變性濕度一致的凝膠位置時,DNA發生部分解鏈,電泳適移率下降,當解鏈的DNA鏈中有一個鹼基改變時,會在不同的時間發生解鏈,因影響電泳速度變化的程度而被分離。
由於本法是利用溫度和梯度凝膠遷移率來檢測,需要一套專用的電泳裝置,合成的PCR引物最好在5`末端加一段40bp-50bp的GC夾,以利於檢測發生於高熔點區的突變。在DGGE的基礎上,又發展了用濕度梯度代替化學變性劑的TGGE法(溫度梯度凝膠電泳temperaturegradientgelelectrophoresis,TGGE)。DGGE和TGGE均有商品化的電泳裝置,該法一經建立,操作也較簡便,適合於大樣本的檢測篩選。
12.RAPD(RandomamplifiedpolymorphicDNA)法,運用隨機引物擴增尋找多態性DNA片段可作為分子標記。這種方法即為RAPD(RandomamplifiedpolymorphicDNA,隨機擴增的多態性DNA)。儘管RAPD技術誕生的時間很短,但由於其獨特的檢測DNA多態性的方式以及快速、簡便的特點,使這個技術已滲透於基因組研究的各個方面。
該RAPD技術建立於PCR技術基礎上,它是利用一系列(通常數百個)不同的隨機排列鹼基順序的寡聚核苷酸單鏈(通常為10聚體)為引物,對所研究基因組DNA進行PCR擴增.聚丙烯醯胺或瓊脂糖電泳分離,經EB染色或放射性自顯影來檢測擴增產物DNA片段的多態性,這些擴增產物DNA片段的多態性反映了基因組相應區域的DNA多態性。
RAPD所用的一系列引物DNA序列各不相同,但對於任一特異的引物,它同基因組DNA序列有其特異的結合位點.這些特異的結合位點在基因組某些區域內的分布如符合PCR擴增反應的條件,即引物在模板的兩條鏈上有互補位置,且引物3'端相距在一定的長度範圍之內,就可擴增出DNA片段.因此如果基因組在這些區域發生DNA片段插入、缺失或鹼基突變就可能導致這些特定結合位點分布發生相應的變化,而使PCR產物增加、缺少或發生分子量的改變。
通過對PCR產物檢測即可檢出基因組DNA的多態性。分析時可用的引物數很大,雖然對每一個引物而言其檢測基因組DNA多態性的區域是有限的,但是利用一系列引物則可以使檢測區域幾乎覆蓋整個基因組。因此RAPD可以對整個基因組DNA進行多態性檢測。另外,RAPD片段克隆後可作為RFLP的分子標記進行作圖分析。
套用領域
法醫物證學基因診斷
基因治療
物種鑑別
個體鑑別