正文
在工業上用得最多的是過渡金屬氧化物,它們廣泛用於氧化還原型機理的催化反應;主族元素的氧化物多數用於酸鹼型機理的催化反應(見固體酸催化劑),包括氧化、脫氫、加氫、氧化脫氫、氨化氧化、氧氯化等反應(見表)。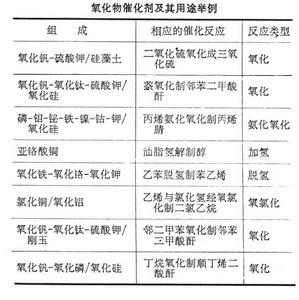 金屬氧化物催化劑
金屬氧化物催化劑過渡金屬氧化物催化劑,一般為非化學計量化合物,存在著負離子或正離子缺位,形成特定的活性中心;分子結構中的某些金屬-氧鍵的強度往往不同於正常化合物,能通過電子轉移的機理而使反應物活化。在金屬氧化物催化的氧化反應中有多種活化的過渡態氧生成,如O娛、O-、O2-,它們表現出不同的反應活性,可分兩種作用機理,即吸附氧作用機理和晶格氧作用機理。前者是藉助因吸附而活化的過渡態氧與被氧化物的作用;後者以氧化物催化劑中的晶格氧與被氧化物發生作用而自身被還原,還原狀態的氧化物催化劑再從催化劑表面氣相中奪取氧而再被氧化,形成催化循環。
從組成上可分為單一氧化物或混合氧化物催化劑,後者存在幾種形式:①生成複合氧化物,如尖晶石、重晶石、含氧酸鹽-雜多酸等;②形成固溶體,如氧化鐵-氧化鉻、氧化釩-氧化磷等;③相互分開的混合物,通過協同效應產生催化作用。有些催化劑雖然在催化劑生產廠出廠時是以氧化物的形態提供,但經用戶活化處理後,或在使用過程中,會轉變或部分轉變為金屬態。在氧化物催化劑中,多含有催化劑載體,如氧化鋁載體、矽膠載體等。
參考書目
清山哲郎著:《金屬酸化物とその觸媒作用》,講談社,東京,1978。

