流行病學
 染色體顯示圖
染色體顯示圖病因:
多為常染色體隱性或顯性遺傳致纖維蛋白原缺乏。
發病機制:
纖維蛋白原是一種含有2964個胺基酸的大分子糖蛋白,分子量為34萬 由Aα Bβ、γ3條多肽鏈以鏈間二硫鍵即AαCys28、γCys8和Cys9相連構成的對稱性二聚體(Aa、Bβ、γ)2,(Aα、Bβ、γ)。另外 單體中AαCys36與另一單體即CβC65組成的二硫鍵對形成二聚體分子也起到關鍵作用。
Aα Bβ γ3條多肽鏈在肝臟由獨立的多核糖體合成其前體蛋白(各包括19、30 26個信號肽),在粗面內質網內將信號肽切除、疏水反應和二硫鍵形成等加工後,摺疊、裝配成成熟的二聚體分子,最後經糖基化、部分磷酸化分泌到胞外。
在成熟的纖維蛋白原二聚體分子中,中央區(E區)由6條多肽鏈的氨基端組成,形成二硫鍵結(DSK);2個外圍區(D區)由Bβ鏈和γ鏈的羧基端組成,而Aα鏈的羧基端折回參與E區結構。E區與D區之間由帶狀結構(coiled-coil區)相連,coiled-coil區為Aα、Bβ、γ 3鏈形成的α-螺鏇結構,大約由110個胺基酸殘基組成,coiled-coil區兩端的二硫鍵對纖維蛋白原分子成熟二聚體結構的形成至關重要。
在凝血共同途徑中,凝血酶先裂解纖維蛋白原2條Aα鏈氨基端Argl6-Gly17釋出一對纖維蛋白肽A(FPA),形成纖維蛋白單體Ⅰ(FMI);再裂解纖維蛋白原2條Bβ鏈氨基端Arg14-Gly15釋出一對纖維蛋白肽B(FPB),形成纖維蛋白單體Ⅱ(FM2),此時纖維蛋白原的分子結構由(Aα、Bβ、γ)2變成(α、β γ)2 暴露出纖維蛋白單體的聚合部位。通過E-D區、D-D區和邊-邊的非共價結合,形成不穩定的可溶性纖維蛋白單體(SFM)。在活化的凝血因子ⅩⅢ(FⅩⅢa)和Ca2+ 的作用下,纖維蛋白單體(SFM)互相交聯,生成穩定的可溶性纖維蛋白,並將血液的有形成分包繞其中,形成牢固的止血血栓。
纖維蛋白原尚有與血小板膜糖蛋白GPⅡb-Ⅲa結合的位點,從而介導血小板的聚集反應,協同起到止血作用。
纖維蛋白原Aα Bβ、γ3條多肽鏈分別由3個獨立的基因FGA、FGB FGG編碼,集中於4q28~4q31約50 kb的區域內 3個基因由5′至3′的排列順序為FGG、FGA、FGB。FGA基因全長5.4kb 在生理情況下 由於3′端的不同剪接可產生2個不同的轉錄版本:人群中98%~99%剪接成5個外顯子 而1%~2%可產生6個外顯子的αE轉錄版本。FGB基因全長8.2kb 有8個外顯子且呈逆序排列 FGG基因全長8.4 kb,有10個外顯子。
遺傳性纖維蛋白原減低和功能異常時,纖維蛋白原基因都是存在的,但是,纖維蛋白原的合成、分泌或最終產物的細胞內處理等存在異常。當新合成的纖維蛋白原不能正常分泌而滯留在肝細胞的粗面內質網中,可能導致肝臟疾病的發生。
在動物實驗中將小鼠的Aα鏈基因剔除後可以導致纖維蛋白原所有的3條鏈缺失,基因剔除小鼠的胚胎髮育並沒有明顯的異常,但是,在出生時有1/3的小鼠發生明顯出血,主要出血部位有腹腔、皮膚和關節腔。由於在出生時發生出血最終都可以得到控制,因此,雖然有反覆發作的出血,大多數小鼠都可以活到成年,但是,雌性小鼠無法進行正常懷孕。
在真正的低纖維蛋白原血症中,患者的纖維蛋白原的2條等位基因是正常的 與之相反,無纖維蛋白原血症的2條基因呈雜合狀態 一條正常,另外一條異常。無論是無纖維蛋白原血症或是低纖維蛋白原血症,纖溶系統和其他的凝血途徑都完全正常,機體中不應存在任何使凝血機制激活,纖維蛋白原消耗或降解的情況。另外,位於4號染色體上的纖維蛋白原基因所包含的3個獨立的基因α、β和γ在無纖維蛋白原血症的患者中都存在,導致無纖維蛋白原血症的分子機制尚不十分清楚。無纖維蛋白原血症為常染色體隱性遺傳性疾病。許多病例都是由於近親婚姻所導致
導致無纖維蛋白原血症最常見的基因突變為FGA基因ⅣS4+1G>T的剪接突變 即FGA基因4號內含子的第一個鹼基G置換為T,從而改變4號內含子5′剪接點的保守序列,影響其與U1snRNP的結合,最終導致FGA基因的異常剪接。上海瑞金醫院上海血液學研究所發現1例遺傳性無纖維蛋白血症家系,父系家族成員FgFGA基因外顯子3-內含子3交界處,缺失AGTA或GTAA,母系家族成員則存在另一個大片段缺失,先證者為這兩種突變的複合雜合。
無纖維蛋白原血症的基因型與表型間關係並不確定 一般纖維蛋白原基因截短得愈多,纖維蛋白原水平愈低,從而產生低或無纖維蛋白原血症。但是,同一基因型也可產生不同的表型。總體上講,在無纖維蛋白原血症的患者中雖然某些篩查實驗,如APTT 出血時間明顯異常,但是,臨床上出血的表現並不嚴重,這一現象與纖維蛋白原基因剔除小鼠中所觀察的現象相吻合,只是在臨床中無纖維蛋白原血症的孕婦發生流產的機率並沒有明顯的升高。在部分患者中甚至有血栓形成,其機制可能與血管內血小板的異常聚集有關。
臨床表現
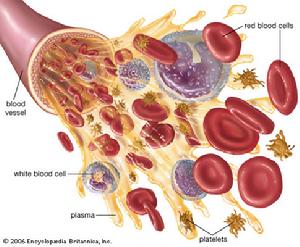 血小板病理圖
血小板病理圖雖然20%的無纖維蛋白原血症的患者曾發生關節出血,但是,其嚴重程度和後果都不如血友病患者。接受纖維蛋白原替代治療的患者中發生血栓性疾病的機率較正常人為高,其機制尚不清楚 除非纖維蛋白原的水平低於50mg/dl 否則低纖維蛋白原血症的患者一般不會發生自發出血。這些患者可能實際上是所謂低異常纖維蛋白原血症患者。
併發症:
主要的病死原因是嬰幼兒時期的並發顱內出血,在年長兒中出血可發生於任何部位,有時出血是致命性的。遺傳性無纖維蛋白原血症的患者有發生自發性脾破裂的危險。
診斷
根據陽性家族史,臨床表現結合實驗室檢查即可診斷。
鑑別診斷:
遺傳性纖維蛋白原缺乏應與獲得性纖維蛋白原缺乏仔細鑑別,後者多見於肝臟疾病或彌散性血管內凝血(DIC)。由於門冬醯胺酶可以阻礙肝臟對纖維蛋白原的合成,因而在套用門冬醯胺酶後可能出現纖維蛋白原減少。再生障礙性貧血的患者在接受抗胸腺細胞球蛋白(ATG)和糖皮質激素的患者也容易發生低纖維蛋白原血症。
實驗室檢查:
1.凝血酶原時間(PT)、活化部分凝血活酶時間(APTT)和凝血時間都延長,這些檢查的異常都可以被加入的正常血漿所糾正。
2.血漿中循環纖維蛋白原抗原的特異性檢測,是無纖維蛋白原血症的特異性檢查。
3.血小板中的纖維蛋白原缺如亦是無纖維蛋白原血症的特異性檢查。
4.外周血 在大多數情況下,血小板的數量不會低於100×109/L。白細胞、紅細胞、血紅蛋白正常。
5.血小板聚集不良。
6.出血時間延長。
其它輔助檢查:
皮膚有超敏反應的無纖維蛋白原血症患者不會出現硬結現象,因為其後續的反應需要皮下纖維蛋白原的堆積,因此,他們在過敏原的作用下僅顯示出皮膚紅斑。在真正的低纖維蛋白原的患者中,血漿纖維蛋白原的水平約為正常的一半,但是,在某些患者中可以觀察到更低水平的表達。
治療
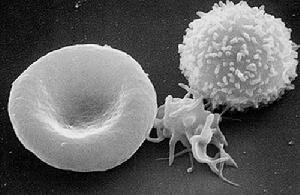 紅細胞(左)血小板(中)白細胞(右)病理圖
紅細胞(左)血小板(中)白細胞(右)病理圖在無纖維蛋白原血症患者並不推薦使用DDAVP 儘管有報導認為DDAVP可以改善血小板功能、縮短出血時間。無纖維蛋白原血症替代治療的主要不良反應包括過敏反應、產生同種抗體等,當同時套用抗纖溶藥物或口服避孕藥時,輸注冷沉澱後可發生包括深靜脈血栓和肺梗死在內的血栓性併發症,在凍乾人纖維蛋白原(纖維蛋白原)替代治療的同時套用低分子量肝素曾被用來預防血栓性疾病的發生。
預後及預防
預後:
病死率很高,主要死因顱內出血。
預防:
1.在女性這些患者中還可觀察到胎盤破裂和產後大出血,如果不給予替代治療,則無纖維蛋白原血症的女性患者大多數會發生早產,部分有可能在孕早期(最初的3個月)發生流產,補充纖維蛋白原可能有一定的防治作用。
2.肝素可用來預防血栓的發生。
