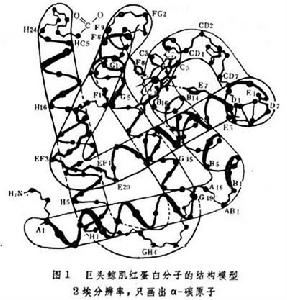
生物大分子衍射技術
X 射線衍射技術能夠精確測定原子在晶體中的空間位置,是迄今研究生物大分子結構的主要技術。中子衍射和電子衍射技術則用來彌補X射線衍射技術之不足。生物大分子單晶體的X射線衍射技術是50年代以後,首先從蛋白質的晶體結構研究中發展起來的,並於70年代形成一門晶體學的分支學科──蛋白質晶體學。生物大分子單晶體的中子衍射技術用於測定生物大分子中氫原子的位置,也屬蛋白質晶體學。纖維狀生物大分子的X射線衍射技術用來測定這類大分子的一些周期性結構,如螺鏇結構等。以電子衍射為原理的電子顯微鏡技術能夠測定生物大分子的大小、形狀及亞基排列的二維圖象。它與光學衍射和濾波技術結合而成的三維重構技術能夠直接顯示生物大分子低解析度的三維結構。歷史回顧 1912年德國物理學家 M.von勞厄預言晶體是 X射線的天然衍射光柵。此後英國物理學家W.H.布喇格和W.L.布喇格開創了X射線晶體學。幾十年來,這門學科不斷發展和完善,測定了成千上萬個無機和有機化合物的晶體和分子結構。由它提供的結構資料已經成為近代結構化學的基礎。但是傳統的小分子晶體結構的分析方法不適用於原子數目多,結構複雜的生物大分子。直到1954年英國晶體學家M.F.佩魯茨等人提出在蛋白質晶體中引入重原子的同晶置換法之後,才有可能測定生物大分子的晶體結構。1960年英國晶體學家J.C.肯德魯等人首次解出一個由153個氨基
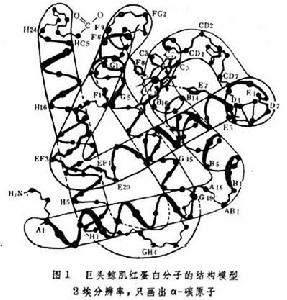 生物大分子衍射技術
生物大分子衍射技術晶體和X射線衍射 電磁波是直線傳播的,但在某些情況下也會拐彎,這就是衍射現象。當可見光通過針孔或狹縫時,就會出現這種現象。由於針孔或狹縫的大小和可見光的波長量級相同,可以把針孔或狹縫看做是一個點光源,它向四面八方輻射出二次電磁波,或稱散射波。如果有多個有序排列的針孔或狹縫,由於這些散射波的干涉,就會形成規則的明暗相間的衍射花樣。這是因為來自不同部位的散射波的相位及振幅不同,它們相加的結果在有些地方加強,而在另一些地方減弱。這些花樣隨波長或針孔的大小及其排布方式不同而變化(圖2)。當X射線通過晶體時,晶體內原子的核外電子能夠散射X射線。如果把每個原子看成是個散射源,由於X射線的波長同原子間的距離量級相同,因此也會發生衍射現象。晶體結構的特徵是晶體內的原子或分子周期重複地排列。如果採用一組抽象的幾何點來表示這種周期重複的規律,那么這種排列可以表示為點陣。晶體的三維點陣結構使得晶體可被劃分成為無數個大小和形狀完全相同的平行六面體,即被稱為晶胞。它是晶體結構的基本重複單位。每個晶胞內包含種類、數目和排列完全相同的原子。可以推得,衍射線(也稱反射線)的強度取決於晶胞的內容,它的方向取決於波長和晶胞的大小和形狀。
晶體結構測定 晶體對X射線、中子束及電子束的衍射,與規則排列的針孔對可見光的衍射遵循相同的光學變換原理,即針孔或晶體的結構(針孔或晶體中原子的排列)經傅立葉變換,可以得到它們的倒易圖像──衍射波譜。反之,衍射波譜的反變換,即為正空間的圖像──針孔的排列或晶體的結構。在可見光的衍射中,這種反變換可由透鏡的聚焦過程實現。但是迄今為止,人們還未找到能使 X射線(或中子)散射線聚焦的辦法。因此也就無法直接觀察生物大分子的像。這只能藉助電子計算機從數學上完成這種反變換的計算。它的計算式為
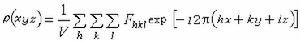 這個算式表示 ρ(xyz)等於
這個算式表示 ρ(xyz)等於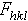 數值的傅立葉綜合。式中V指晶胞體積,hkl稱為衍射指標,表示衍射方向或反射的位置。ρ(xyz)是電子密度函式,表示晶胞中坐標為(xyz)點上電子密度的數值。電子密度峰的位置即為原子的中心位置。
數值的傅立葉綜合。式中V指晶胞體積,hkl稱為衍射指標,表示衍射方向或反射的位置。ρ(xyz)是電子密度函式,表示晶胞中坐標為(xyz)點上電子密度的數值。電子密度峰的位置即為原子的中心位置。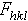 稱為晶胞對應hkl反射的結構因子。它的表達式為:
稱為晶胞對應hkl反射的結構因子。它的表達式為: 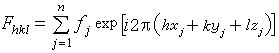
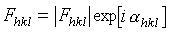
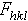 為複合波的振幅,稱為結構振幅。它的平方值與衍射強度成正比關係,因此可由實驗測定。指數
為複合波的振幅,稱為結構振幅。它的平方值與衍射強度成正比關係,因此可由實驗測定。指數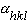 為複合波相對晶胞原點散射的相位差。對於生物大分子晶體,一般情況下它的值難以從衍射強度數據直接求得,因而也就無法直接由此計算電子密度函式。這是大分子晶體結構測定的主要困難所在,通常也被稱為相位問題。
為複合波相對晶胞原點散射的相位差。對於生物大分子晶體,一般情況下它的值難以從衍射強度數據直接求得,因而也就無法直接由此計算電子密度函式。這是大分子晶體結構測定的主要困難所在,通常也被稱為相位問題。 目前確定生物大分子晶體晶胞衍射相位的方法已有幾種,如同晶置換法,反常散射法及分子置換法等。其中同晶置換法可以普遍適用,其他方法根據情況選用。同晶置換法需要製備同晶型的重原子衍生物,即在不會改變分子和晶體結構的情況下,在晶體中引入一種較重的金屬原子。這些金屬原子在晶體中以和其他原子相同的周期重複規律排列。它們對於 X射線的散射僅影響晶體的衍射強度,而不改變衍射方向。這時重原子的結構振幅可由衍生物與天然晶體衍射強度的差值求得。由於晶體中引入重原子的數目有限,我們可以採用別的辦法(例如帕特遜函式法)來確定它們的位置,進而可以計算重原子的結構因子。如果能有兩個以上同晶型的衍生物,就可利用矢量三角形法則求得天然晶體的相位,因而也就可以解出這種晶體的結構。這種方法稱為多對同晶置換法。當晶體中重原子的吸收邊接近入射 X射線的波長時,重原子內層的約束電子對於入射線會有很強的散射作用,稱為反常散射。此時晶體衍射強度的中心對稱定律不再成立,即|
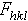 |≠|
|≠|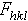 |。這就相當於使用一種晶體收集兩套衍射強度數據。其效果等於有了兩個同晶型的衍生物。因此可以採用類似同晶置換的辦法解出晶體結構。這種方法稱為反常散射法。許多蛋白質分子是由相同或相似的亞基組成的,它們之間具有結構的相似性。對於那些結構相同或相似的蛋白質分子,如果得到晶型不同的晶體,那么它們在不同晶胞中的差異在於空間處向以及排布方式不同。另外,即使在一種晶胞的晶體學不對稱單位內,也可存在相同或相似的亞基結構。它們之間存在非晶體學的對稱關係。因此可以通過鏇轉變換和平移變換的辦法,使得這些相同或相似的結構重合。這樣,如果已知一個結構,就可結合晶體學的結構修正方法求得另外一個未知的結構。這種方法稱為分子置換法。
|。這就相當於使用一種晶體收集兩套衍射強度數據。其效果等於有了兩個同晶型的衍生物。因此可以採用類似同晶置換的辦法解出晶體結構。這種方法稱為反常散射法。許多蛋白質分子是由相同或相似的亞基組成的,它們之間具有結構的相似性。對於那些結構相同或相似的蛋白質分子,如果得到晶型不同的晶體,那么它們在不同晶胞中的差異在於空間處向以及排布方式不同。另外,即使在一種晶胞的晶體學不對稱單位內,也可存在相同或相似的亞基結構。它們之間存在非晶體學的對稱關係。因此可以通過鏇轉變換和平移變換的辦法,使得這些相同或相似的結構重合。這樣,如果已知一個結構,就可結合晶體學的結構修正方法求得另外一個未知的結構。這種方法稱為分子置換法。 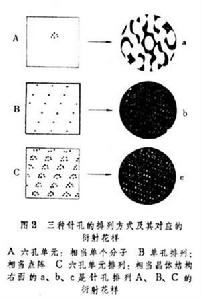 生物大分子衍射技術
生物大分子衍射技術蛋白質晶體學的成就 在晶體結構測定的早期階段,人們首先看到的是α-螺鏇,β-摺疊層等二級結構在天然蛋白中的實際表現。隨著更多的結構問世,人們逐漸地對於蛋白質中非成鍵原子間的弱相互作用有了更加透徹的了解,從而不斷總結出一些結構規律。例如人們已可以對球蛋白的結構進行解析和分類。有人將這類蛋白質的結構單元分為幾大類,即螺鏇、β-結構、回折、凸包、硫橋、不重複結構、無序結構、水結構及結構域等。並對每一類的結構規律有了一定的了解(見蛋白質)。
目前,由晶體學所測定的蛋白質大致可以分為:酶、氧化還原蛋白、運載蛋白、貯存蛋白、激素、抗體、DNA結合蛋白、糖結合蛋白、肌肉蛋白、毒素膜蛋白等。這些晶體結構的測定揭示了結構與功能的緊密關係。例如溶菌酶的活性部位是個界限清楚的裂縫,而胰凝乳蛋白酶的活性部位是個深為10~12埃的口袋。這些結構特徵都和它們的底物或抑制劑分子的性質、大小和形狀有關。胰蛋白酶、彈性蛋白酶與胰凝乳蛋白酶具有十分相似的三維結構,它們結合底物或抑制劑特異性的差別僅由於活性部位的少數殘基不同。在醇脫氫酶中,反應是通過活性部位上的鋅結合水而起作用的。在大多數情況下,當底物與酶結合時,酶分子將發生構象變化,即所謂誘導契合。在某些情況下,一些催化基團可移動相當距離。血紅蛋白是一類運載蛋白,在血液中擔負輸氧的任務。晶體結構的測定闡明了它的別構效應。其他由 4個相同的亞基配對組成。每個亞基都含一個鐵原子,它們位於各個血紅素的中心。晶體結構測定表明這些血紅素處於蛋白表面的疏水袋中。這個低介電常數的環境使得它們不易氧化而利於氧合。當第一個亞基發生氧合時,血紅素上的鐵原子相對卟啉環作微小的移動,同時鐵原子的自鏇態躍遷。這些變化被傳遞到分子的其他亞基上,並使它們的鐵原子也與氧結合。這種構象上的協同變化稱為別構效應,它是血紅蛋白輸氧的主要機制。胰島素是一種激素蛋白。在它的晶體結構問世以前,人們對它的作用機理和部位了解甚少。70年代初,牛津小組和北京小組分別獨立解出胰島素的晶體結構,為胰島素作用機理的研究開闢了廣闊的前景。從結構模型上可以看到不同種屬中保持不變的殘基集中於某些部位。這些殘基的化學修飾對於生物活性非常敏感。說明這些部位對於靶細胞膜表面胰島素受體結合的重要性。光合作用是植物有效地將光能轉換成化學能的過程。長期以來,人們曾以極大的努力研究它的原理,試圖揭示它的奧秘。但是直到80年代,也是由於晶體學的成就才使這個研究領域取得突破性的進展。1985年由聯邦德國晶體學家R.胡伯領導的研究組測定了一種綠色細菌光合反應中心蛋白質複合體的晶體結構,並闡明了光激發電子是如何在這複合體上產生、傳遞,從而通過細胞膜的。他們的成就不僅使得人們能在原子水平上認識光合作用的原初機制,而且對於人類新能源的開發,也是一個重要的啟示。
蛋白質的三維結構還為生命物質的進化研究提供非常有用的信息。特別是那些一級結構相差甚遠,功能已經完全迥異的一類蛋白質的所謂發散進化。研究它們的祖先同源性不可能依賴解剖學、組織學,甚至一級結構的測定工作。但有趣的是這一類蛋白質的三維結構卻是保守的,尤其是活性部位的結構更不因一級結構的變化而改變。例如最近的三維結構研究表明,內分泌控制系統的大多數激素都屬於一個家族。這一家族現在正在擴充它的成員,甚至包含來自血漿和神經傳導物質的生長因子以及來自中樞神經系統的神經調節物質。胰島素和胰島素樣生長因子的結構同源性就是例子。
70年代以來,核酸中的一類──tRNA的晶體結構分析、一些與 DNA專一性結合的蛋白質及其複合體的結構分析、以及組成染色質的基本單位核小體的結構分析使得生物大分子晶體學的發展進入一個新的階段。這些工作為研究構成生命的兩大類物質核酸-蛋白質的相互作用及其裝配機制奠定了基礎,並開始在分子水平上揭開基因的表達與調控之謎。最近完成的動物病毒如小兒麻痹病毒,感冒病毒的高解析度的結構分析使得可能透徹研究這些最小的生命實體,具有深遠的理論和實際意義。
近來,由於蛋白質晶體學與基因工程相結合,產生了蛋白質工程這一新的領域。利用這項技術,人們已經開始按照主觀的願望來設計和製造原來自然界中並不存在的蛋白質,其中包括治療各種疾病的有效藥物。
X 射線衍射技術在生物大分子結構與功能關係的研究中也有它的局限性。首先,這項技術要求待測結構的大分子必須長成單晶體。但在千萬種生物大分子中能夠結晶的僅是少數。很多具有重要生物學意義的生物大分子以及其他重要的生命物質還難以結晶,因而也就無法套用這項技術測定它們的結構。其次,這項技術只能測定生物大分子在晶態時按時間平均的靜態構象。雖然已有一些事實證明這種結構與生物大分子在生理狀態時的結構基本相同。但是生物大分子結構的更多奧妙在於它們的運動形式。它們的功能往往是在構象變化中表現出來的。近年來,由於二維核磁共振(NMR)及其他技術的發展,已有可能測定溶液中生物大分子的三維結構及其動態行為。
 生物大分子衍射技術
生物大分子衍射技術中子衍射技術 氫原子在生物大分子的結構與功能中具有重要作用。但是它們對X射線的散射能力很弱,因而一般情況下很難由X射線衍射技術測定它們的位置。中子衍射技術正是用來彌補這個欠缺。中子具有波的性質。它的衍射原理與 X射線衍射相似。原子對中子的散射主要由原子核貢獻。它們的散射能力由核結構決定,而與原子序數無一定關係。而且同一元素中各同位素原子的散射能力,由於核的結構不同而有顯著的差別。甚至有些原子由於產生核內共振而使它們的散射振幅(或稱散射長度)為負值。例如氫原子。但是它的同位素氘原子(2 H或D)的散射振幅卻大到與碳、 氧原子的數值相近【H=-3.8,D=6.7,C=6.6,O=5.8×10-12 厘米】。利用這對同位素原子對於中子散射的不同性質,並通過D-H交換的辦法,由氘原子取代分子及晶體結構中的氫原子,它們的位置就可由中子衍射技術測定。另外,新近有人還從氘氫交換前後兩套衍射數據計算的 D2O-H2O差值中子密度圖上,得到了有關蛋白質中水結構的更多信息。在這項技術的套用中,可舉牛胰蛋白酶為例。在絲氨酸類蛋白酶水解肽鍵時伴隨一個質子轉移的過程。但不知這個質子最終定位何處。由量子化學計算及多種技術測量得到的結論各不相同。最後通過氘氫交換的晶體中子衍射研究,辨明這個質子定位在活性部位中57位組氨酸的咪唑環上。從而確定這個基團在催化過程中起鹼催化作用。
中子衍射用的中子束一般來自核反應堆。但從反應堆引出的熱中子流經準直和單色化後強度較弱,因此要求被測晶體大於2立方毫米,測量時間至少長達1~2個月。由於這些限制,使得至今還只有肌紅蛋白、核糖核酸酶、胰蛋白酶、溶菌酶、甘比菜蛋白及牛胰蛋白酶抑制劑等少數生物大分子晶體已被用來進行中子衍射研究。
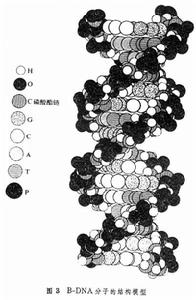
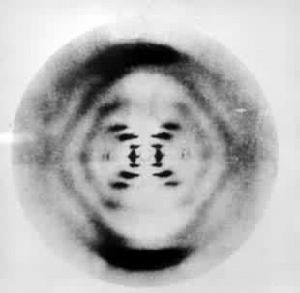
X射線纖維衍射技術 生物大分子中的螺鏇分子,如角蛋白、膠原及遺傳物質 DNA(脫氧核糖核酸)等大多難以結晶(寡聚核苷酸例外),但能聚集成為纖維。平行排列這些纖維也能使 X射線發生衍射。這些螺鏇分子的外形相似於彈簧,有可測量的螺距和半徑。每圈螺鏇包含數目相同的單元。因此它們的長軸方向具有周期結構的性質。它們的衍射花樣呈X形,且在水平方向衍射點按層線排列。由X形的斜度及層線的間距可以計算螺距和半徑。由中心至垂直最遠衍射弧的距離可以計算單元間沿螺軸方向的距離。由於這些大分子的徑向側鏈處於無序狀態,它們對X射線僅產生背景散射。因此纖維衍射技術無法測定大分子中原子的空間位置。但是如果結合考慮這些大分子的化學組份及立體化學等性質,也可由衍射花樣推斷該分子的結構模型。DNA分子的右手雙螺鏇模型(圖3)的建立是個典型的例子。這是由美國生物學家J.D.沃森和英國物理學家F.H.C.克里克於1953年提出來的。當時已知 DNA分子由多聚脫氧核苷酸鏈組成
 生物大分子衍射技術
生物大分子衍射技術雖然纖維衍射所能提供的結構信息遠比晶體衍射少,但是這項技術可以用來研究生物大分子在接近生理條件下的構象及其變化。例如當改變同一 DNA分子的相對濕度或離子含量時,它的構象可有A、B、C、S等幾種類型的相互轉換。採用由同步回旋加速器輻射產生的強 X射線,可以研究肌肉纖維收縮的運動模式。
參考書目
周公度:《晶體結構測定》,科學出版社,北京,1981。
T.L.Blundell,L.N.Johnson,Protein Crystallogra-phy,Academic Press,New York,1976.