簡介
DNA 是負責遺傳的主要分子,由 A、C、T、G 四種不同的單元依任意的順序排列,例如一個有 10 個單元的 DNA 分子,會有 4 的 10 次方種不同的排列順序,各種生物的遺傳雖然均由 DNA 分子負責,由於排列順序的差異,以致造成相互間極大的不同;RNA 是負責傳遞遺傳訊息的分子,它將 DNA 的遺傳密碼攜帶出來,並負責將 DNA 所下達的遺傳指令,合成相關的蛋白質。
蛋白質分子在生物細胞中,負責所有生化反應及新陳代謝的催化工作,如果身體中一個蛋白質功能失調,或合成的數量失衡,將導致生理機制失常的連鎖反應。由此可知這三種生物分子的重要性。
DNA 分子會進行自我複製,而 DNA 分子將遺傳訊息傳遞給 RNA 分子的過程稱為轉錄,RNA 分子根據 DNA 所提供的訊息製造出相關蛋白質的過程則稱為轉譯。
生物分子的常見基團
(一)羥基-OH
很多有機分子上含有羥基-OH,如醇、糖、核酸、蛋白質等,“羥”的字和音都由“氫氧”二字拼合而成。羥基與水有某些相似的性質,羥基是典型的極性基團,與水可形成氫鍵,因此,分子上羥基越多,親水性就越大。羥基與電負性大的原子如-NH中的氮能形成氫鍵,氫鍵在維持蛋白質、核酸等大分子的空間結構中發揮著重要的作用。氫鍵是一種比離子鍵弱得多的靜電吸引力,容易被一些外力如加熱所破壞,蛋白質、核酸遇熱變性就是因為熱力導致分子中氫鍵斷裂,空間結構破壞,蛋白質與核酸的性質與功能發生改變,原有生物學功能喪失。
醇與醇的脫水縮合產物稱為醚,含有-C-O-C-結構;單糖分子通過半縮醛與另一分子的-OH脫水縮合後也存在-C-O-C-結構,不稱醚,而特稱為苷(音gan,舊稱甙dai),澱粉、糖原等分子中的-C-O-C-稱為糖苷鍵。
苯環上連線羥基的化合物稱為酚。
(二)羰基 >C=O(-CHO醛基、>CO 酮基、-COOH羧基)
>C=O稱為羰基(羰的字和音均由碳氧二字拼合而成)。細胞里含有羰基的化合物常見的有四種:羰基(酮基)在碳鏈中間的化合物稱為酮;如果羰基在碳鏈末段的有兩種形式,含-CHO的分子稱為醛,含-COOH的稱為羧酸(羧字是“羥基酸”的拼合);如果同時有2個羰基存在於苯環上稱之為醌。醛、酮、羧酸、醌化合物在細胞里很常見,尤其是酮和羧酸,如丙酮、β-酮丁酸(乙醯乙酸)、α-酮戊二酸、泛醌(輔酶Q)、磷酸吡哆醛等。羧基可解離產生氫離子而形成負電離子-COO-,因此,羧基是酸性基團。
(三)氨基-NH2和亞氨基-NH
體內含氨基和亞氨基的化合物種類很多,所有的胺基酸都含有氨基或亞氨基,如丙氨酸(含氨基)、脯氨酸(含亞氨基)。如果羧基上的羥基與氨脫水縮合而成-CO-NH2,這樣的化合物稱為醯胺,在碳鏈中間的形式是-CO-NH-,稱為醯胺鍵,蛋白質分子中胺基酸與胺基酸就是通過醯胺鍵連線的。肽鏈中間的醯胺鍵特稱肽鍵。含有氨基和亞氨基的還有胍基和眯唑基。氨基中的氮原子電負性較強,可以結合氫離子而成-NH3+、=NH2+,因此,氨基和亞氨基是鹼性基團。
(四)巰基-SH和二硫鍵-S-S-
巰的字和音均由氫硫二字拼合而成。帶有巰基的化合物最常見的是半胱氨酸HOOC-CH(NH2)-CH2-SH、谷胱甘肽G-SH以及含半胱氨酸殘基的各種蛋白質。兩個半胱氨酸的兩個巰基可以脫氫氧化為胱氨酸而在分子中形成-S-S-結構,-S-S-稱為二硫鍵(二硫橋),二硫鍵是巰基的氧化形式,二硫鍵可加氫再還原為巰基。谷胱甘肽、巰基蛋白及巰基酶的活性基團是巰基,通過巰基參與反應。
(五)磷酸基-H2PO4
體內含磷酸基的化合物非常廣泛,如葡萄糖-6-磷酸,磷酸烯醇式丙酮酸,核苷酸和核酸,磷酸蛋白質等等。2分子磷酸可以脫水縮合為焦磷酸酐(亦稱焦磷酸酯),如ATP分子含有三個磷酸基,其中3個磷酸基之間含有2個磷酸酯(酐)鍵,此鍵斷開時可釋放大量能量,因此稱為高能鍵。在細胞的很多代謝反應中,往往第一階段的反應是使底物分子活化(使不活潑分子變得活潑以進行反應),活化的常見反應是由ATP提供一個高能磷酸基團給被活化的分子,如葡萄糖由ATP供能活化為葡萄糖-6-磷酸。
(六)酯、酐、醯胺
含氧酸與醇的脫水縮合產物稱為酯。細胞內常見的酯有羧酸與醇(-OH)形成的酯,如甘油(丙三醇)和三分子脂肪酸脫水縮合形成的三脂醯甘油(甘油三酯,即脂肪);羧酸與-SH形成的硫酯(-SH與-OH性質類似),如輔酶A上的巰基與乙酸上的羧基脫水縮合為乙醯輔酶A,乙醯輔酶A就是一種硫酯,這個硫酯鍵斷開時也能釋放大量能量,因此稱為高能硫酯鍵。含有高能硫酯鍵的化合物還有琥珀酸單醯輔酶A、脂肪醯輔酶A等。
含氧酸與含氧酸的脫水縮合產物稱為酐,如羧酸-羧酸酐,羧酸-磷酸酐,磷酸-磷酸酐等。羧基、磷酸基由於含有羥基,因此羧酸-羧酸酐,羧酸-磷酸酐,磷酸-磷酸酐相當於是酸與醇的脫水縮合產物,因此這些酐也可稱為酯。正如上述,ATP中的兩個高能磷酸酯鍵亦稱為高能磷酸酐鍵。
前已述及,羧酸與氨的脫水縮合產物稱為醯胺R-CO-NH2,胺基酸的α-羧基與另一胺基酸的α-氨基脫水縮合形成的特殊醯胺鍵-CO-NH-稱為肽鍵。
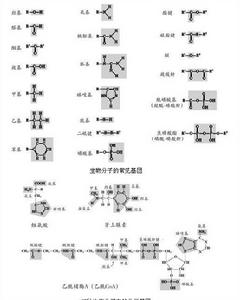 生物分子基團
生物分子基團水:生命活動的介質環境
水是生物體的第一大化合物,含量在50%以上,甚至可達99%。人體的含水量隨年齡增長而減少,從新生兒80%到老年的55%。
地球表面的70%為水覆蓋,水是地球表面最豐富的物質,水在地球表面以三種狀態同時存在。液態水是良好的極性溶劑,很多物質都能溶於水中,眾多的化學反應在水中能非常好的進行。生命現象主要是生物體內一系列生物化學反應的外部體現,因此,水是生命存在的介質環境,沒有水就沒有生命。
水分子的形狀是一個等腰三角形,分子內O-H間的鍵長約為0.0965nm,H-O-H鍵角為104.5°。氫原子的電子由於氧原子核的強力吸引而偏向氧,結果使氫被氧化而呈正電,氧呈負電。由於氧原子只有兩對電子是與質子(氫原子核)共享的,在8電子殼層中還有兩對電子暴露在O-H的外部,這兩對電子吸引相鄰水分子上的正電,從而形成氫鍵。因此,水分子通過氫鍵而相互連線起來。水與其他分子的負電性原子形成鍵能大致相同的氫鍵,例如羧基中的-OH基團中的氧或蛋白質-NH基團中的氮都可與水分子的氫形成氫鍵。在分子中如果含有-OH、-NH等極性基團的分子與電負性強的原子也能形成氫鍵。在蛋白質分子中,存在著大量的氫鍵,從而使蛋白質的結構得到加固。氫鍵在加固核酸的特殊結構中也起著重要的作用。此外,水還能夠和一些小分子有機化合物形成氫鍵。氫鍵的鍵能大約只有共價鍵的十分之一,幅度較小的溫度變化就可以使氫鍵斷開。這就使得帶氫鍵的結構具有顯著的柔順性,使它們能隨著內外環境的變化而變化。
生物體內物質的運輸是依賴水良好的流動性完成的,另外水還有恆溫、潤滑等多種作用。
無機鹽:參與和調節新陳代謝
無機鹽在細胞里含量很小,人體內的無機鹽大約占5%左右,種類很多,含量最多的無機鹽是鈣和磷鹽約占無機鹽含量的一半左右,主要沉積在骨骼和牙齒中,無機鹽的另一半大多以水合離子狀態存在於體液中。由於無機鹽的種類多樣,因此功能不一。總體來說,無機鹽有如下功能:
1.構成骨骼和牙齒的無機成分,對身體起支撐作用。骨骼中無機物約占1/3,有機物占2/3。存在於骨骼中的無機鹽主要是鈣和磷,有機物主要是蛋白質。有機物使骨骼具有韌性,無機鹽使骨骼具有硬度。骨骼中的鈣磷鹽是體液中鈣磷鹽的貯存場所(鈣磷庫)。
2.維持生命活動的正常生理環境。Na+、Cl-、K+、HPO42-在維持細胞內外液的容量方面起著重要的作用。體內各種酶的作用需要相對恆定的pH,體液的緩衝系統由這些鹽類構成,發揮穩定氫離子濃度的功能。同樣,無機鹽對肌肉、心肌的應激性的維持也有重要的作用。
3.參與或調節新陳代謝。體內很多酶需要離子結合才具有活性,有些離子可以增強或抑制酶的活性。某些離子參與物質轉運、代謝反應、信息傳遞等多種功能。
無機鹽是機體新陳代謝的重要調節和參與因素。
蛋白質:生命活動的主要表現者
蛋白質是生物體的第二大化合物,在細胞的乾重中,約一半以上是蛋白質,在活細胞中的含量在15%以上。蛋白質是大分子物質,分子量在6000至百萬道爾頓。蛋白質的英文名叫做protein,源自希臘文προτο,它是“最原初的”,“第一重要的”意思。“朊”這個詞就是根據protein的原意翻譯的,但由於蛋白質一詞沿用已久,所以“朊”並未被廣泛採用。蛋白質在生物體內占有特殊的地位。蛋白質和核酸構成原生質中的主要成分,而原生質是生命現象的物質基礎。
蛋白質是生命的結構基礎和功能基礎。蛋白質廣泛地存在於細胞膜、液態基質、細胞器、核膜、染色體等結構中,蛋白質中的一半左右是酶-生物催化劑,細胞中眾多的化學反應由酶分子催化。蛋白質種類眾多,功能各異,總體來說,蛋白質具有下述功能:
1.催化和調控:體內物質代謝的一系列化學反應幾乎都是由酶催化的。體內各組織細胞各種代謝的進行和協調,都與蛋白質的調控功能密切相關。
2.在協調運動中的作用:肌肉收縮是一種協調運動,肌肉的主要成分是蛋白質,肌肉收縮是肌肉中多種蛋白質組裝成的粗絲、細絲完成的,從微觀上看是細胞內微絲、微管的活動,精子、纖毛的運動等都與蛋白質的作用有關。
3.在運輸及貯存中的作用:蛋白質在體內物質的運輸和貯存中起重要作用。例如,全身各組織細胞時刻不能缺少的氧分子,就是由血紅蛋白運輸的;氧在肌肉中的貯存靠肌紅蛋白來完成。鐵在細胞內需與鐵蛋白結合才能貯存。
4.在識別、防禦和神經傳導中的作用:體內各種傳遞信息的信使需與特異的受體相互識別,受體多為蛋白質,可見蛋白質在信息傳遞過程中起重要作用,另外,抗體對抗原的結合,神經衝動的傳遞等也是蛋白質參與完成的。
因此,蛋白質是生命過程中的主要分子,是生命現象的主要“演員”,蛋白質-生命的體現者。
核酸:生命活動的主宰者
核酸在體內含量很少,分為兩類:脫氧核糖核酸(DNA)和核糖核酸(RNA)。DNA主要存在於細胞核中,RNA主要存在於細胞質中。RNA主要有信使核糖核酸(mRNA)、轉運核糖核酸(tRNA)和核糖核蛋白體核糖核酸(rRNA)三種。
核酸是重要的生物大分子,是生物化學與分子生物學研究的重要對象和領域。生物的特徵是生物大分子決定的。生物大分子有四類:核酸、蛋白質、多糖和脂質複合物。糖和脂質的合成由酶(蛋白質)催化完成,它們與蛋白質在一起,增加了蛋白質結構與功能的多樣性。蛋白質的合成取決於核酸;然而生物功能通過蛋白質來實現,包括核酸的合成也需要蛋白質的作用。因此,生物體內最重要的大分子物質是DNA、RNA和蛋白質。由生物大分子和有關生物分子與無機分子或離子共同構成生物機體不同層次的結構;生物大分子之間以及與其他分子之間的相互作用決定了一切生命活動。概括地說,核酸(主要是DNA)是生命的操縱者,蛋白質是生命的表現者,糖和脂肪是生命的能源物質,磷脂是生物膜的結構基礎,水是生命存在的介質環境,無機鹽參與和調節新陳代謝。
G. Mendel於1865年發現豌豆雜交後代性狀分離和自由組合的遺傳規律。F. Miescher於1868年發現核酸(當時稱核素),細胞學家和遺傳學家曾猜測核素可能與遺傳有關。19世紀開始知道有兩類核酸,直到20世紀40年代才了解DNA和RNA都是細胞的重要組成物質,前者可引起遺傳性狀的變化,後者可能參與蛋白質的生物合成。50年代初生物學家開始接受DNA是遺傳物質的觀點。1953年,Watson和Crick提出DNA的雙螺鏇結構模型,才從分子結構上闡明了其遺傳功能。半個世紀以來,核酸研究已經成為生物化學與分子生物學研究的核心和前沿,其研究成果改變了生命科學的面貌,也促進了生物技術產業的迅猛發展,充分表明這類物質有重要的生物功能。
核酸的功能主要有以下三點:
1.DNA是主要的遺傳物質:DNA分布在細胞核內,是染色體的主要成分,而染色體是基因的載體。細胞內的DNA含量十分穩定,而且與染色體數目平行。基因是染色體上占有一定位置的遺傳單位。基因有三個基本屬性:一是可通過複製,將遺傳信息由親代傳給子代;二是通過轉錄表達產生表型效應;三是可突變形成各種等位基因。但有些病毒的基因組是RNA,基因是RNA的一個片段。一些可作用於DNA的物理化學因素均可引起DNA突變從而引起遺傳性狀的改變。DNA的突變是生物進化的基礎,即突變的累積導致生物進化。
2.RNA參與蛋白質的生物合成:實驗表明,由3類RNA共同控制著蛋白質的生物合成。核糖體是蛋白質合成的場所。過去以為蛋白質肽鍵的形成是由核糖體的蛋白質所催化,稱轉肽酶。1992年H. F. Noller等證明23S rRNA具有核酶活性,能夠催化肽鍵形成。rRNA約占細胞總RNA的80%,它是裝配者並起催化作用。tRNA占細胞總RNA的15%,它是轉換器,攜帶胺基酸並起解譯作用。mRNA占細胞總RNA的3~5%,它是信使,攜帶DNA的遺傳信息並起蛋白質合成的模板作用。
3.RNA功能的多樣性:20世紀80年代RNA的研究揭示了RNA功能的多樣性,它不僅是遺傳信息由DNA傳遞到蛋白質的中間傳遞體,雖然這是它的核心功能,。歸納起來,RNA有5類功能:①控制蛋白質合成;②作用於RNA轉錄後加工與修飾;③基因表達和細胞功能的調節;④生物催化與其他細胞持家功能;⑤遺傳信息的加工與進化。病毒RNA是上述功能RNA的游離成分。
生物體通過DNA複製,而使遺傳信息由親代傳給子代;通過RNA轉錄和翻譯而使遺傳信息在子代得到表達。RNA具備諸多功能,無不關係著生物機體的生長和發育,其核心作用是基因表達的信息加工和調節。
糖:生命活動的主要能源物質
糖在動物體內是四大類生物分子中含量最小的,但糖類是草食動物及人體消化吸收最多的食物成分(不計水),原因在於吸收的糖類消耗很快(能源物質)、可大量轉化為脂肪貯存及糖原貯存量較小造成的。
糖是多羥基醛或多羥基酮類化合物。糖的基本單位是單糖,如葡萄糖、果糖等。多數單糖有鏈式和環式兩種結構,並且環式結構存在α和β兩種異構體,三者之間可以相互轉化。由單糖可以聚合成雙糖、寡糖、多糖。雙糖如蔗糖(葡萄糖-果糖二聚體)、麥芽糖(葡萄糖二聚體)和乳糖(半乳糖二聚體),多糖的典型代表是植物中的澱粉和動物體的糖原。
糖在植物體中貯存較多,在動物體相對含量較小。動物體不能由無機物合成糖,動物體內的糖最初都是由植物提供的,植物通過光合作用能將二氧化碳和水合成為糖。
糖在體內有以下兩方面的功能:
1.細胞的重要能源物質:動物體攝取糖後,大量的糖是作為能源物質被使用。糖在體內氧化,釋放能量,釋放的能量以熱散發維持體溫和貯存於ATP、磷酸肌酸中以供生命活動所用。動物體攝取的糖如果有剩餘,能夠合成肝糖原和肌糖原以貯存糖,但量相對較小,一個中等身材的人只能貯存約500g左右的糖原。糖在身體內很容易轉化為高度還原的能源貯存形式脂肪,貯存於脂肪組織,以供糖缺乏的時候給身體提供能量。
2.糖在細胞內與蛋白質構成複合物,形成糖蛋白和蛋白聚糖,廣泛地存在與細胞間液、生物膜和細胞內液中,它們有些作為結構成分出現,有些作為功能成分出現。因此,糖蛋白和蛋白聚糖也是生命現象的“演員”。
脂類:生命的備用能源和生物膜的結構基礎
脂類是動物體內的第三大類物質。脂類大都是非極性物質,很難溶於水,脂類分為脂肪和類脂兩大類。脂肪是由甘油和脂肪酸縮合而成,類脂有磷脂、膽固醇及膽固醇酯等形式。脂肪的含量不穩定,是體內貯存的能源物質,變化很大,稱為可變脂或貯脂,一般成年男性脂肪占體重的10~20%。磷脂由於是細胞的結構成分,因此含量是穩定的,稱固定脂或膜脂,約占體重的5%。
1. 三脂醯甘油(脂肪)的丙三醇頭部是親水的,而3條脂肪酸尾部是疏水的。
2. X基團是極性的,常見的有膽鹼、乙醇胺、絲氨酸等。
3. 磷脂和糖脂只有2條或1條疏水性尾部,其餘都是親水的,因此磷脂和糖脂很容易形成油與水的分界膜。
脂類的主要作用有以下三點:
1.脂肪是貯存的能源物質:脂肪是高度還原的能源物質,含氧很少,因此相同質量的脂肪和糖相比氧化釋放的能量很多,可達糖的兩倍以上,並且由於脂肪疏水,因此可以大量貯存,但脂肪作為能源物質的缺點也是明顯的,因為疏水,所以脂肪的動員速度比親水的糖要慢。脂肪主要的貯存部位是皮下、大網膜、腸系膜和臟器周圍,貯存量可達15~20kg,足以維持一個人一個月的能量需要。
2.磷脂是生物膜的結構基礎:磷脂是脂肪的一條脂肪酸鏈被含磷酸基的短鏈取代的產物,因為這條磷酸基鏈的存在,使磷脂的親水性比脂肪的大,能夠自發形成磷脂雙分子層膜。生物膜的骨架就是磷脂雙分子層,再加上一系列的蛋白質和多糖就構成生物膜。生物膜在細胞中是廣泛存在的,因此,一個細胞的膜表面積很大。膜分隔細胞的空間使不同類的化學反應可以在不同的區間完成而不互相干擾,很多化學反應在膜的表面上進行。神經元細胞由於樹突軸突的存在,細胞膜面積十分巨大,因此神經組織是體內含磷脂最豐富的組織。
3.膽固醇的衍生物是重要的生物活性物質:膽固醇可在肝臟轉化為膽汁酸排入小腸,膽汁酸可以乳化脂類食物而加速脂類食物的消化;7-脫氫膽固醇可在皮膚中(日光照射下)轉化為維生素D3,然後在肝臟和腎臟的作用下形成1,25-(OH)2-D3,通過促進腸道和腎臟對鈣磷的吸收使骨骼牙齒得以生長發育;膽固醇可在腎上腺皮質轉化為腎上腺皮質激素和性激素;膽固醇可在性腺轉化為性激素。另外,不飽和脂肪酸也是體內其他一些激素或活性物質的代謝前體,膽固醇也作為生物膜的結構成分出現。
脂類物質是貯存的能源物質、生物膜的結構成分和體內一些生理活性物質的代謝前體。
生物分子的功能分類
生物體體內的物質是多種多樣的,但可以從大的功能上劃分為三大類,即結構物質、能源物質和活性物質(功能物質)。
一、結構物質
結構物質是生物體各種結構的基礎,它們構成生物膜、細胞質骨架、各種細胞器、細胞核等結構,這些結構是細胞執行各種生命活動的場所。
(一)生物膜系統
生物膜系統包括細胞質膜(外周膜)、細胞質內各種細胞器包膜(如線粒體膜、葉綠體膜、內質網膜、溶酶體膜、高爾基體膜、過氧化物酶體膜)及核膜等。與真核細胞相比,原核細胞的內膜系統不很豐富,只有少量的膜結構,例如某些細菌的間,藍綠藻中進行光合作用的類囊體膜的。
生物膜結構是細胞結構的基本形式,它對細胞內很多生物大分子的有序反應和區域化提供了必須的結構基礎,從而使各個細胞器和亞細胞結構既各自有恆定、動態的內環境,又相互聯繫,相互制約,從而使整個細胞活動有條不紊、協調一致地進行。
生物膜系統主要由類脂、蛋白質和糖類3類分子構成,還有水、金屬離子等。
1.類脂有磷脂、膽固醇,膜的主體成分是磷脂。糖類與脂類複合構成糖脂,通常存在於膜的外表面,神經組織是含類脂比例最大的組織,尤以神經元為甚,因為神經元是多突起的細胞,膜/質比例很大。
膜的骨架是磷脂雙分子層。磷脂分子是一端親水一端疏水的分子,它們通過疏水端粘合、親水端指向外側構成雙分子層。膜的外側是親水的,膜中間是疏水的。膜內的磷脂分子位置是流動的,並不具有固定的位置,因此生物膜的物理狀態是介於液態和固態之間的一種狀態,既有類似於固體的相對穩定形狀,又具有液態分子的流動性。正因為此,膜上的所有分子都具有流動性。
2.膜蛋白。根據粗略計算,細胞中大約20%~25%的蛋白質是與膜結構相連的蛋白質,膜蛋白可根據它們在膜上的定位分為膜周邊蛋白質(表面蛋白)和膜內在蛋白質(鑲嵌蛋白質),這些蛋白質有些是酶,有些是支撐細胞外形的支撐蛋白,有些是受體,有些是離子通道。
3.在生物膜中,糖類的含量較少,其中多數分布在質膜上,約占質膜的2%~10%,內膜的含量相對較少。糖類在膜上通常與蛋白質和脂質複合,在質膜的外側形成一層多糖,即所謂的“糖被”,這在細胞膜尤其明顯。糖被與細胞識別、信息分子傳遞等相關,例如ABO血型物質、一些激素和活性物質(干擾素、霍亂菌素、促甲狀腺素、破傷風素、某些藥物等)的受體。
(二)細胞壁
植物細胞和細菌都存在細胞壁,動物細胞缺乏細胞壁。細胞壁的主要成分是多糖。
(三)細胞溶膠(細胞質基質、細胞漿)及核基質
細胞溶膠的成分複雜,含結構物質、功能物質和能源物質,其中起主要支撐定型作用的物質是蛋白質。
(四)細胞間質
細胞間質的主要成分是蛋白質和多糖,在結締組織尤為明顯。
機體的結構物質還有皮膚的角質層、肌腱、肌肉纖維、毛髮、角、甲等,這些結構的主體成分都是蛋白質。
二、能源物質
前已述及,體內的能源物質有糖、脂肪和蛋白質,其中糖類和脂肪是主要的能源物質,蛋白質亦可作為能源物質使用,但蛋白質的主要功能是活性物質(功能物質)和結構物質。
三、功能物質或活性物質
此類物質從化學組成上種類繁多,有蛋白質、脂類、糖類、核酸、維生素及其他化學物質,但可分為以下幾種類型。
(一)功能蛋白
諸如紅細胞中的血紅蛋白、肌肉細胞中的肌球蛋白和肌動蛋白、細胞間質的膠原蛋白和彈性蛋白、貯鐵蛋白、血漿中的轉運蛋白、膜上的轉運蛋白等,這些蛋白質有些既是功能蛋白又是結構蛋白。
(二)酶-生物催化劑
其化學本質是蛋白質,即具有催化能力的蛋白質。廣泛分布於各種細胞中,現已鑑定出4000多種酶,而且每年都有新酶被發現。生物機體是一個複雜的化學系統,細胞內絕大多數的化學反應都依賴酶的催化。
(三)細胞間信息物質
這類物質攜帶信息從而使機體細胞進行聯絡和溝通,調節機體生命活動。有激素、神經遞質、細胞因子等。從化學組成上分為3類,蛋白質及肽類、胺基酸類(胺基酸衍生物)、膽固醇類(甾醇類),某些細胞間信息物質還含有糖。
從產生細胞到靶細胞的傳輸距離上劃分,細胞間信息物質分為遠距離信息物質(激素)、旁細胞分泌的信息物質(細胞因子)和作用於自身細胞的自分泌信息物質(細胞因子)。
(四)細胞內信息物質
擔當細胞內信息傳遞的任務,這些物質有核苷酸類(如cAMP、cGMP)、糖類(如磷酸肌醇)、無機離子(如Ca2+)等。
(五)DNA和RNA
DNA和RNA是遺傳信息的載體,通過複製與細胞分裂將遺傳信息傳遞至子細胞和子代,通過表達途徑產生蛋白質和酶,全面調控細胞的新陳代謝。
需要注意的是,很多物質的功能不是單一的,而具有多種功能。例如細胞膜上的受體蛋白,它既是細胞膜的結構蛋白,又是功能蛋白,在細胞破解死亡後可作為其他細胞的能源物質;肌肉中的肌球蛋白和肌動蛋白既是結構蛋白,又是功能蛋白,在長期飢餓時,肌肉中的一部分蛋白質被動員,而被當作能源物質利用;同樣,酶是生物催化劑,蛋白質及胺基酸類激素是信息物質,它們降解後,也作為能源物質被利用。
生物元素
無機化合物簡稱無機物,指除碳氫化合物及其衍生物以外的一切元素及其化合物,如水、食鹽、硫酸等。絕大多數的無機物可以歸入氧化物、酸、鹼和鹽4大類。生物體中的無機物主要有水及一些無機離子,如Na+、K+、Ca2+、Mg2+、Cl-、HCO-3、SO42-、HPO42-等。
有機物是有機化合物的簡稱,所有的有機物都含有碳元素。但是並非所有含碳的化合物都是有機化合物,比如CO,CO2。除了碳元素外有機物還可能含有其他幾種元素。如H、N、S等。雖然組成有機物的元素就那么幾種(碳最重要),但到現在人類卻已經發現了超過1000萬中有機物。而它們的特性更是千變萬化。因此,有機化學是化學中一個相當重要的研究範疇。
有機物即碳氫化合物(烴)及其衍生物,簡稱有機物。除水和一些無機鹽外,生物體的組成成分幾乎全是有機物,如澱粉、蔗糖、油脂、蛋白質、核酸以及各種色素。過去誤以為只有動植物(有機體)能產生有機物,故取名“有機”。現在不僅許多天然產物可以用人工方法合成,而且可以從動植物、煤、石油、天然氣等分離或改造加工製成多種工農業生產和人民生活的必需品,象塑膠、合成纖維、農藥、人造橡膠等。與無機物相比,有機物的種類眾多,一般揮發性較大、熔點和沸點較低,反應較慢(較複雜)。溶於有機溶劑,且能燃燒。碳原子可用共價鍵彼此連線生成多種結構,組成數量巨大的不同種類的有機分子骨架。按照基本結構,有機物可分成3類:(1)開鏈化合物,又稱脂肪族化合物,因為它最初是在油脂中發現的。其結構特點是碳與碳間連線成不閉口的鏈。(2)碳環化合物(含有完全由碳原子組成的環),又可分成脂環族化合物(在結構上可看成是開鏈化合物關環而成的)和芳香族化合物(含有苯環)兩個亞類。(3)雜環化合物(含有由碳原子和其他元素組成的環)。在烴分子中,共價連線的碳原子是骨架,碳的其他鍵則與氫結合。烴骨架非常穩定,因為形成碳-碳單鍵和雙鍵的碳原子同等享用它們之間的電子對。烴的氫原子可以被不同的功能團(官能團)取代產生不同類的有機物。功能團決定分子的主要性質,所以有機物也常根據其功能團分類。有機生物分子的功能團比其烴骨架在化學上活潑得多,它們能改變鄰近原子的幾何形狀及其上的電子分布,從而改變整個有機分子的化學反應性。從有機分子中的功能團可以分析和推測其化學行為和反應。如酶(細胞的催化劑)可識別生物分子中的特殊功能團並催化其結構發生特徵性變化,大多數生物分子是多功能的,含有兩種或多種功能團。在這些分子中,每種類型的功能團有其自己的化學特徵和反應。如胺基酸具有至少兩種功能團——氨基和羧基。丙氨酸的化學性質就基本決定於其氨基和羧基。又如葡萄糖也是多功能的生物分子,其化學性質基本決定於羥基和醛基兩種功能團。生物分子的功能團在其生物活性中起著重要的作用。
例如甲烷分子式CH4。最簡單的有機化合物。甲烷是沒有顏色、沒有氣味的氣體,沸點-161.4℃,比空氣輕,它是極難溶於水的可燃性氣體。甲烷和空氣成適當比例的混合物,遇火花會發生爆炸。化學性質相當穩定,跟強酸、強鹼或強氧化劑(如KMnO4)等一般不起反應。在適當條件下會發生氧化、熱解及鹵代等反應。
甲烷在自然界分布很廣,是天然氣、沼氣、坑氣及煤氣的主要成分之一。它可用作燃料及製造氫、一氧化碳、炭黑、乙炔、氫氰酸及甲醛等物質的原料。
413kJ/mol、109°28′,甲烷分子是正四面體空間構型,上面的結構式只是表示分子裡各原子的連線情況,並不能真實表示各原子的空間相對位置。
生物單分子
生物單分子是指一些與生命有著密切關係的有機低相對分子量化合物,包括胺基酸、脂肪酸、糖、嘌呤、嘧啶、單核苷酸、卟啉、ATP等高能化合物。它們是構成生物高分子的基本成分。
生物大分子
像胺基酸、脂肪酸等都叫做生物單分子,是與生命有著密切關係的物質,它們是構成大分子的基本物質。生物大分子是構成生命的基礎物質,包括蛋白質、核酸、碳氫化合物等。生物大分子指的是作為生物體內主要活性成分的各種分子量達到上萬或更多的有機分子。常見的生物大分子包括蛋白質、核酸、脂質、糖類。
這個定義只是概念性的,與生物大分子對立的是小分子物質(二氧化碳、甲烷等)和無機物質,實際上生物大分子的特點在於其表現出的各種生物活性和在生物新陳代謝中的作用。
比如:某些多肽和某些脂類物質的分子量並未達到驚人的地步,但其在生命過程中同樣表現出了重要的生理活性。與一般的生物大分子並無二致。
生物大分子大多數是由簡單的組成結構聚合而成的,蛋白質的組成單位是胺基酸,核酸的組成單位是核苷酸……
生物大分子都可以在生物體內由簡單的結構合成,也都可以在生物體內經過分解作用被分解為簡單結構,一般在合成的過程中消耗能量,分解的過程中釋放能量。
高相對分子量的生物有機化合物(生物大分子)主要是指蛋白質、核酸以及高相對分子量的碳氫化合物。與低相對分子量的生物有機化合物相比,高相對分子量的有機化合物具有更高級的物質群 。它們是由低相對分子量的有機化合物經過聚合而成的多分子體系。從化學結構而言,蛋白質是由α-L-胺基酸脫水縮合而成的,核酸是由嘌呤和嘧啶鹼基,與糖D-核糖或2-脫氧-D-核糖)、磷酸脫水縮合而成,多糖是由單糖脫水縮合而成。由此可知,由低相對分子量的生物有機化合物變為高相對分子量的生物有機化合物的化學反應都是脫水縮合反應。
在原始地球條件下,有兩條路徑可以達到脫水縮合以形成高分子:其一是通過加熱,將低相對分子量的構成物質加熱使之脫水而聚合;其二是利用存在於原始地球上的脫水劑來縮合。前者常常是在近於無水的火山環境中進行,後者則可以在水的環境中進行。
生物大分子是生物體的重要組成成份,不但有生物功能,而且分子量較大,其結構也比較複雜。在生物大分子中除主要的蛋白質與核酸外,另外還有糖、脂類和它們相互結合的產物。如糖蛋白、脂蛋白、核蛋白等。它們的分子量往往比一般的無機鹽類大百倍或千倍以上。蛋白質的分子量在一萬至數萬左右,核酸的分子量有的竟達上百萬。這些生物大分子的複雜結構決定了它們的特殊性質,它們在體內的運動和變化體現著重要的生命功能。如進行新陳代謝供給維持生命需要的能量與物質、傳遞遺傳信息、控制胚胎分化、促進生長發育、產生免疫功能等等。
生物大分子是生物體的重要組成成份,不但有生物功能,而且分子量較大,其結構也比較複雜。在生物大分子中除主要的蛋白質與核酸外,另外還有糖、脂類和它們相互結合的產物。如糖蛋白、脂蛋白、核蛋白等。它們的分子量往往比一般的無機鹽類大百倍或千倍以上。蛋白質的分子量在一萬至數萬左右,核酸的分子量有的竟達上百萬。這些生物大分子的複雜結構決定了它們的特殊性質,它們在體內的運動和變化體現著重要的生命功能。如進行新陳代謝供給維持生命需要的能量與物質、傳遞遺傳信息、控制胚胎分化、促進生長發育、產生免疫功能等等。
人類對生物大分子的研究經歷了近兩個世紀的漫長歷史。由於生物大分子的結構複雜,又易受溫度、酸、鹼的影響而變性,給研究工作帶來很大的困難。在20世紀末之前,主要研究工作是生物大分子物質的提取、性質、化學組成和初步的結構分析等。
19世紀30年代以來,當細胞學說建立的時候,有人已經研究蛋白質了。蛋白質命名始於1836年,當時著名的瑞典化學家柏爾采留斯(J.Berzelius)和正在研究雞蛋蛋白類化合物的荷蘭化學家穆爾德(G.J.Mulder)就提出用“蛋白質”命名這類化合物。並且把它列為生命系統中最重要的物質。到本世紀初,組成蛋白質的20種胺基酸已被發現了12種,1940年陸續發現了其餘的胺基酸。19世紀末,有機化學家們就開始探討蛋白質的結構。德國有機化學家費舍爾(E.Fischer)與別人合作提出了胺基酸之間的肽鍵相連線而形成蛋白質的論點,1907年費舍爾又合成了一個由15個甘氨酸和3個亮氨酸組成的18個肽的長鏈。同時英國晶體分析學派中的貝爾納(J.D.Bernal)和阿斯特伯理(W.T.Astbury)等曾用X射線衍射分析方法分析羊毛、頭髮等蛋白的結構,證明它們是摺疊捲曲纖維狀物質。隨著研究的逐步深入,科學家們搞清了蛋白質是肌肉、血液、毛髮等的主要成份,有多方面的功能。
核酸的發現要比蛋白質晚得多。1868年在德國工作的24歲的瑞士化學家米歇爾(F.Miescher)從病人傷口膿細胞中提取出當時稱為“核質”的物質。這就是被後來公認的核酸的最早發現。後來科賽爾(A.Kssel)及他的兩個學生瓊斯(W.Jones)和列文(P.A.Levene)弄清了核酸的基本化學結構,證實核酸是由許多核苷酸組成的大分子。核苷酸是由鹼基、核糖和磷酸構成。其中鹼基有4種(腺瞟呤、鳥瞟呤、胞嘧啶和胸腺嘧啶),核糖有2種(即核糖與脫氧核糖)。據此核酸分成兩類:核糖核酸(RNA)和脫氧核糖核酸(DNA)。他們根據當時比較粗糙的分析認為,4種鹼基在核酸中的量相等,從而錯誤地推導出核酸的基本結構是由4個含不同鹼基的核苷酸連線成四核苷酸,以此為基礎聚合成核酸,這就是較著名的“四核苷酸假說”。這個假說從20年代後起統治了核酸結構的研究大約20多年的時間,對認識複雜的核酸結構和功能起了相當大的阻礙作用。核酸當時雖然是在細胞核中發現的,但由於它的結構過於簡單,也就很難想像它能在異常複雜多變的遺傳現象中起什麼作用。甚至有些科學家在當時蛋白質的結構被闡明之後,認為很可能是蛋白質在遺傳中起主要作用。
酶的闡明是1897年德國化學家布希納(E.Buchner)從磨碎的酵母細胞中提取出了能使酒精發酵的釀酶開始的。布希納研究表明,從活體內提取出來的酶能同在活體內一樣起作用。不但打擊了當時流行的活力論,而且使生物化學的研究進入了解細胞內的化學變化的階段。後來英國的生物化學家哈登(A.Harden)等對酒精發酵的具體化學步驟作了許多研究。到20年代大量實驗結果表明,酵母使糖發酵產生酒精同肌肉收縮時使糖變為乳酸這兩個過程基本上是一致的,又稱糖酵解作用。到30年代經許多科學家的研究,最後由德國的生物化學家克雷布斯(H.A.Krebs)綜合,提出了生物呼吸作用最後產生CO2和H2O及能量(ATP)的三羧酸循環。在此期間還有許多科學家研究了脂肪和胺基酸等的代謝以及糖、脂肪及蛋白質在代謝中相互轉化和它們的生物合成等。這些過程均是在酶的催化下完成的。
生物大分子衍射技術
生物大分子相對分子質量至少在5000以上,甚至超過百萬的生物學物質,如蛋白質、核酸、多糖等。它與生命活動關係極為密切,由被認為單體的簡單分子單位所組成。在溶液中有形成凝膠的物質。一般把相對分子質量超過一萬的化合物稱為大分子化合物或高分子化合物。它是由許多重複的結構單元組成,一般具有線狀結構,有的具有枝狀結構。許多具有重要生物作用的物質,如蛋白質和核酸等均屬於這類化合物。?
大分子蛋白質的基本組成單位或構件分子(building-block molecule)是胺基酸(amino acid,AA)
從衍射花樣(衍射線的方向和強度)推算生物大分子的三維結構(也常稱空間結構、立體結構或構象)的技術。其主要原理是 X射線、中子束或電子束通過生物大分子有序排列的晶體或纖維所產生的衍射花樣與樣品中原子的排布規律有可相互轉換的關係(互為傅立葉變換)。
X 射線衍射技術能夠精確測定原子在晶體中的空間位置,是迄今研究生物大分子結構的主要技術。中子衍射和電子衍射技術則用來彌補X射線衍射技術之不足生物大分子單晶體的X射線衍射技術是50年代以後,首先從蛋白質的晶體結構研究中發展起來的,並於70年代形成一門晶體學的分支學科──蛋白質晶體學。生物大分子單晶體的中子衍射技術用於測定生物大分子中氫原子的位置,也屬蛋白質晶體學。纖維狀生物大分子的X射線衍射技術用來測定這類大分子的一些周期性結構,如螺鏇結構等。以電子衍射為原理的電子顯微鏡技術能夠測定生物大分子的大小、形狀及亞基排列的二維圖象。它與光學衍射和濾波技術結合而成的三維重構技術能夠直接顯示生物大分子低解析度的三維結構。
歷史回顧 1912年德國物理學家 M.von勞厄預言晶體是 X射線的天然衍射光柵。此後英國物理學家W.H.布格和W.L.布格開創了X射線晶體學。幾十年來,這門學科不斷發展和完善,測定了成千上萬個無機和有機化合物的晶體和分子結構。由它提供的結構資料已經成為近代結構化學的基礎。但是傳統的小分子晶體結構的分析方法不適用於原子數目多,結構複雜的生物大分子。直到1954年英國晶體學家等人提出在蛋白質晶體中引入重原子的同晶置換法之後,才有可能測定生物大分子的晶體結構。1960年英國晶體學家J.C.肯德魯等人首次解出一個由153個胺基酸組成、分子量為17500的蛋白質分子──肌紅蛋白的三維結構。圖1 [巨頭鯨肌紅蛋白分子的結構模型]表示它的 2埃解析度的結構模型。此後生物大分子晶體結構的研究工作迅速發展。至80年代初,已有近 200個、等生物大分子的三維結構被測定,從而有力地推動了分子生物學的發展。中國繼60年代首次人工合成牛胰島素之後,於70年代初測定了三方二鋅豬胰島素的三維結構。1986年中國已經完成這個結構1.2埃高解析度的修正工作。
晶體和X射線衍射 電磁波是直線傳播的,但在某些情況下也會拐彎,這就是衍射現象。當可見光通過針孔或狹縫時,就會出現這種現象。由於針孔或狹縫的大小和可見光的波長量級相同,可以把針孔或狹縫看做是一個點光源,它向四面八方輻射出二次電磁波,或稱散射波。如果有多個有序排列的針孔或狹縫,由於這些散射波的干涉,就會形成規則的明暗相間的衍射花樣。這是因為來自不同部位的散射波的相位及振幅不同,它們相加的結果在有些地方加強,而在另一些地方減弱。這些花樣隨波長或針孔的大小及其排布方式不同而變化(圖2[三種針孔的排列方式及其對應的衍射花樣])。當X射線通過晶體時,晶體內原子的核外電子能夠散射X射線。如果把每個原子看成是個散射源,由於X射線的波長同原子間的距離量級相同,因此也會發生衍射現象。晶體結構的特徵是晶體內的原子或分子周期重複地排列。如果採用一組抽象的幾何點來表示這種周期重複的規律,那么這種排列可以表示為點陣。晶體的三維點陣結構使得晶體可被劃分成為無數個大小和形狀完全相同的平行六面體,即被稱為晶胞。它是晶體結構的基本重複單位。每個晶胞內包含種類、數目和排列完全相同的原子。可以推得,衍射線(也稱反射線)的強度取決於晶胞的內容,它的方向取決於波長和晶胞的大小和形狀。
晶體結構測定晶體對X射線、中子束及電子束的衍射,與規則排列的針孔對可見光的衍射遵循相同的光學變換原理,即針孔或晶體的結構(針孔或晶體中原子的排列)經傅立葉變換,可以得到它們的倒易圖像──衍射波譜。反之,衍射波譜的反變換,即為正空間的圖像──針孔的排列或晶體的結構。在可見光的衍射中,這種反變換可由透鏡的聚焦過程實現。但是迄今為止,人們還未找到能使 X射線(或中子)散射線聚焦的辦法。因此也就無法直接觀察生物大分子的像。這只能藉助電子計算機從數學上完成這種反變換的計算。
生物高分子
生物高分子一般是指自然界生物體內的高分子。生物高分子及其衍生物是一類重要的生命物質,協助生命體實現著許多重要的生理功能。
生物高分子種類豐富,特性多樣,根據其不同的化學結構可以分為八大類:①核酸,如脫氧核糖核酸、核糖核酸;②聚醯胺,如蛋白質、聚胺基酸;③多糖,如纖維素、澱粉、殼聚糖和黃原膠;④有機聚氧酯,如聚羥基脂肪酸酯;⑤聚硫酯;⑥無機聚酯,以聚磷酸酯為惟一代表;⑦聚異戊二烯,如天然橡膠或古塔波膠;⑧聚酚,如木質素、腐殖酸。
與傳統化學工業中的合成高分子相比,生物高分子具有許多誘人的特性和奇妙的功能。生物高分子可以特異性地與許多物質、材料發生相互作用,表現出極強的親和性;生物高分子具有很高的強度;生物高分子通常是生物可降解的;生物高分子來源於生物體,在工業上套用可以實現可持續性。正因為如此,生物高分子的開發與套用已成為各國生物技術領域和高分子材料領域研究的熱點。
生物靶分子Biotarget molecule
外源性物質進入生物體後進攻並與之結合的生物大分子(如蛋白質,脫氧核糖核酸)。生物體是一複雜體系,進入體內的外源性物質可以遇到各種不同的生物分子,與何者結合除與物質的結構有關還與熱力學和動力學等因素有關。
DNA分子
DNA即脫氧核糖核酸(英文Deoxyribonucleic acid的縮寫),又稱去氧核糖核酸,是染色體的主要化學成分,同時也是組成基因的材料。有時被稱為“遺傳微粒”,因為在繁殖過程中,父代把它們自己DNA的一部分複製傳遞到子代中,從而完成性狀的傳播。原核細胞的染色體是一個長DNA分子。真核細胞核中有不止一個染色體,每個染色體也只含一個DNA分子。不過它們一般都比原核細胞中的DNA分子大而且和蛋白質結合在一起。DNA分子的功能是貯存決定物種性狀的幾乎所有蛋白質和RNA分子的全部遺傳信息;編碼和設計生物有機體在一定的時空中有序地轉錄基因和表達蛋白完成定向發育的所有程式;初步確定了生物獨有的性狀和個性以及和環境相互作用時所有的應激反應.除染色體DNA外,有極少量結構不同的DNA存在於真核細胞的線粒體和葉綠體中。DNA病毒的遺傳物質也是DNA,極少數為RNA.
DNA分子就是帶有以上特徵結構的分子。DNA結構的發現是科學史
DNA結構的發現是科學史上最具傳奇性的“章節”之一。發現DNA結構是劃時代的成就,但發現它的方法是模型建構法,模型建構法就像小孩子拼圖遊戲一樣的“拼湊”法。而在這場“拼湊”中表現最出色的是沃森和克里克。
1928年4月6日,沃森出生於美國芝加哥。16歲就在芝加哥大學畢業,獲得動物學學士學位,在生物學方面開始顯露才華。22歲時取得博士學位,隨後沃森來到英國劍橋大學的卡文迪什實驗室,結識了早先已在這裡工作的克里克,從此開始了兩人傳奇般的合作生涯。克里克於1916年6月8日生於英格蘭的北安普敦,21歲在倫敦大學畢業。二戰結束後,來到劍橋的卡文迪什實驗室,克里克和沃森一樣,對DNA有著濃厚的興趣,從物理學轉向研究生物學。
當時人們已經知道,DNA是一種細長的高分子化合物,由一系列脫氧核苷酸鏈構成,脫氧核苷酸又是由脫氧核糖、磷酸和含氮鹼基組成,鹼基有4種。在1951年,很多科學家對DNA的結構研究展開了一場競賽。當時有兩個著名的DNA分子研究小組,一個是以著名的物理學家威爾金斯和化學家富蘭克林為首的英國皇家學院研究小組,他們主要用X射線衍射來研究DNA結構。一個是以著名化學家鮑林為首的美國加州理工大學研究小組,他們主要用模型建構法研究DNA結構,並且已經用該方法發現蛋白質a螺鏇。
1951年2月,威爾金斯將富蘭克林拍的一張非常精美的DNA的X光衍射照片在義大利舉行的生物大分子結構會議上展示,一直對DNA有濃厚興趣的沃森看到這張圖時,激動得話也說不出來,他的心怦怦直跳,根據此圖他斷定DNA的結構是一個螺鏇體。他打定主意要製作一個DNA模型。他把這種想法告訴了他的合作者克里克,得到了克里克的認可。
沃森和克里克構建DNA分子結構模型的工作始於1951年秋。他們用模型構建法,仿照著名化學家鮑林構建蛋白質α螺鏇模型的方法,根據結晶學的數據,用紙和鐵絲搭配脫氧核苷酸。
他們構建了一個又一個模型,都被否定了。但沃森堅持認為,DNA分子可能是一種雙鏈結構。因為自然界中的事物,很多是成雙成對的,細胞中的染色體也是成對的。之後他們分別完成了以脫氧核糖和磷酸交替排列為基本骨架,鹼基排在外面的雙螺鏇結構(如圖一),和以脫氧核糖和磷酸交替排
列為基本骨架,鹼基排在內部,且同型鹼基配對的雙螺鏇結構(如圖二)。
1952年,生物化學家查伽夫訪問劍橋大學時向報導了他對人、豬、牛、羊、細菌和酵母等不同生物DNA進行分析的結果。查伽夫的結果表明,雖然在不同生物的DNA之間,4種脫氧核苷酸的數量和相對比例很不相同,但無論哪種物質的DNA中,都有A=T和G=C,這被稱為DNA化學組成的“查伽夫法則”。1952年7月,查伽夫訪問卡文迪什實驗室時,向克里克詳細解釋了A:T=G:C=1:1的法則。之後,克里克的朋友,理論化學家格里菲斯通過計算表明,DNA的4種脫氧核苷酸中,A必須與T成鍵,G必須與C成鍵。這與查伽夫法則完成一致。隨後,鮑林以前的同事多諾告訴沃森,A-T和G-C配對是靠氫鍵維繫的。以上這些工作,就成了沃森和克里克DNA分子模型中A—T配對、G—C配對結構的基礎。
至此,DNA模型已經浮現。2月28日,沃森用紙板做成4種鹼基的模型,將紙板粘到骨架上朝向中心配對,克里克馬上指出,只有兩條單鏈的走向相反才能使鹼基完善配對,這正好與X光衍射資料一致。完整的DNA分子結構模型完成於1953年3月7日。根據這個模型,DNA分子是一個雙螺鏇結構,每一個螺鏇單位包含10對鹼基,長度為34埃(1埃=10-10米)。螺鏇直徑為20埃。4月15日,沃森和克里克關於該模型的第一篇論文在《自然》(Nature)雜誌上發表。
DNA分子雙螺鏇結構模型的發現,是生物學史上的一座里程碑,它為DNA複製提供了構型上的解釋,使人們對DNA作為基因的物質基礎不再懷疑,並且奠定了分子遺傳學的基礎。DNA雙螺鏇模型在科學上的影響是深遠的。
生物鹼(alkaloid)
生物鹼為一類含氮的有機化合物,存在於自然界(一般指植物,但有的也存在於動物)。有似鹼的性質,所以過去又稱為贗鹼。大多數生物鹼均有複雜的環狀結構,氮素多包括在環內,具有光學活性。但也有少數生物鹼例外。如麻黃鹼是有機胺衍生物,氮原子不在環內;咖啡因雖為含氮的雜環衍生物,但鹼性非常弱,或基本上沒有鹼性;秋水仙鹼幾乎完全沒有鹼性,氮原子也不在環內……等。由於它們均來源於植物的含氮有機化合物,而又有明顯的生物活性,故仍包括在生物鹼的範圍內。而有些來源於天然的含氮有機化合物,如某些維生素、胺基酸、肽類,習慣上又不屬於“生物鹼",所以"生物鹼"一詞到現在還未有嚴格而確切的定義。
已知生物鹼種類很多,約在2,000種以上,有一些結構式還沒有完全確定。它們結構比較複雜,可分為59種類型。隨著新的生物鹼的發現,分類也將隨之而更新。由於生物鹼的種類很多,各具有不同的結構式,因此彼此間的性質會有所差異。
組成細胞的分子
基本:C、H、O、N(90%)大量:C、H、O、N、P、S、(97%)K、Ca、Mg
元素微量:Fe、Mo、Zn、Cu、B、Mo等
(20種)最基本:C,占乾重的48.4%,生物大分子以碳鏈為骨架
物質說明生物界與非生物界的統一性和差異性。
基礎水:主要組成成分;一切生命活動離不開水
無機物無機鹽:對維持生物體的生命活動有重要作用
化合物蛋白質:生命活動(或性狀)的主要承擔者/體現者
核酸:攜帶遺傳信息
有機物糖類:主要的能源物質
脂質:主要的儲能物質
一、蛋白質(占鮮重7-10%,乾重50%)
結構元素組成C、H、O、N,有的還有P、S、Fe、Zn、Cu、B、Mn、I等
單體胺基酸(約20種,必需8種,非必需12種)
化學結構由多個胺基酸分子脫水縮合而成,含有多個肽鍵的化合物,叫多肽。
多肽呈鏈狀結構,叫肽鏈。一個蛋白質分子含有一條或幾條肽鏈。
高級結構多肽鏈形成不同的空間結構,分二、三、四級。
結構特點由於組成蛋白質的胺基酸的種類、數目、排列次序不同,於是肽鏈的空間結構千差萬別,因此蛋白質分子的結構是極其多樣的。
功能○蛋白質的結構多樣性決定了它的特異性/功能多樣性。
1.構成細胞和生物體的重要物質:如細胞膜、染色體、肌肉中的蛋白質;
2.有些蛋白質有催化作用:如各種酶;
3.有些蛋白質有運輸作用:如血紅蛋白、載體蛋白;
4.有些蛋白質有調節作用:如胰島素、生長激素等;
5.有些蛋白質有免疫作用:如抗體。
備註○連線兩個胺基酸分子的鍵(—NH—CO—)叫肽鍵。
○各種蛋白質在結構上所具有的共同特點(通式):
1.每種胺基酸至少都含有一個氨基和一個羧基連同一碳原子上;
2.各種胺基酸的區別在於R基的不同。
○變性(熟雞蛋)&鹽析&凝固(豆腐)
計算○由N個aa形成的一條肽鏈圍成環狀蛋白質時,產生水/肽鍵N個;
○N個aa形成一條肽鏈時,產生水/肽鍵N-1個;
○N個aa形成M條肽鏈時,產生水/肽鍵N-M個;
○N個aa形成M條肽鏈時,每個aa的平均分子量為α,那么由此形成的蛋白質
的分子量為N×α-(N-M)×18;
二、核酸
一切生物的遺傳物質,是遺傳信息的載體,是生命活動的控制者。
元素組成C、H、O、N、P等
分類脫氧核糖核酸(DNA雙鏈)核糖核酸(RNA單鏈)
單體
成分磷酸H3PO4
五碳糖脫氧核糖核糖
含氮
鹼基A、G、C、TA、G、C、U
功能主要的遺傳物質,編碼、複製遺
傳信息,並決定蛋白質的合成將遺傳信息從DNA傳遞給
蛋白質。
存在主要存在於細胞核,少量線上粒
體和葉綠體中。甲基綠主要存在於細胞質中。吡羅紅
△每一個單體都以若干個相連的碳原子構成的碳鏈為基本骨架,由許多單體連線成多聚體。
三、糖類和脂質
元素類別存在生理功能
糖類C、H、O單糖核糖C5H10O5主細胞質核糖核酸的組成成分;
脫氧核糖C4H10O5主細胞核脫氧核糖核酸的組成成分;
六碳糖:葡萄糖
C6H12O6、果糖等主細胞質是生物體進行生命活動的重要能源物質(70%以上);
二糖
C12H22O11麥芽糖、蔗糖植物
乳糖動物
多糖澱粉、纖維素植物(細胞壁的組成成分),
重要的儲存能量的物質;
糖原(肝、肌)動物
脂質C、H、O
有的還有N、P脂肪動、植物儲存能量、維持體溫恆定;
類脂/磷脂腦、豆構成生物膜的重要成分;
固醇膽固醇動物動物的重要成分;
性激素促性器官發育和第二性徵;
維生素D促進鈣、磷的吸收和利用;
△組成生物體的任何一種化合物都不能夠單獨地完成某一種生命活動,而只有按照一定的方式有機地組織起來,才能表現出細胞和生物體的生命現象。細胞就是這些物質最基本的結構形式。
四、鑑別實驗
試劑成分實驗現象常用材料
蛋白質雙縮脲A:0.1g/mLNaOH紫色大豆
雞蛋
B:0.01g/mLCuSO4
脂肪蘇丹Ⅲ橘黃色花生
還原糖班氏(加熱)磚紅色沉澱蘋果、梨、白蘿蔔
澱粉碘液I2藍色馬鈴薯
○具有還原性的糖:葡萄糖、麥芽糖、果糖
五、無機物
存在方式生理作用
水
結合水4.5%
自由水95%部分水和細胞中
其他物質結合。細胞結構的組成成分。
絕大部分的水以
游離形式存在,可以自由流動。1.細胞內的良好溶劑;
2.參與細胞內許多生物化學反應;
3.水是細胞生活的液態環境;
4.水的流動,把營養物質運送到細胞,並把廢物運送到排泄器官或直接排出;
無機鹽多數以離子狀態存,如K+、
Ca2+、Mg2+、Cl--、PO2+等1.細胞內某些複雜化合物的重要組成部分,如Fe2+是血紅蛋白的主要成分;
2.持生物體的生命活動,細胞的形態和功能;
3.維持細胞的滲透壓和酸鹼平衡;
六、小結
化合有機組合分化
化學元素化合物原生質細胞
○原生質1.泛指細胞內的全部生命物質,但並不包括細胞內的所有物質,如細胞壁;
2.包括細胞膜、細胞質和細胞核三部分;其主要成分為核酸、蛋白質(和脂類);
3.動物細胞可以看作一團原生質。
○細胞質:指細胞中細胞膜以內、細胞核以外的全部原生質。
○原生質層:成熟的植物細胞的細胞膜、液泡膜以及兩層膜之間的細胞質,為一層半透膜。
