病因學
 成人呼吸窘迫綜合症
成人呼吸窘迫綜合症成人呼吸窘迫綜合徵(ARDS),這種常見的醫學急診,是由各種直接或間接損害肺臟的急性過程所促成的,如敗血症,原發性細菌或病毒性肺炎,吸入骨內容物,胸部直接外傷,持續或深度休克,燒傷,脂肪栓塞,溺水,大量輸血,體外循環,O2 中毒,急性出血性胰腺炎,煙或其他毒性氣體吸入和某些藥物的吸收,同時有敗血症的ARDS發病率估計在30%以上。儘管稱為"成人"呼吸窘迫綜合徵,但它同樣可以發生於兒童。
病理生理學
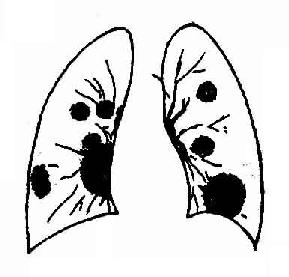 成人呼吸窘迫綜合症
成人呼吸窘迫綜合症對於最初的肺部損害,知之甚少。動物模型研究提示,活化的白細胞和血小板積聚於毛細血管,間質和氣腔內;它們可釋放前列腺素,毒性O2 原子團,蛋白溶解酶和其他介質(如腫瘤壞死因子和白細胞介素),這些物質損害細胞,促使炎症形成和纖維化,並改變支氣管舒縮性和血管反應性。
當肺毛細血管內皮和肺泡內皮受損時,血漿和血液逸漏至間質和肺泡腔內。導致肺泡積水和肺不張,肺不張部分是由於表面活性物質減少所致。這種損傷並非是均勻的,它主要發生在肺的下垂部位。2~3天內,出現間質和支氣管肺泡炎症以及上皮和間質細胞增生。然後,膠原迅速積聚,在2~3周內導致嚴重的間質纖維化。這些病理改變使肺順應性降低,功能殘氣量下降,通氣/灌注比例失調,生理死腔量增加,嚴重的低氧血症和肺動脈高壓。
症狀和診斷
 成人呼吸窘迫綜合症
成人呼吸窘迫綜合症ARDS通常在最初損傷或疾病的24~48小時後發生。首先出現呼吸困難,通常呼吸淺速。吸氣時可存在肋間隙和胸骨上窩凹陷。皮膚可出現發紺和斑紋,吸氧不能使之改善。聽診可聞及囉音,鼾音或哮鳴音,也可能正常。
早期診斷對發生於可能引起ARDS情況下的呼吸困難應予高度警惕。此時,通過立即測動脈血氣和胸部X線檢查可以作出推測性診斷。這種最初的血氣分析顯示急性呼吸性鹼中毒:PaCO2 正常或降低,PaO2 明顯降低,pH值升高。胸部X線通常顯示類似於急性心源性肺水腫的雙側瀰漫性肺泡浸潤,但心廓影通常正常。然而,X線改變常晚於功能改變許多小時,且比X線所見的肺水腫,低氧血症嚴重得多。儘管吸入高濃度O2 (FiO2 ),極度低氧血症仍常持續存在,表明由於肺部的不張和實變,使右向左分流,造成不能換氣。
在立即治療低氧血症以後,應作進一步診斷。當懷疑症狀是否由於心力衰竭所致時,Swan-Ganz導管可幫助鑑別。ARDS的特徵是肺動脈楔壓低下(PAWP<18mmHg),如果升高則是心力衰竭的表現(PAWP>20mmHg)。如考慮像肺栓塞,臨床表現了類似於ARDS 應在病人穩定後實行適當的診斷措施(如肺血管造影)。卡氏肺囊蟲肺炎和其他偶發的原發性肺感染可類似ARDS,應予考慮,尤其對免疫功能受損的病人,肺活檢或支氣管肺泡灌洗可能有幫助。
併發症和預後
 成人呼吸窘迫綜合症
成人呼吸窘迫綜合症繼發性肺部多重細菌感染,尤其是革蘭氏陰性細菌(如克雷白桿菌,假單孢菌和變形桿菌屬)和革蘭氏陽性菌金黃色葡萄球菌,尤其是耐甲氧西林菌株;多器官衰竭,尤其是腎功能衰竭;和有創性生命支持措施的併發症導致了高病殘率和高死亡率。與放置中心靜脈導管以及使用正壓通氣(PPV)和呼氣末正壓(PEEP)有關的張力性氣胸可突然發生。為防止死亡,需要迅速認識並治療張力性氣胸,心動過速,低血壓和機械通氣時吸氣峰壓突然增加均與張力性氣胸有關。在ARDS晚期發生的張力性氣胸是一種不詳的徵象,因為它往往由於嚴重的肺損傷和所需要的高的通氣壓氣所致。沒有足夠的血容量補充,PPV和PEEP所致靜脈回流減少使心排量降低,組織供氧減少,引起繼發性多臟器系統衰竭。
經適當治療的嚴重ARDS的生存率為60%。如ARDS嚴重的低氧血症未被認識和治療,90%的病人可發生心臟功能停止。治療很快見效的病人通常極少或不會殘留下肺功能不全。需要用FiO2 >50%長期通氣支持的病人常發生肺纖維化。在絕大多數嚴重急性病例中,可發現肺纖維化在數月之後消失,但其機制未明。
疾病概述
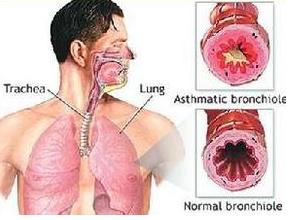 成人呼吸窘迫綜合症
成人呼吸窘迫綜合症成人呼吸窘迫綜合徵(adult respiratory distress syndrome )(簡稱ARDS)是患者原心肺功能正常,如嚴重創傷、燒傷、休克、感染、大手術等過程中繼發的一種以進行性呼吸窘迫和難以糾正的低氧血症為特徵的急性肺循環障礙性呼吸衰竭。臨床特點為進行性低氧血症和呼吸窘迫。本病多發生在原來無明顯肺部疾病的健康人,於多種肺內外因素造成急性肺部損傷後引起的肺順應性喪失,瀰漫性肺內浸潤性病變。
雖其病因各異,但肺組織損傷的病理和功能改變大致相同,臨床表現均為急性呼吸窘迫,難治性低氧血症,因其臨床類似嬰兒呼吸窘迫征,而它們的病因和發病機制不盡相同,故遂冠以“成人”,以示區別。
現在注意到本徵亦發生於兒童,故歐美學者協同討論達成共識,以急性(acute)代替成人(adult),稱為急性呼吸窘迫綜合徵,縮寫仍是ARDS。
疾病病因
病因甚多,如嚴重休克、嚴重創傷、骨折時脂肪栓塞、嚴重感染(特別是革蘭染色陰性桿菌敗血症所致的感染性休克)、吸入刺激性氣體和胃內容物、氧中毒、溺水、大量輸血、急性胰腺炎、藥物或麻醉品中毒等。
注意有無休克、嚴重感染、創傷、手術、補液過量、大量輸入陳血、誤吸胃液或溺水、藥物過量、吸入有毒氣體(如高濃度氧、氯氣等)、血液系統疾病、代謝性疾病及心臟病等病史。
病因和發病機制 引起ARDS的原發病或基礎病大致有以下幾種:
①休克。敗血性、出血性、過敏性休克。
②大的創傷、燒傷。非胸部外傷、挫傷、脂肪栓子。
③嚴重感染。細菌性或病毒性感染。
④中毒。吸入毒氣、N2O、高濃度氧。
⑤誤吸。誤吸胃液、淡水或海水。
⑥大量輸血感染。
⑦瀰漫性血管內凝血(DIC)。
⑧放射。
⑨其他。急性胰腺炎、尿毒症、妊娠中毒症、心臟轉復術後、心肺體外循環等。
儘管引起ARDS的基礎病多種多樣,但ARDS 時肺臟發生的病理生理改變大同小異,主要是肺毛細血管內皮細胞通透性增加,肺泡表面活性物質減少,最終造成肺間質和肺泡水腫及難以糾正的低氧血症。
症狀體徵
 成人呼吸窘迫綜合症
成人呼吸窘迫綜合症注意呼吸是否頻數(大於28次/min),有無發紺及胸部異常體徵。
臨床表現均為急性呼吸窘迫,難治性低氧血症,因其臨床類似嬰兒呼吸窘迫征,而它們的病因和發病機制不盡相同,故遂冠以“成人”,以示區別。本病起病急驟,發展迅猛,如不及早診治,其病死率高達50%以上(25%-90%),常死於多臟器功能衰竭。大手術後,嚴重創傷或其他危重疾病搶救過程中,或急性期已趨穩定幾個小時甚至幾天后逐漸出現呼吸困難,表現為呼吸淺而快。部分患者出現鼻翼扇動,吸氣三凹征。早期缺氧不明顯,病情嚴重時缺氧逐漸加重,而且用鼻導管吸氧難以糾正。早期體格檢查無異常體徵,晚期雙肺叩診濁音,並可聽到濕羅音。X射線檢查早期可正常或僅有肺紋理增粗,之後出現斑片狀陰影,逐漸擴展、融合形成大片實變。
除原發病如外傷、感染、中毒等相應症狀和體徵外,主要表現為突發性、進行性呼吸窘迫、氣促、紫紺、常伴有煩躁、焦慮表情、出汗等。其呼吸窘迫的特點不能用通常的療法使之改善,亦不能用其他原發心肺疾病(如氣胸、肺氣腫、肺不張、肺炎、心力衰竭)解釋。
起病急劇或隱藏,多發生於原發性疾病的搶救或醫治過程中。早期僅表現為原發疾病的症狀,而後感到胸悶、氣促、呼吸淺而頻繁,心跳增快,唇指紫紺, 漸感煩躁不安,呼吸困難。上述症狀呈進行性加重。呼吸頻率一般在30次/分以上,不能用原發疾病解釋。低氧血症經一般氧療難以緩解。
體徵:早期除原發病體徵外可無異常發現,有時可聽到乾性羅音或哮喘音;病情進展可見呼吸淺速,吸氣時肋間隙及鎖骨上窩下陷,唇指紫紺並逐漸加重。後期出現肺實質性變化體徵,雙肺呼吸音減低,並可聞及廣泛性的細濕性羅音。
診斷檢查
1、胸部X線檢查
兩肺有無肺紋理增加、斑片狀陰影或兩肺廣泛密度增加及呈“白肺”外觀;恢復期病變吸收可表現為網狀和線狀陰影,有時用X線可不留異常表現。
2、血氣分析
①PaO2:吸空氣小於8.0kPa(60mmHg),吸純氧小於46.5kPa(350mmHg);
②PA-aO2:吸空氣大於6.65kPa(50mmHg),吸純氧大於13.3kPa(100mmHg);
③PaO2/F1O2<40k Pa(300mmHg)診斷為急性肺損傷,而PaO2/F1O2<26.7kPa(200mmHg)則診斷為ARDS;
④PaCO2:早期降低,小於4kPa(30mmHg),晚期升高,大於6.0kPa(45mmHg)。
3、注意有無DIC情況
有條件時進行中心靜脈壓、Swan~Ganz導管檢查以測定混合靜脈血氧分壓和肺毛細血管楔壓以及靜動脈分流占總血流量百分數(Qs/Qt)]、血液膠體滲透壓監測等,了解心、肺及血液膠體情況。
4、排除慢性肺疾病、心源性肺水腫等疾病
可能引起ARDS的患者,當出現明顯呼吸困難和缺氧時應警惕ARDS,如果胸部X射線檢查及動脈血氣分析結果符合ARDS,並能除外造成肺水腫,缺氧的其他疾病,就可診斷為ARDS。
診斷依據
1.在休克、創傷、燒傷、嚴重感染、中毒等過程中出現非原發病引起的進行性呼吸困難和用一般吸氧方法難以糾正的低氧血症,呼吸頻率〉35次/分,早期肺部無異常體徵,後期可有肺實變體徵或水泡音等。
2.胸部X線表現:早期可無異常或有紋理增多,邊緣模糊。病情進展後出現斑片狀陰影,逐漸擴展形成大片實變。
3.血氣分析: 吸空氣時PaO2〈8.0KPa(60mmHg); 吸純氧15分鐘後,PaO2〈46.6KPa(350mmHg);PaCO2〈4.66KPa(35mmHg),後期PaCO2可高於正常; 分流率(Qs/Qt)〉10%。
4.肺泡氣-動脈血氧分壓差(P(A-a)O2)顯著增大。
5.必要時用漂浮導管測定肺楔壓(PCWP)以鑑別因左心衰所致的肺水腫,ARDS時PCWP不超過正常範圍(0.67-1.3kPa,即5~10mmHg)。具備以上1、2、3或1、3兩項者即可作出臨床診斷。本標準僅適用於在海拔不高地區居住的病人。
鑑別診斷
本病須與大片肺不張、自發性氣胸、上呼吸氣道阻、塞急性肺拴塞和心源性肺水腫相鑑別。通過詢問病史體檢和胸部x線檢查等可作出鑑別,心源性肺水腫患者臥位時呼吸困難加重、咳粉紅色泡沫樣痰、雙肺底有濕哆音。對強心利尿等治療效果較好;若有困難可通過測定PAwP超產心動閣檢查來鑑別。
治療
 成人呼吸窘迫綜合症
成人呼吸窘迫綜合症1.糾正缺氧:吸入50%以上濃度的氧,使PaO2維持在8kPa上。2.防止肺泡萎陷:機械通氣,予呼氣末正壓呼吸(PEEP)或持續正壓呼吸(cPAP)。3.改善肺微循環,如腎上腺皮質激素的套用。4.消除肺水腫:限制入水量,酌情使用利尿劑。5.積極治療原發病。
用藥原則: 1.積極治療原發病(抗感染、抗休克等)。2.套用腎上腺皮質激素,以早期、大量、短程為原則。3.在本病早期,血清蛋白濃度無明顯減少時,補液應以晶體為主。4.有低蛋白血症時,可補充白蛋白和血漿。5.創傷、出血過多、必須輸血。6.注意糾正酸鹼失衡、電解質紊亂。
應早期診斷和治療,措施包括:積極治療原發病(如控制感染、抗休克);實行機械通氣並使用呼氣末正壓,以糾正低氧血症;控制液體入量,保持液體負平衡,以解除肺水腫;使用α受體阻斷劑、低分子右鏇糖酐、腎上腺皮質激素學藥物改善微循環;及時發現並處理各種併發症,如消化道出血、急性肝腎功能衰竭、DIC、感染、心力衰竭、心律失常。
糾正低氧血症
(1)氧療:立即給氧並積極清除呼吸道分泌物,保持呼吸道濕化。吸空氣時PaO2<6.65kPa(50mmHg),吸氧時<9.3kPa(70mmHg)時,應進行氣管插管或氣管切開行機械通氣。
(2)機械通氣:先用間歇正壓通氣(IPPV),如吸氧濃度需50%才能使PaO2達理想水平時,應改用呼氣末期正壓通氣(PEEP)。IPPV吸氣末壓力一般用0.78~1.47kPa(8~15cmH2O),PEEP採用呼吸頻率20~30/min,吸氣壓約為3.7kPa(40cmH2O),呼氣末壓0.49~1.47kPa(5~15cmH2O)。應選擇最佳壓力以維持足夠的氧合及足夠的心排血量。慎防壓力過高引起氣胸和縱隔氣腫。
(3)高頻正壓通氣(HFPPV)、模式人工肺(ECMO):兩者療效均未完全肯定,且前者易引起CO2瀦留,後者可破壞血液的有形成分,故都只能在有心功能不全時短時間套用。
消除肺水腫
(1)早期套用大劑量糖皮質激素:地塞米松40mg,1次/6h,靜注,或甲基氫化潑尼松200~400mg,每6h一次,靜注。維持48~72h。
(2)改善微循環:①酚妥拉明5~10mg加入10%葡萄糖液500ml,靜滴,每12h一次,可擴張肺血管,降低肺楔壓,減輕肺淤血;②有DIC存在時可用肝素。
(3)保持液體平衡:①限止入量,保持水的負平衡(每日出量>入量500ml);②利尿劑套用:呋塞米40mg,每6h一次靜注;③強心劑套用;肺楔壓>3.3kPa(25mmHg)時應給予快速洋地黃製劑靜注;④低鹽白蛋白套用:療效可疑,多主張肺毛細血管通透性改善後再給予。
防治肺泡群不張
除使用PEEP可減少肺泡不張外,也可套用肺表面活性物質氣管內滴入或霧化吸入,以改善和減少肺泡群不張,進而增加通氣量,改善低氧血症。
注意各臟器功能衰竭的防治療
積極進行病因治療
併發症
急性呼吸窘迫綜合徵:患者病後不久數天或數周后病情未得緩解時,可由於氧供不足引起。出現其他器官的併發症:缺氧時間過長可引起嚴重的併發症,如腎功能衰竭,如未獲及時治療可因嚴重缺氧而死亡。由於急性呼吸窘迫綜合徵患者防禦肺部感染的能力低下,在其患病過程中常常出現細菌性肺炎。
預防常識
對高危的患者應嚴密觀察,加強監護,當發現呼吸頻速,PaO2降低等肺損傷表現,應早期給予呼吸支持和其它有效的預防及干預措施,防止ARDS進一步發展和重要臟器損傷。
預後注意
ARDS的預後除與搶救措施是否得當有關外,常與患者原發病、併發症以及對治療的反應有關。如嚴重感染所致的敗血症得不到控制,則預後極差。骨髓移植並發ARDS死亡率幾乎100%。經積極治療後,若持續肺血管阻力增加,示預後不良。脂肪栓塞引起的ARDS,經積極處理,機械通氣治療可獲得90%存活。刺激性氣體所致的急性肺水腫和ARDS,一般脫離現場,治療及時,亦能取得較好的療效。ARDS能迅速得到緩解的病人,大部分能恢復正常。
