 急性雜合性白血病
急性雜合性白血病急性雜合性白血病(hybrid acute leukemia,HAL)又稱急性混合細胞白血病(acute mixed leukemia),是一種髓細胞系和淋巴細胞系共同受累且達到一定積分的急性白血病。該病與髓系抗原表達的急性淋巴細胞白血病(MY+ALL)和淋系抗原表達的急性髓系白血病(LY+AML)不同,是一種少見的具有獨特臨床及生物學特徵的急性白血病。隨著免疫標記及遺傳學技術的不斷發展,其發病率有增高趨勢,占急性白血病3%~20%本病臨床可見程度不等的貧血感染、出血及浸潤表現,治療療效差預後不佳。
流行病學
是一種少見類型的白血病,發病率有增高趨勢占急性白血病的3%~20%。
病因
 基因表達
基因表達人類白血病的確切病因至今未明。許多因素被認為和白血病發生有關。病毒可能是主要因素此外尚有電離輻射、化學毒物或藥物遺傳因素等。
1.病毒 已證實雞小鼠貓、牛和長臂猿等動物的自發性白血病組織中可分離出白血病病毒為一種反轉錄病毒在電鏡下大多呈C型人類白血病的病毒病因研究已有數十年歷史但至今只有成人T細胞白血病肯定是由病毒引起的1976年日本高月清首先報導成人T細胞白血病或淋巴瘤(ATL),以後的流行病學調查發現在日本西南部加勒比海區域及中部非洲為高發流行區。1980年在ATL細胞系中發現ATL相關抗原並在電鏡下發現了病毒顆粒。美國Gallo和日本的日昭賴夫分別從病人培養細胞株中分離出C形反轉錄RNA病毒分別命名為HTLV-Ⅰ和ATLV以後證實二者是一致的這是對人類白血病病毒病因研究的重大貢獻。ATL高發區也是HTLV-Ⅰ感染的高發區。HTLV-Ⅰ具有傳染性可通過乳汁母嬰傳播,通過性交和輸血傳播其他病毒如HTLV-Ⅱ和毛細胞白血病,EB病毒和ALL-L3亞型的關係尚未完全肯定其他類型白血病尚無法證實其病毒病因,並不具有傳染性。
2.電離輻射 電離輻射有致白血病作用其作用與放射劑量大小和照射部位有關一次大劑量或多次小劑量照射均有致白血病作用全身照射特別是骨髓受到照射,可致骨髓抑制和免疫抑制,照射後數月仍可觀察到染色體的斷裂和畸變1945年日本廣島和長崎遭核子彈襲擊後倖存者中發生白血病數較未輻射地區高30倍和17倍放射治療強直性脊柱炎和32P治療真性紅細胞增多症,白血病發生率均較對照組為高。據我國1950~1980年調查,臨床X線工作者白血病發病率9.61/10萬(標化率9.67/10萬)而其他醫務人員為2.74/10萬(標化率2.77/10萬)放射可誘發急性非淋巴細胞白血病(ANLL)急性淋巴細胞白血病(ALL)和慢性粒細胞白血病(CML),並且發病前常有一段骨髓抑制期,其潛伏期為2~16年。診斷性照射是否會致白血病尚無確切的根據但孕婦胎內照射可增加出生後嬰兒發生白血病的危險性。
3.化學物質 苯致白血病作用比較肯定苯急性白血病以急粒和紅白血病為主。苯致慢性白血病主要為CML。烷化劑和細胞毒藥物可致繼發性白血病也較肯定多數繼發性白血病是發生在原有淋巴系統惡性腫瘤和易產生免疫缺陷的惡性腫瘤經長期烷化劑治療後發生髮病間隔2~8年化療引起的繼發性白血病以ANLL為主且發病前常有一個全血細胞減少期近年來國內陸續報導乙雙嗎啉致繼發性白血病近百例,該藥用於治療銀屑病是一種極強的致染色體畸變物質,服乙雙嗎啉後1~7年發生白血病。
4.遺傳因素 某些白血病發病與遺傳因素有關。單卵雙胎如一人患白血病另一人患白血病的機會為20%。家族性白血病占白血病例總數0.7%,偶見先天性白血病某些遺傳性疾病常伴較高的白血病發病率包括DownBloom、Klinefelter、Fanconi和Wiskott-Aldrich綜合徵等,如Down綜合徵急性白血病發生率比一般人群高20倍。上述多數遺傳性疾患具有染色體畸變和斷裂但極大多數白血病不是遺傳性疾病。
發病機制
綜合以往研究資料與AML或ALL發病機制不同之處在於:①系早期造血細胞惡性變所致因本病患者造血乾、祖細胞標誌性抗原CD34高表達;部分患者因髓性白血病細胞存在TdT一種來源於B、T和白血病淋巴細胞的核苷酶表明患者可能存在含早期分化相關抗原的多能幹細胞受累;②因某些內在或外在因素導致細胞分化異常而發生髓系或淋系系列轉化。
臨床表現
本病各年齡組均可發病具有貧血、出血、感染及浸潤等白血病常見臨床特徵但與AML或ALL相比,以下表現更為突出:①發病時白細胞增高者較多,高白細胞綜合徵較易見;②髓外浸潤表現明顯,如睪丸、中樞神經系統受累肝、脾淋巴結腫大者較多見;③多種標準治療方案無效復發率高,療效差。
併發症:
1.感染、發熱是常見的併發症 可以出現肺部感染皮膚黏膜感染等。
2.並發中樞神經系統白血病 表現為顱內壓增高顱內出血,腦實質受壓及腦神經麻痹。
3.並發睪丸白血病 可表現為無痛性腫大、局部變硬、可呈結節狀、陰囊皮膚色澤改變等。
4.此類型白血病白細胞增高者多,易合併高細胞綜合徵。
診斷
 表2
表21.診斷標準 1987年Gale和Ben-Bassat提出了HAL診斷標準主要是使用細胞化學形態學(Auers小體)、免疫學及免疫球蛋白重鏈基因重排和T細胞受體基因重排等技術近來國內外均採用白血病免疫學特徵歐洲協作組(European group of immunological characterization of leukemia,EGIL)1994年制定的HAL診斷標準(表2)診斷雙表型必須有一個細胞同時表達髓系及淋系標誌。
需指出的是,僅異常表達個別次要非本系列相關抗原者不能診斷HAL而應診斷為伴有淋巴細胞系相關抗原陽性的急性髓系白血病(Ly+AML)或伴髓系相關抗原陽性的急性淋巴細胞白血病(MY+ALL)。
2.HAL分型 HAL分類尚未統一目前可根據受累細胞來源與免疫表達不同分為4種不同類型:
(1)雙表型(biphentypic):白血病細胞較均一,患者白血病細胞同時表達髓細胞系和淋巴細胞系特徵即單個白血病細胞同時表達髓系和淋巴細胞系組織化學及免疫標記特徵且細胞計數≥10%.
(2)雙克隆型(biclonic)亦稱雙細胞系型(bilineal):白血病細胞具有不均一性其中一部分白血病細胞表達髓系特徵另一部分則表達淋系特徵二類細胞分別來源於各自多能幹細胞。需限定只有當二類細胞並存,或在半年內相繼發生,方屬此型。
(3)雙系列型(bilined):與雙克隆型類似但這兩類細胞來源於同一多能幹細胞。
(4)系列轉變型(1ineal switch):指白血病細胞由一種表現型轉變為另一表現型(病程多在半年以上發生轉變)白血病化療可能是導致系列轉化(如淋系→髓系,或髓系→淋系)最重要因素之一。
鑑別診斷:
主要是根據細胞免疫標記及基因分型來加以鑑別。
檢查
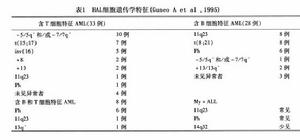 表1
表1實驗室檢查
:1.外周血 血紅蛋白下降明顯,多為中~重度,白細胞增高者(WBC>10×109/L)較多見多數患者發病時可見血小板減少血塗片可見白血病細胞較均一,類似於AML或ALL原始和幼稚細胞形態特徵:白血病細胞亦可不均一,即外周血視野分別存在粒細胞樣和淋巴細胞樣原始及幼稚細胞。
2.骨髓象及化學染色特徵 根據形態學及細胞化學染色常將本病診斷為AML或ALL文獻曾報導18例HAL患者根據FAB分型標準,其中9例診斷為AML(M11例;M24例;M41例;M53例)另9例則診斷為ALL(L13例和L26例)。骨髓細胞形態學發現白血病細胞可為均一性或不均一性,呈現髓系和(或)淋系特徵,部分病例可見Auers小體國內曾報導5例HAL患者,其化學染色特徵為:4例POX陽性1例陰性;5例PAS均有不同程度陽性;4例NAS-D-AE陽性,加NaF後1例被抑制,該4例同時查NAS-D-CE,僅1例陽性。
3.細胞免疫標記 可採用免疫組化和流式細胞儀檢測迄今,流式細胞術已廣泛套用於臨床以檢測HAL的免疫標記如T淋巴細胞以CD3最為特異,特別是胞質CyCD3先於膜表達(MCD3);CyCD22現認為是B-ALL最敏感的標誌在AML均未見CyCD22表達近來發現CD20是B-ALL較可靠的表達之一,而抗MPO則是髓系最可靠的標誌之一此外CD13和CD33也是粒細胞系一線診斷標誌。
4.細胞遺傳學 本病細胞遺傳學變化較為複雜較常出現的染色體改變有:t(9;22)、-5/5q-inv(16)11q23、t(8;21)等。Cuneo等回顧性分析HAL染色體變異資料(表1)發現t(15;17)inv(16)及-5/5q-和/或-7/7g-常見於含T淋巴細胞特徵的AML,T(8;21)(q22;q22)t(q;22)及11q23重排多見於含B淋巴細胞特徵的AML,而t(9;22)、tllq23和14q32(無免疫球蛋白重鏈基因重排)則見於含髓系標誌的ALL。
其它輔助檢查:
根據臨床表現、症狀體徵選擇胸片、CT、MRI、B超心電圖等檢查
治療
1.加強支持療法 輸血血小板、套用細胞因子、抗感染
2.DAPTO方案誘導治療
3.DA方案。
4.採用難治和復發的AL的治療方案
5.骨髓移植。
預後
HAL預後不佳可能與免疫標記有一定的關係,資料表明伴低分化細胞相關抗原CD34、HCL或CD7表達者對治療反應差,含CD4+患者預後亦較差同時CD14+和CD7+ 同時出現者預後更差,研究表明,HCL染色體對預後有較大的影響。如有pH染色體,11q23重排及+13者,均預後不良而t(4;11)則被認為與白血病細胞,脾大及預後不良有關。
