基本介紹
解離常數是現代詞,是一個專有名詞,指的是解離常數(pK)是水溶液中具有一定離解度的溶質的的極性參數。離解常數給予分子的酸性或鹼性以定量的量度,pKa減小,對於質子給予體來說,其酸性增加;對於質子接受體來說,其鹼性增加。
性質
pKa是Ka的負對數。Ka越大,pKa越小。
pH=pK+lg(電子受體/電子供體)
相當於化學中的解離常數。
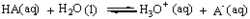 解離常數
解離常數1.一元弱酸的解離平衡 在一元弱酸HAc的水溶液中。存在著下列質子轉移反應:
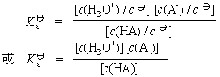 解離常數
解離常數其平衡常數
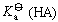 解離常數
解離常數— 弱酸的HA的解離常數。
生成物濃度比上反應物濃度 ,弱酸的解離常數可以藉助pH計測定溶液的pH來確定。若已知弱酸的解離 常數,就可以計算出一定濃度的弱酸的平衡組成.
一般都是對於弱酸弱鹼、難溶電解質和絡合物會使用解離常數k,來表示和計算濃度與解離能力
意義
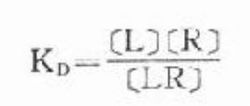 解離常數
解離常數1、KD為解離常數,指引起最大效應一半(50%受體被占位)時的藥物濃度。
2、KD值越大,引起最大效應所需藥物濃度越多,親和力越小。
3、用1/KD來表示親和力。

