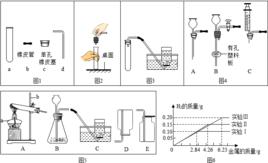
過濾
定義
從液體中分離不溶性固體物質的操作
一貼;用蒸餾水潤濕的濾紙緊貼在漏斗壁上。
二低;濾紙邊緣略低於漏斗邊緣。
三靠濾液液面略低於濾紙邊緣。
1.燒杯中的混合物在過濾前套用玻璃棒攪拌,然後進行過濾。
過濾筒
2.過濾器中的沉澱的洗滌方法:用燒瓶或滴管向過濾器中加蒸餾水,使水面蓋沒沉澱物,待溶液全部濾出後,重複2~3次。
失敗原因
1.濾紙作用失效
1.濾紙破裂
過濾海綿
2.混合物沒有經過濾紙。
2.儀器不乾淨
1.漏斗下端不乾淨
2.下面收集濾液的燒杯不乾淨
這兩種情況下,濾液都是渾濁的。
過濾操作實驗口訣
斗架燒杯玻璃棒,濾紙漏斗角一樣。
過濾之前要靜置,三靠兩低不要忘。
蒸發
實驗儀器
蒸發皿、鐵架台、玻璃棒、坩堝鉗、酒精燈
要求
1.蒸發皿中液體的量不得超過容積的2/3。
2.當加熱至(大量)固體出現時,應停止加熱利用餘熱蒸乾。
3不能把熱的蒸發皿直接放在實驗台上,應墊上石棉網。
4坩堝鉗用於夾持蒸發皿。
溫度、濕度、液體的表面積、液體表面上方的空氣流動的速度等。
1液面表面積大小。如果液體表面面積增大,處於液體表面附近的分子數目增加,因而在相同的時間裡,從液面飛出的分子數量就增多,所以液面面積越大,蒸發速度越快。
蒸餾
指利用液體混合物中各組分揮發性的差異而將組分分離的傳質過程。
注意事項
操作時要注意
(1)在蒸餾燒瓶中放少量碎瓷片,防止液體暴沸。
(2)溫度計水銀球的位置應與支管口下端位於同一水平線上。
(3)冷凝管中冷卻水從下口進,上口出。
(4)加熱溫度不能超過混合物中沸點最高物質的沸點。
蒸餾化學口訣
隔網加熱冷管傾,上緣下緣兩相平。
需加碎瓷防暴沸,熱氣冷水逆向行。
瓶中液限掌握好,先撤酒燈水再停。
暴沸
易引起暴沸的場合和種類很多,粗歸起來有兩種:
1由汽化熱引發的“暴沸”:如冷水滴入熱油中引發的“暴沸”。
處理方式
編輯
1,在反應體系中加入毛細管,素瓷片,沸石等多孔物。
2,在反應體系中加入大量的玻璃纖維。
3,小心控制溫度與入料速度,或者更換為間接加熱方式。
分餾
定義
分餾在常壓下進行,獲得低沸點餾分,然後在減壓狀況下進行。
石油分餾原理圖
獲得高沸點餾分。
每個餾分中還含有多種化合物,可以再進一步分餾。
屬於 物理變化
分餾實驗儀器
酒精燈,石棉網,鐵架台,圓底燒瓶,冷凝管,牛角管(接液器),錐形瓶,溫度計。
萃取
實驗儀器
儀器:分液漏斗。
用四氯化碳萃取碘水中的碘。
常見萃取劑:甲苯,二氯甲烷,三氯甲烷,汽油,乙醚,直餾汽油,正丁醇,四氯化碳。
要求:萃取劑和原溶劑互不混溶 。
萃取劑和溶質互不發生反應 。
溶質在萃取劑中的溶解度遠大於在原溶劑中的溶解度。
方法
單級萃取對給定組分所能達到的萃取率(被萃組分在萃取液中的量與原料液中的初始量的比值)較低,往往不能滿足工藝要求,為了提高萃取率,可以採用多種方法:①多級錯流萃取。料液和各級萃余液都與新鮮的萃取劑接觸,可達較高萃取率。但萃取劑用量大,萃取液平均濃度低。②多級逆流萃取。料液與萃取劑分別從級聯(或板式塔)的兩端加入,在級間作逆向流動,最後成為萃余液和萃取液,各自從另一端離去。料液和萃取劑各自經過多次萃取,因而萃取率較高,萃取液中被萃組分的濃度也較高,這是工業萃取常用的流程。③連續逆流萃取。在微分接觸式萃取塔(見萃取設備)中,料液與萃取劑在逆向流動的過程中進行接觸傳質,也是常用的工業萃取方法。料液與萃取劑之中,密度大的稱為重相,密度小的稱為輕相。輕相自塔底進入,從塔頂溢出;重相自塔頂加入,從塔底導出。萃取塔操作時,一種充滿全塔的液相,稱連續相;另一液相通常以液滴形式分散於其中,稱分散相。分散相液體進塔時即行分散,在離塔前凝聚分層後導出。料液和萃取劑兩者之中以何者為分散相,須兼顧塔的操作和工藝要求來選定。此外,還有能達到更高分離程度的回流萃取和分部萃取
利用物質的溶解性差異,將液體和不溶於液體的固體分離開來的一種方法。如用過濾法除去粗食鹽中少量的泥沙。
定義
從液體中分離不溶性固體物質的操作
一貼;用蒸餾水潤濕的濾紙緊貼在漏斗壁上。
二低;濾紙邊緣略低於漏斗邊緣。
三靠濾液液面略低於濾紙邊緣。
1.燒杯中的混合物在過濾前套用玻璃棒攪拌,然後進行過濾。
2.過濾後若溶液還顯渾濁,應再過濾一次,直到溶液變得透明為止。
過濾筒
3.過濾器中的沉澱的洗滌方法:用燒瓶或滴管向過濾器中加蒸餾水,使水面蓋沒沉澱物,待溶液全部濾出後,重複2~3次。
失敗原因
1.濾紙作用失效
1.濾紙破裂
過濾海綿
造成原因:①。玻璃棒下端緊靠在一層濾紙處。(濾紙被戳破)②.盛混合物的燒杯沒有緊靠玻璃棒。(濾紙被混合物衝破)
2.混合物沒有經過濾紙。
造成原因:液面高於濾紙邊緣。(混合物直接從濾紙和漏斗的間隙直接流下)
2.儀器不乾淨
1.漏斗下端不乾淨
2.下面收集濾液的燒杯不乾淨
這兩種情況下,濾液都是渾濁的。
過濾操作實驗口訣
斗架燒杯玻璃棒,濾紙漏斗角一樣。
過濾之前要靜置,三靠兩低不要忘。
相關解釋
①斗架燒杯玻璃棒,濾紙漏斗角一樣:“斗”指漏斗;“架”指漏斗架。這兩句點明了過濾操作實驗所需要的儀器:漏斗、漏斗架、燒杯、玻璃棒、濾紙,並且強調濾紙摺疊的角度要與漏斗的角度一樣。
過濾
②過濾之前要靜:意思是說在過濾之前須將液體靜置一會兒,使固體和液體充分分離。
蒸發
定義
利用加熱的方法,使溶液中溶劑不斷揮發而析出溶質(晶體)的過程。
實驗儀器
蒸發皿、鐵架台、玻璃棒、坩堝鉗、酒精燈
要求
1.蒸發皿中液體的量不得超過容積的2/3。
2.蒸發過程中必須用玻璃棒不斷攪拌,使液體受熱均勻,以防止局部溫度過高而使液體飛濺。
3.當加熱至(大量)固體出現時,應停止加熱利用餘熱蒸乾。
4.不能把熱的蒸發皿直接放在實驗台上,應墊上石棉網。
5.坩堝鉗用於夾持蒸發皿。
液體的蒸發
這就是蒸發現象。飛出去的分子在和其他分子碰撞後,有可能再回到液面上或進入液體內部。如果飛出的分子多於飛回的,液體就在蒸發。
其他條件相同的不同液體,蒸發快慢亦不相同。這是由於液體分子之間內聚力大小不同而造成的。例如,水銀分子之間的內聚力很大,只有極少數動能足夠大的分子才能從液面逸出,這種液體蒸發就極慢。而另一些液體如乙醚,分子之間的內聚力很小,能夠逸出液面的分子數量較多,所以蒸發得就快。
在蒸發過程中,液體蒸發不僅吸熱還有使周圍物體冷卻的作用。當液體蒸發時,從液體裡跑出來的分子,要克服液體表面層的分子對它們的引力而做功。這些分子能做功,是因為它們具有足夠大的動能。比平均動能大的分子飛出液面,速度大的分子飛出去,而留存液體內部的分子所具有的平均動能變小了。所以在蒸發過程中,如外界不給液體補充能量,液體的溫度就會下降。這時,它就要通過熱傳遞方式從周圍物體中吸取熱量,於是使周圍的物體冷卻。
影響因素
溫度、濕度、液體的表面積、液體表面上方的空氣流動的速度等。
主要因素:(一)溫度。溫度越高,蒸發越快。因為在任何溫度下,分子都在不斷地運動,液體中總有一些速度較大的分子能。
蒸發儀器蒸發皿
1夠飛出液面脫離束縛而成為汽分子,所以液體在任何溫度下都能蒸發。液體的溫度升高,分子的平均動能增大,速度增大,從液面飛出去的分子數量就會增多,所以液體的溫度越高,蒸發得就越快。
2液體表面上方空氣流動的速度。當飛入空氣里的汽分子和空氣分子或其他汽分子發生碰撞時,有可能被碰回到液體中來。如果液面上方空氣流動速度快,通風好,分子重新返回液體的機會越小,蒸發就越快。
蒸餾
定義
指利用液體混合物中各組分揮發性的差異而將組分分離的傳質過程。
將液體沸騰產生的蒸氣導入冷凝管,使之冷卻凝結成液體的一種蒸發、冷凝的過程。蒸餾是分離沸點相差較大的混合物的一種重要的操作技術。
主要儀器
蒸餾燒瓶(帶支管的),溫度計,冷凝管,牛角管,酒精燈,石棉網,鐵架台,支口錐形瓶,橡膠塞。
原理
利用液體混合物中各組分揮發度的差別,使液體混合物部分汽化並隨之使蒸氣部分冷凝,從而實現其所含組分的分離。
是一種屬於傳質分離的單元操作。廣泛套用於煉油、化工、輕工等領域。
將液體加熱至沸騰,使液體變為蒸氣,然後使蒸氣冷卻再凝結為液體,這兩個過程的聯合操作稱為蒸餾。很明顯,蒸餾可將易揮發和不易揮發的物質分離開來,也可將沸點不同的液體混合物分離開來。但液體混合物各組分的沸點必須相差很大(至少30℃以上)才能得到較好的分離效果。在常壓下進行蒸餾時,由於大氣壓往往不是恰好為0.1MPa,因而嚴格說來,應對觀察到的沸點加上校正值,但由於偏差一般都很小,即使大氣壓相差2.7KPa,這項校正值也不過±1℃左右,因此可以忽略不計。
注意事項
操作時要注意
(1)在蒸餾燒瓶中放少量碎瓷片,防止液體暴沸。
(2)溫度計水銀球的位置應與支管口下端位於同一水平線上。
(3)蒸餾燒瓶中所盛放液體不能超過其容積的2/3,也不能少於1/3。
(4)冷凝管中冷卻水從下口進,上口出。
(5)加熱溫度不能超過混合物中沸點最高物質的沸點。
蒸餾化學口訣
隔網加熱冷管傾,上緣下緣兩相平。
需加碎瓷防暴沸,熱氣冷水逆向行。
瓶中液限掌握好,先撤酒燈水再停。
暴沸
(只有液體中存在汽化核時,高於沸點的液體才能圍繞汽化核進行汽化形成氣泡,這就是液體沸騰。)當液體中缺少氣泡或雜質時,即使溫度達到並超過了沸點,也不會沸騰,形成了過熱液體。過熱液體是不穩定的,如果過熱液體的外部環境溫度突然急劇下降或侵入氣泡或雜質,則會形成 劇烈的沸騰,並伴有爆裂聲,這種現象叫 暴沸。暴沸的結果是使液體的溫度回到沸點。暴沸有時是危險的,應當增加液體中的氣泡或雜質防止暴沸的發生。
易引起暴沸的場合和種類很多,粗歸起來有兩種:
1)由溶解熱+汽化熱引發的“暴沸”:如誤操作時將水倒入濃硫酸中,由於二者互溶時放出的熱量滿足了水的汽化熱,而又未能均勻導出,以致產生“暴沸”。
2)由汽化熱引發的“暴沸”:如冷水滴入熱油中引發的“暴沸”。
處理方式
編輯
1,在反應體系中加入毛細管,素瓷片,沸石等多孔物。
2,攪拌。通常反應使用磁力攪拌,非常容易暴沸的反應與放熱大的反應需要使用更激烈的機械攪拌。
3,在反應體系中加入大量的玻璃纖維。
4,小心控制溫度與入料速度,或者更換為間接加熱方式。
例如:
乙醇制乙烯實驗中為了防止催化劑/脫水劑濃硫酸暴沸濺出發生危險,必須放入碎瓷片或者沸石。
分餾
定義
分餾是利用分餾柱將多次氣化—冷凝過程在一次操作中完成的方法。因此,分餾實際上是多次蒸餾。它更適合於分離提純沸點相差不大的液體有機混合物。
分餾是分離提純液體有機混合物的沸點相差較小的組分的一種重要方法,石油就是用分餾來分離的。
分餾在常壓下進行,獲得低沸點餾分,然後在減壓狀況下進行。
石油分餾原理圖
獲得高沸點餾分。
每個餾分中還含有多種化合物,可以再進一步分餾。
屬於 物理變化
分餾實驗原理
1.進行分餾的必要性。(1)蒸餾分離不徹底。(2)多次蒸餾操作繁瑣,費時,浪費極大。
2..分餾的原理:混合液沸騰後蒸氣進入分餾柱中被部分冷凝,冷凝液在下降途中與繼續上升的 蒸氣接觸,二者進行熱交換,蒸汽中高沸點組分被冷凝,低沸點組分仍呈蒸氣上升,而冷凝液中低沸點組分受熱氣化,高沸點組分仍呈液態下降。結果是上升的蒸汽中低沸點組分增多,下降的冷凝液中高沸點組分增多。如此經過多次熱交換,就相當於連續多次的普通蒸餾。以致低沸點組分的蒸氣不斷上升,而被蒸餾出來;高沸點組分則不斷流回蒸餾瓶中,從而將它們分離。
分餾實驗儀器
酒精燈,石棉網,鐵架台,圓底燒瓶,冷凝管,牛角管(接液器),錐形瓶,溫度計。
萃取
萃取利用物質在兩種互不相溶(或微溶)的溶劑中溶解度或分配係數的不同使物質從一種溶劑內轉移到另外一種溶劑中。
原理
原理示意圖
物理變化。
CA/CB=K
CA.CB分別表示一種物質在兩種互不相溶地溶劑中的量濃度。K是一個常數,稱為“分配係數”。
有機化合物在有機溶劑中一般比在水中溶解度大。用有機溶劑提取溶解於水的化合物是萃取的典型實例。
分液漏斗
在水溶液中加入一定量的電解質(如氯化鈉),利用“鹽析效應”以降低有機物和萃取溶劑在水溶液中的溶解度,常可提高萃取效果。
要把所需要的溶質從溶液中完全萃取出來,通常萃取一次是不夠的,必須重複萃取數次。利用分配定律的關係,可以算出經過萃取後化合物的剩餘量。
當用一定量溶劑時,希望在水中的剩餘量越少越好。而上式KV/(KV+S)總是小於1,所以n越大,wn就越小。也就是說把溶劑分成數次作多次萃取比用全部量的溶劑作一次萃取為好。但應該注意,上面的公式適用於幾乎和水不相溶地溶劑,例如苯,四氯化碳等。而與水有少量互溶地溶劑乙醚等,上面公式只是近似的。但還是可以定性地指出預期的結果。
實驗儀器
儀器:分液漏斗。
用四氯化碳萃取碘水中的碘。
常見萃取劑:甲苯,二氯甲烷,三氯甲烷,汽油,乙醚,直餾汽油,正丁醇,四氯化碳。
要求:萃取劑和原溶劑互不混溶 。
萃取劑和溶質互不發生反應 。
溶質在萃取劑中的溶解度遠大於在原溶劑中的溶解度。
相關規律:有機溶劑易溶於有機溶劑,極性溶劑易溶於極性溶劑,反之亦然。
方法
單級萃取對給定組分所能達到的萃取率(被萃組分在萃取液中的量與原料液中的初始量的比值)較低,往往不能滿足工藝要求,為了提高萃取率,可以採用多種方法:①多級錯流萃取。料液和各級萃余液都與新鮮的萃取劑接觸,可達較高萃取率。但萃取劑用量大,萃取液平均濃度低。②多級逆流萃取。料液與萃取劑分別從級聯(或板式塔)的兩端加入,在級間作逆向流動,最後成為萃余液和萃取液,各自從另一端離去。料液和萃取劑各自經過多次萃取,因而萃取率較高,萃取液中被萃組分的濃度也較高,這是工業萃取常用的流程。③連續逆流萃取。在微分接觸式萃取塔(見萃取設備)中,料液與萃取劑在逆向流動的過程中進行接觸傳質,也是常用的工業萃取方法。料液與萃取劑之中,密度大的稱為重相,密度小的稱為輕相。輕相自塔底進入,從塔頂溢出;重相自塔頂加入,從塔底導出。萃取塔操作時,一種充滿全塔的液相,稱連續相;另一液相通常以液滴形式分散於其中,稱分散相。分散相液體進塔時即行分散,在離塔前凝聚分層後導出。料液和萃取劑兩者之中以何者為分散相,須兼顧塔的操作和工藝要求來選定。此外,還有能達到更高分離程度的回流萃取和分部萃取