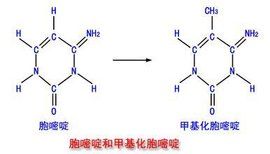
甲基化的功能
甲基化是蛋白質和核酸的一種重要的修飾,調節基因的表達和關閉,與
癌症、
衰老、
老年痴呆等許多疾病密切相關,是
表觀遺傳學的重要研究內容之一。 最常見的甲基化修飾有
DNA甲基化和
組蛋白甲基化。
DNA甲基化能關閉某些基因的活性,去甲基化則誘導了基因的重新活化和表達。DNA甲基化能引起染色質結構、DNA構象、DNA穩定性及DNA與蛋白質相互作用方式的改變,從而控制基因表達。研究證實,CpG二核苷酸中胞嘧啶的甲基化導致了人體1/3以上由於鹼基轉換而引起的遺傳病。DNA甲基化主要形成
5-甲基胞嘧啶(5-mC)和少量的N6-甲基腺嘌呤(N6-mA)及7-甲基鳥嘌呤(7-mG)。在真核生物中,5-甲基胞嘧啶主要出現在CpG序列、CpXpG、CCA/tgg和GATC中。
DNA甲基化是指生物體在DNA甲基轉移酶(DNA methyltransferase,DMT) 的催化下,以s-腺苷甲硫氨酸(SAM)為甲基供體,將甲基轉移到特定的鹼基上的過程。DNA甲基化可以發生在
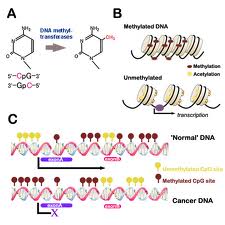 甲基化
甲基化腺嘌呤的N-6位、胞嘧啶的N-4位、鳥嘌呤的N-7位或胞嘧啶的C-5位等。但在哺乳動物中DNA甲基化主要發生在5’-CpG-3’的C上生成5-甲基胞嘧啶(5mC)
在哺乳動物中CpG以兩種形式存在:一種是分散於DNA序列中;另一種呈現高度聚集狀態,人們稱之為CpG島(CpG island)。在正常組織里,70%~90%散在的CpG是被甲基修飾的,而CpG島則是非甲基化的。正常情況下,人類基因組“垃圾”序列的CpG二核苷酸相對稀少,並且總是處於甲基化狀態,與之相反,人類基因組中大小為100-1000bp左右,富含CpG二核苷酸的CpG島則總是處於未甲基化狀態,並且CpG島常位於轉錄調控區附近,與56%的人類基因組編碼基因相關,因此基因轉錄區CpG島的甲基化狀態的研究就顯得十分重要。人類基因組序列草圖分析結果表明,人類基因組CpG島約為28890個,大部分染色體每1Mb就有5-15個CpG島,平均值為每Mb含10.5個CpG島,CpG島的數目與基因密度有良好的對應關係。
DNA甲基化主要是通過DNA甲基轉移酶家族來催化完成的。目前,在真核生物中發現了3類DNA甲基轉移酶(Dnmt1、Dnmt2、Dnmt3a、Dnmt3b).Dnmt1一種是維持性甲基化酶;Dnmt2可與DNA上特異位點結合,但具體作用尚不清楚;Dnmt3a和Dnmt3b是重新甲基化酶,它們使去甲基化的CpG位點重新甲基化,即參與DNA的從頭甲基化。在哺乳動物的生殖細胞發育時期和植入前胚胎期,其
基因組範圍內的甲基化模式通過大規模的去甲基化和接下來的再甲基化過程發生重編程,從而產生具有發育潛能的細胞;在細胞分化的過程中,基因的甲基化狀態將遺傳給後代細胞。由於DNA甲基化與人類發育和腫瘤疾病的密切關係,特別是CpG島甲基化所致抑癌基因轉錄失活問題,DNA甲基化已經成為表觀遺傳學和
表觀基因組學的重要研究內容。
組蛋白甲基化是指發生在H3和H4組蛋白N端Arg或Lys殘基上的甲基化,由組蛋白甲基轉移酶介導催化。組蛋白甲基化的功能主要體現在異染色質形成、基因印記、
X染色體失活和轉錄調控方面。除了存在組蛋白甲基轉移酶以外,現在還發現了去甲基化酶。先前人們認為組蛋白的甲基化作用是穩定而不可逆的,使這種去甲基化酶的發現使組蛋白甲基化過程更具動態性。