術語簡介
摩爾吸光率術語因吸光光度法的誕生而出現,最初稱molar extinction coeffient,我國譯成“克分子消光係數”。其後,隨著人們認識的深化,發現不是“消光”,而是“吸光”(absorption)作用,因而改稱“克分子吸光係數”(molar absorption coeffi-cient)。
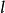 吸光率
吸光率1983年國際純粹與套用化學聯合會分析化學部分析反應與試劑委員會明確指出:“係數”一詞存在濫用的傾向,應限於在比例式中數字套用。這就是說,“係數”應無量綱,是純數學概念;它與任何物理量無關,“克分子吸光係數”一詞就因而不能成立。它的定義是:在1 cm光程()條件下1摩爾濃度的分析物的吸光度,它有量綱:dm ·mol cm (現階段也可以用L·mol ·cm 表示)。據此,刪去“係數”而改稱molar absorptivity。文革之後我國頒布《計量法》,明確採用國際計量制,原來的“克分子”也就改為“摩爾”,“Absorptivity”譯作“吸收率”。這是就字義的廣義而言,也可譯作“吸光率”,這是就特定的吸光光度法而言,其中“率”是無疑義地被普遍肯定和接受的。由於我國科學工作者與時俱進思想不強,有關術語既不嚴謹,也不統一,更未能及時與國際接軌,跟不上時代的步伐。原子吸收光譜法簡稱“原子吸收”而不稱“原子吸光”即其一例,吸收的是“原子”?還是“光能”?
術語缺陷
摩爾吸光率是表達正確的術語,比過去的命名進步;但有其固有的缺點,測定其數值很難。眾所周知,吸光度與待測顯色物的濃度(在一定範圍內)成比例關係(這一規則舊稱Beer定律,但現已不為謹嚴的分析工作者採用,因後經考證,發現此規律是Bourguer,不是Beer),1 mol·L 濃度顯然不在上述的“一定範圍”內,故難直接測定,須在稀濃度條件下測定,再行推算。但即使如此,仍有困難。設待測定的顯色產物濃度為[ML],其測定波長處的摩爾吸光率為ε,加入的顯色劑濃度(過量)為L,其在同一波長處的摩爾吸光率為ε,測定光程為1 cm(所以濃度均以mol· L )計,在此條件下[ M]≥[ML](假定100%反應),[ L]-[ nL]為剩餘的顯色劑濃度。
直接測定的顯色體系吸光度
A= [ML]ε+[ L- nL]ε (1)
ε=A-[ L- nL]ε[ML] (2)
由式(1)可知,測得的吸光度尚包括多餘顯色劑本身吸光度在內,由式(2)可知,求ε須先求出ε和n,兩者均與顯色劑的純度有關,n值更與顯色劑的結構等因素有關。
朗伯-比爾定律
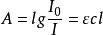 吸光率
吸光率經實踐證明,溶液對光的吸收程度 與溶液的濃度、液層的厚度以及入射光的波長等因素 有關。當保持入射光波長不變,則光吸收的程度與溶液 的濃度、液層厚度和溶液本身吸光性質等有關。這種關 系即是朗伯-比爾定律,用數學式表達如下:
式中 A——吸光度;
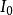 吸光率
吸光率——入射光強度;
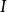 吸光率
吸光率——透過光強度;
ε——摩爾吸光率(L·mol ·cm )。它表示 在某一單色光波長下,物質濃度為1mol ·L ,液層厚度為1cm時,該溶液的吸光度;
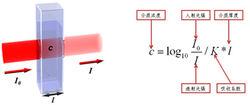 郎伯比爾定律
郎伯比爾定律 吸光率
吸光率——物質的濃度(mol·L ),
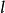 吸光率
吸光率——液層厚度(cm)。
摩爾吸光率表明物質對某一特定波長光的吸收能 力,ε值越大,表示該物質對該波長光的吸收能力越 強,吸光度測定的靈敏度就越高。因此,在進行光度分 析時,為了提高分析的靈敏度,應選擇摩爾吸光率大的 待測化合物,以及選擇具有最大ε值的波長作為入射光。
高吸光率材料
英國薩里大學(University of Su rrey)創造出了一種超級吸光且超薄的材料。這種納米級別的材料運用了納米紋理技術,是一種新型、超薄的石墨烯薄板(graphene sheets)。
研究人員稱,他們是從飛蛾的眼睛獲得的啟發,創造出這種新材料的。石墨烯是一種傳統的優良電子材料,具有顯著的導電性和很好的機械強度,但是它對光能的吸收率不高,一般只能吸收2%~3%的光能,而新的技術可以將石墨烯的光能吸收率提升到90%。
該材料大有用處,如用這種材料可以製作太陽能電池,將其安置在室內,成為一種智慧型壁紙或者智慧型窗戶;利用廢棄閒置的熱能或者光能。這種材料可以為很多智慧型設備提供能源;一些通過新型的感測器和能源發生器互聯的新設備,也可以從這種材料的使用中受益。