名詞解釋
初次免疫應答發生在免疫系統遭遇某種病原體第一次被宿主B細胞識別時,識別抗原後B細胞分化形成漿細胞,後者開始合成抗體。幾天后,抗體開始在血漿中出現,其濃度開始在1~10周內遞增。產生的第一種抗體是IgM,它能與外來物直接結合。細胞因子引發B細胞從增殖分泌IgM的漿細胞轉為增殖分泌IgG的漿細胞。當IgM產量衰減時,IgG生產加速,但最後也一樣會衰減。最終,血漿樣本中IgM和IgG的濃度可降至檢測不到的程度。但是,已增殖和形成記憶的B細胞仍留於淋巴組織中。他們不參於初次應答,但他們保留了識別特定抗原的能力。他們抗原不分化存活幾個月到幾年時間。初次應答學習過程很慢,發生在初次感染前幾天,要用幾周時間清除感染。
免疫性能
 免疫性能
免疫性能免疫是人體的一種生理功能,人體依靠這種功能識別“自己”和“非己”成分,從而破壞和排斥進入人體的抗原物質,或人體本身所產生的損傷細胞和腫瘤細胞等,以維持人體的健康。抵抗或防止微生物或寄生物的感染或其它所不希望的生物侵入的狀態。免疫涉及特異性成分和非特異性成分。非特異性成分不需要事先暴露,可以立刻回響,可以有效地防止各種病原體的入侵。特異性免疫是在主體的壽命期內發展起來的,是專門針對某個病原體的免疫。
免疫力就是機體抵禦外來病原體的能力,它可以由先天遺傳獲得,非特異性地抵禦多種病菌的入侵,稱為天然免疫;也可以在出生後因感染某種特定病菌而產生特異的抵抗力,稱為獲得性免疫。正是免疫系統的積極工作,構築了人體防病的"長城"。隨著年齡增長,孩子的免疫機能逐漸成熟,3歲以上孩子體內免疫血清的抗體濃度即接近成人;8歲後,整個免疫系統的抵抗力已和成人相當。
主要種類
 免疫血清蛋白
免疫血清蛋白特種免疫:個體與生俱有,一般為非特異性免疫,如吞噬細胞的作用。
獲得性免疫
自動獲得性免疫:一般免疫時間長。可待終身,如麻疹、天花、痄腮。
自然獲得:有被天花病毒感染髮病史的人,一般不會再次感染。
人工獲得:如種牛痘免疫天花。
被動獲得性免疫:免疫時間短,人工獲得時,已較少採用。
自然獲得:如嬰兒在母體胎盤或初乳中獲得的免疫 人工獲得:如注射具有免疫力的免疫血清,獲得免疫,如治療蛇毒時注射的血清蛋白。
免疫防線
第一道防線
是由皮膚和黏膜構成的,他們不僅能夠阻擋病原體侵入人體,而且它們的分泌物(如乳酸、脂肪酸、胃酸和酶等)還有殺菌的作用。呼吸道黏膜上有纖毛,可以清除異物
第二道防線
是體液中的殺菌物質和吞噬細胞,這兩道防線是人類在進化過程中逐漸建立起來的天然防禦功能,特點是人人生來就有,不針對某一種特定的病原體,對多種病原體都有防禦作用,因此叫做非特異性免疫(又稱先天性免疫)多數情況下,這兩道防線可以防止病原體對機體的侵襲。
第三道防線
主要由免疫器官(胸腺、淋巴結和脾臟等)和免疫細胞(淋巴細胞)組成,第三道防線是人體在出生以後逐漸建立起來的後天防禦功能,特點是出生後才產生的,只針對某一特定的病原體或異物起作用,因而叫做特異性免疫(又稱後天性免疫)。
相關學科
所謂“免疫”原由拉丁字“immunis”而來,其原意為“免除稅收”(exceptionfromcharges), 也包含著“免於疫患”之意。免疫學是研究生物體對抗原物質免疫應答性及其方法的生物-醫學科學。免疫應答是機體對抗原刺激的反應,也是對抗原物質進行識別和排除的一種生物學過程。
 免疫學
免疫學免疫學是一門既古老而又新興的學科。免疫學的發展是人們在實踐中不斷探索、不斷總結和不斷創新的結果。一般認為免疫學的發展經歷了四個時期即經驗免疫學時期、經典免疫學時期、近代免疫學時期和現代免疫學時期。
一、經驗免疫學時期
早在公元 11 世紀,我國醫學家在實踐中創造性地發明了人痘苗,即用人工輕度感染的方法預防天花。在明代隆慶年間(1567 ~ 1572),人痘苗已在我國廣泛套用;至 17 世紀,人痘苗接種預防天花的方法引起鄰國的注意,先後傳入俄國、朝鮮、日本、土耳其、英國等地,進而使人痘苗預防天花的方法得以推廣和驗證。此即經驗免疫學時期。它是人類認識機體免疫性的開端,為以後英國醫生Jenner (琴納)發明牛痘苗奠定了基礎。該時期發現了免疫現象,對醫學實為一項偉大貢獻。
二、經典免疫學時期
18 世紀至 20 世紀中葉為經典免疫學時期。這一時期,人們對免疫功能的認識由人體現象的觀察進入了科學實驗時期。在此期間取得的重要成果包括:
牛痘苗的發明
牛痘苗的發明是繼人痘苗之後免疫學的一個重要發展,是由英國醫生 Jenner 在觀察到患過牛痘的擠奶女工,不再患天花的事實後,通過長期研究的科學成果。該疫苗給人體接種後,只引起局部反應,並不造成嚴重損害,但能有效地預防天花。它不僅彌補了人痘苗的不足,而且可在實驗室大量生產。因此很快地代替了人痘苗,被醫學界所接受。
減毒活疫苗的發明
19 世紀末,隨著微生物學的發展,法國免疫學家巴斯德(Pasteur)和德國細菌學家郭霍(Koch)在創立了細菌分離培養技術的基礎上,通過系統地科學研究,利用物理、化學,以及生物學方法獲得了減毒菌苗,並用於疾病的預防和治療。 Pasteur 以高溫培養法製備了炭疽疫苗,用狂犬病毒在兔體內經連續傳代製備了狂犬病疫苗。這些減毒疫苗的發明不但為實驗免疫學打下了基礎,也為疫苗的發展開闢了新局面。
抗體的發現
1890 年德國學者 Behring (貝苓)和日本學者北里用白喉外毒素免疫動物時發現,在被免疫的動物血清中有一種能中和外毒素的物質,稱為抗毒素。將此免疫血清被動轉移給正常動物,使後者獲得了中和外毒素的能力。同年 Behring 又與 Kitasato 將白喉抗毒素正式用於白喉的治療,開創了人工被動免疫療法之先河。為此, Behring 於 1901 年獲得諾貝爾醫學和生理學獎。後來,人們相繼發現了凝集素、沉澱素等能與細菌或細胞特異性反應的物質,統稱為抗體;而將能引起抗體產生的物質稱為抗原,從而確立了抗原和抗體的概念。
補體的發現
1894 年, Pfeiffer 發現了免疫溶菌現象。他將霍亂弧菌注射到已被該菌免疫的豚鼠腹腔內,發現新注入的霍亂弧菌迅速溶解。此外,取細菌免疫血清與相應細菌注入正常豚鼠腹腔也可得到同樣結果。 Bordet 將新鮮免疫血清加熱 30 分鐘後,再加入相應細菌,發現只出現凝集,喪失了溶菌能力。據此認為,免疫血清中可能存在兩種與溶菌有關的物質,一種是對熱穩定的物質即抗體,其能與相應細菌或細胞特異性結合,引起凝集;另一種是對熱不穩定的物質,稱之為補體,它是正常血清中的成分,無特異性,但具有協助抗體溶解細菌或細胞的作用。
血清學方法的建立
根據抗原和抗體特異性結合的特點,在抗毒素髮現以後的 10 年中,建立了許多體外檢測抗原、抗體的血清學方法如凝集反應、沉澱反應、補體結合反應等,為傳染病的診斷和流行病學調查提供了新的重要手段。
免疫化學的研究
在抗原和抗體概念確立後,人們對其理化性質、抗原與抗體特異性結合的化學基礎等問題產生了興趣。 20 世紀初, Landsteiner 等套用偶氮蛋白的人工結合抗原,即以芳香族有機化學分子偶聯到蛋白質分子上形成的抗原,研究抗原抗體反應特異性的物質基礎,從中認識到,抗原特異性實際上是由一些小分子的結構及構象決定的,進而提出了關於抗原抗體反應的格子學說,從理論上解釋了血清學反應現象。 20 世紀 30 年代, Tiselies 和 Kabot 建立了血清電泳技術,證明抗體是丙種球蛋白,並利用分離、純化抗體的方法對抗體分子的結構與功能進行研究。 Grubar 等人建立了免疫電泳技術,發現了抗體分子的不均一性的本質,從而使抗體分子與結構研究取得了重大進展。
抗體生成理論的提出
 初次免疫應答
初次免疫應答1897 年, Ehrlich 提出關於抗體產生的學說,即側鏈學說。他認為抗毒素分子存在於細胞表面,當外毒素進入機體與其結合後,可刺激細胞產生更多的抗毒素分子,由細胞表面脫落入血。該學說當時未被免疫學界接受。 20 世紀 30 年代 Haurowitz 和 Pauling 等先後提出抗體生成的直接模板學說和間接模板學說,他們均認為抗原決定了抗體的特異結構,否認抗體產生細胞的膜上具有識別抗原受體。這種只片面強調抗原對機體免疫反應的作用,忽視機體免疫系統對抗原識別的本質的理論,違背了免疫反應的基本規律,阻礙了抗體生成研究的過程。直到細胞系選擇學說提出後,才使免疫學有了新的進展。
?對機體保護性免疫機制的探討
19 世紀末,對機體保護性免疫機制的探討引起人們的關注,在此期間形成兩大學派。一為以 Metchnikoff 為代表的細胞免疫學派,該學派認為抗感染免疫是由體內的吞噬細胞所決定;一為以 Ehrlich 為代表的體液免疫學派,該學派認為血清中的抗體是抗感染免疫的主要因素。它們各持己見,爭論不休,但每一學派都僅僅反應了複雜免疫機制的不同側面,存在一定的片面性。直至 1903 年, Wright 和 Douglas 在研究吞噬現象時,發現血清和其它體液中存在一種物質(調理素),能大大增強吞噬作用,從而初步將兩大學派統一起來,使人們開始認識到機體的免疫機制包括兩個方面:體液免疫和細胞免疫。
三、近代免疫學時期
20 世紀中葉至該世紀 60 年代期間,為近代免疫學時期。這一時期人們衝破了抗感染免疫模板學說的束縛,對生物體的免疫反應性有了比較全面的認識,使免疫學開始研究生物問題,出現了全新的免疫學理論。因此,這一期實際上是免疫生物學時期。在此期間獲得的主要成就包括:
(一)遲髮型超敏反應的發現
Koch 在用結核桿菌給患者皮下注射,試圖進行免疫治療時發現,在注射局部出現組織壞死現象,稱為 Koch 現象。該現象具有特異性。 Chase 等對 Koch 現象進一步深入研究,他們以致敏豚鼠血清轉移給正常動物,未能引起結核菌素反應;而用其淋巴細胞轉移則引起了陽性反應。從而證明了結核菌素反應不是由抗體,而是由致敏淋巴細胞引起,機體的免疫性不僅僅只有體液免疫,也可形成細胞免疫。
(二)免疫耐受的發現
1945 年, Owen 發現異卵雙生的兩頭小牛體內有兩種血型紅細胞共存,稱其為血型細胞相嵌現象。由於不同血型細胞天然存在於同一機體內不引起免疫應答故又稱為天然耐受。此後, Medawar 等在新生期小鼠體內成功地進行了人工誘導異己抗原耐受實驗,揭示了體內處於發育階段的免疫細胞無論接觸自身抗原還是異己抗原,均可導致對相應抗原的耐受。
( 三 ) 細胞系選擇學說的提出
1958 年,澳大利亞免疫學家 Burnet 在 Ehrlich 側鏈學說影響下,提出細胞系選擇學說。該學說闡明了抗體產生的機制,並對諸如抗原識別、免疫記憶及自身耐受與自身免疫等許多重要免疫生物學現象作了解釋,大大促進了現代免疫學的發展。該學說基本觀點為① 認為機體記憶體在識別不同抗原的多種細胞系,每一細胞系的細胞表面表達識別相應抗原的同一受體;② 抗原進入機體後,選擇性地與具有相應受體細胞系的細胞作用,使之活化、增殖、分化成效應細胞或記憶細胞;③ 胚胎期針對自身抗原的免疫細胞與自身抗原接觸後可被破壞、排除或處於抑制狀態;④免疫細胞可突變形成與自身抗原反應的細胞系,導致自身免疫病。
(四)免疫學技術的發展
在此期間,免疫學技術也得到快速發展,建立了間接凝集反應和免疫標記技術,進一步促進了免疫學基礎理論的研究和套用。
四、現代免疫學時期
現代免疫學時期指 20 世紀 60 年代至今的時期。在這一時期,確認了淋巴細胞系在免疫反應中的地位,闡明了免疫球蛋白的分子結構與功能,對免疫系統特別是細胞因子、粘附分子等進行了大量研究,並從分子水平對免疫球蛋白的多樣性、類別轉化等進行了有益的探討,在許多方面取得了突破性成就。
(一)免疫系統的研究
 免疫系統
免疫系統1957 年 Click 發現摘除雞法氏囊,可引起抗體產生缺陷。認為法氏囊是抗體產生細胞存在的主要場所,並將產生抗體的細胞稱為 B 細胞。 Miller 和 Good 通過在哺乳類動物體內進行早期胸腺摘除,導致細胞免疫缺陷和抗體產生嚴重下降,證明了存在於胸腺的免疫細胞主要執行細胞免疫,稱之為 T 細胞。 1969 年 Claman 和 Mitchell 等提出了 T 細胞亞群的概念。此後,人們進一步證實了經胸腺和法氏囊分化、成熟的 T 、 B 淋巴細胞在外周淋巴組織的分布,以及 T 、 B 細胞在抗體產生中的協同作用,從而建立了免疫系統的組織學和細胞學基礎。
(二)抗體結構與功能的研究
20 世紀 60 年代, Porter 用木瓜蛋白酶水解抗體,獲得了抗體活性片段( Fab )和可結晶片段( Fc )。用化學還原法證明抗體是由多肽鏈組成,並以抗原分析法證明了抗體分子的不均一性。此後,人們統一了抗體球蛋白名稱,並建立了免疫球蛋白的分類。
(三)免疫網路學說的提出
1972 年, Jerne 提出免疫網路學說。該學說認為:抗體和淋巴細胞表面的抗原受體存在獨特性,在抗原進入前,抗體處於相對穩定狀態,當抗原進入機體後,使這種平衡被打破,導致特異性抗體產生,當後者達到一定量時,可引起抗獨特型抗體產生。由此可見,在同一機體內一組抗體的獨特型
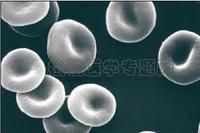
正常紅細胞電鏡圖
決定基可被另一組抗獨特型抗體分子識別;而一組淋巴細胞表面的抗原受體可被另一組淋巴細胞表面抗獨特型表面受體所識別,這樣在淋巴細胞和抗體之間就形成了獨特型 - 抗獨特型免疫網路。
網路學說探討了免疫調節機制,提出由抗原刺激引起的免疫應答不是無休止地進行,而是受獨特型抗體的制約,籍以維持機體的生理穩定和平衡。
(四)抗體多樣性研究
早在 20 世紀 60 年代 Dreyer 和 Benner 等曾提出一種假設,認為編碼免疫球蛋白( Ig )肽鏈的基因是由兩種基因組成。在胚胎期,它們彼此分隔存在,在 B 細胞分化、發育過程中重排和拼接在一起。日本學者利根川進等套用分子雜交技術克隆出編碼 Ig 分子 V 區和 C 區基因,並套用 cDNA 克隆探針證明了 B 細胞在分化發育過程中編碼 Ig 的基因結構,進而闡明了抗原結合部位多樣性的遺傳控制。
(五)細胞因子與免疫細胞膜分子研究
細胞因子和免疫細胞膜分子研究是近 20 年來免疫學研究的熱點。
最初人們從細胞培養液中提取細胞因子進行功能和結構的研究,相繼發現了白細胞介素(IL) 、干擾素(IFN) 、腫瘤壞死因子(TNF) 、集落刺激因子(CSF) 等細胞因子,對其生物學功能、作用特點有了進一步的了解。在此基礎上,通過基因工程技術,可大批量生產細胞因子,促進了細胞因
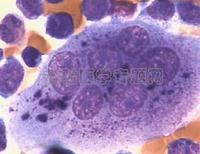
吞噬細胞吞噬病菌
子在臨床治療和實驗研究中的套用。
免疫細胞膜分子種類很多,主要包括 T 、 B 細胞抗原識別受體( TCR / BCR )、主要組織相容性抗原、白細胞分化抗原(CD) 、促分裂素受體、細胞因子受體、免疫球蛋白受體,以及其它受體和分子。 20 世紀初,人們發現在不同種屬或同種不同個體間進行正常組織或腫瘤移植時出現的排斥反應是由細胞表面主要組織相容性分子( MHC Ⅰ/Ⅱ類分子)決定的。此後,人們又注意到 T 細胞識別抗原時,存在 MHC 的限制性即 T 細胞抗原受體 (TCR) 在識別異己抗原時,同時識別自身 MHC 分子。
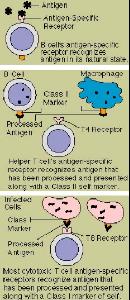 初次免疫應答
初次免疫應答人們對白細胞分化抗原 (CD) 的大量研究,揭示了 T 細胞亞群的功能、細胞激活途經和膜信號的轉導及細胞分化過程中的調控等機制。此外,在研究細胞毒性T 細胞( CTL )殺傷作用時,發現 CTL 表達的 FasL 可與靶細胞表達的 Fas 結合,引起靶細胞內半胱天冬蛋白酶( caspsase )級聯活化,裂解 DNA ,導致靶細胞死亡稱為細胞程式性死亡( PCD )或細胞凋亡( apoptosis )。
(六)套用免疫學的發展
1975 年 Kohler 和 Milstein 首創雜交瘤技術。他們將小鼠骨髓瘤細胞和經綿羊紅細胞( SRBC )致敏的 B 細胞在體外進行融合形成雜交瘤( hybridoma )。這種雜交瘤細胞既保持了骨髓瘤細胞大量無限制生長繁殖的特性,又具有合成和分泌抗體的能力。套用該技術可產生均一的、只針對單一抗原決定基的抗體,稱為單克隆抗體( McAb )。 McAb 具有純度高、特異性強、可大量生產等優點,已被廣泛套用於血清學診斷、免疫細胞及其它組織細胞表面分子的檢測,並通過與核素、各種毒素或藥物化學偶聯進行腫瘤導向治療研究。
將分子生物學技術套用於免疫學研究也是一項突破性成就。利用分子雜交技術和分子遺傳學理論製備的基因工程抗體如完全人源化抗體、單鏈抗體及雙特異性抗體等較 McAb 更具優越性。目前,分子雜交技術也被用於研究免疫球蛋白分子、 T 細胞受體分子、補體、細胞因子,以及 MHC 分子等的基因結構、功能及其表達機制。 20 世紀 80 年代出現的聚合酶鏈反應( PCR )是一種體外核酸擴增技術。套用該技術製備重組疫苗、 DNA 疫苗及轉基因植物疫苗,為免疫預防開闢了嶄新的前景。而利用基因工程製備重組細胞因子的廣泛開展,已取得了較大的經濟效益和社會效益。
免疫功能
現代免疫學認為,機體的免疫功能是對抗原刺激的應答,而免疫應答又表現為免疫系統識別自己和排除非己的能力。免疫功能根據免疫識別發揮作用。這種功能大致有:對外源性異物(主要是傳染性因子)的免疫防禦;去除衰退或損傷細胞的免疫,以保持自身穩定;消除突變細胞的免巨噬細胞疫監視。
只有免疫系統在正常條件下發揮相應的作用和保持相對的平衡,機體才能維持生存。如果免疫功能發生異常,必然導致機體平衡失調,出現免疫病理變化。
免疫系統在發揮免疫功能的過程中,識別是個重要的前提。一切生物都具有這種能力。單細胞生物只具有分辨食物、入侵微生物和本身細胞成分等低級的識別功能。脊椎動物的機體免疫系統逐漸完善,不僅具有完整的免疫器官和免疫細胞,而且免疫活性細胞還能產生特異性抗體和琳巴因子,從而準確地識別自己,排除異物以達到機體內環境的相對穩定,這對保護自己、延續種族和生物進化都有重大意義。高等生物的免疫系統充分發展,它對內外環境的各種抗原異物刺激既表現出多樣性和適應性,又表現出特異性和回憶性,這對生物的進化過程、生物種系的生存和適應具有重大影響。
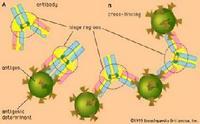
抗原抗體
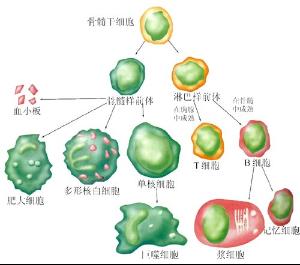 初次免疫應答
初次免疫應答免疫功能是免疫系統在識別和清除“非己”抗原的過程中所產生的各種生物學作用的總稱。主要包括:
1.免疫防禦(Immunologicaldefence)
是機體排斥外來抗原性異物的一種免疫保護功能。正常時可產生抗感染免疫的作用,防禦功能過強會產生超敏反應,過弱則產生免疫缺陷(後兩種情況均屬異常反應)。
2、免疫自穩
是機體免疫系統維持內環境相對穩定的一種生理功能。
正常時:機體可及時清除體內損傷、衰老、變性的血細胞和抗原-抗體複合物,而對自身成份保持免疫耐受
異常時:發生生理功能紊亂、自身免疫病等。
單克隆抗體技術
3、免疫監視
是機體免疫系統及時識別、清除體內突變、畸變和病毒干擾細胞的一種生理保護作用。
喪失:機體突變細胞失控,有可能導致腫瘤發生;或出現病毒的持續感染。