介紹
發明者
 侯氏制鹼法
侯氏制鹼法侯德榜(1890年8月9日~1974年8月26日),名啟榮,字致本,生於福建閩侯,著名科學家,傑出化學家,侯氏制鹼法的創始人,中國重化學工業的開拓者。近代化學工業的奠基人之一。
20世紀20年代,突破氨鹼法制鹼技術的奧秘,主持建成亞洲第一座純鹼廠;30年代,領導建成了中國第一座兼產合成氨、硝酸、硫酸和硫酸銨的聯合企業;40~50年代,又發明了連續生產純鹼與氯化銨的聯合制鹼新工藝,以及碳化法合成氨流程制碳酸氫銨化肥新工藝;並使之在60年代實現了工業化和大面積推廣。
1926年中國“紅三角”牌純鹼入萬國博覽會,獲金質獎章。
他還積極傳播交流科學技術,培育了很多科技人才,為發展科學技術和化學工業做出了貢獻。
發明原理
氨氣與水和二氧化碳反應生成一分子的碳酸氫銨,這是第一步。第二步是:碳酸氫銨與氯化鈉反應生成一分子的氯化銨和碳酸氫鈉沉澱。 根據 NHCl 在常溫時的溶解度比 NaCl 大,而在低溫下卻比 NaCl 溶解度小的原理,在 278K ~ 283K(5 ℃~ 10 ℃ ) 時,向母液中加入食鹽細粉,而使 NHCl 單獨結晶析出供做氮肥。
化學原理
總反應方程式:
NaCl + CO+NH+HO=NaHCO↓+NHCl(可作氮肥)
2NaHCO=NaCO+HO+CO↑(CO循環使用)(以加熱作為反應條件)
(在反應中NaHCO沉澱,所以這裡有沉澱符號,這也正是這個方法的便捷之處)
即:①NaCl(飽和溶液)+NH(先加)+HO(溶液中)+CO(後加)=NHCl+NaHCO↓ (NaHCO能溶於水,但是侯氏制鹼法向飽和氯化鈉溶液中通入氨氣,由於氯化鈉溶液飽和,生成的碳酸氫鈉溶解度小於氯化鈉,所以碳酸氫鈉以沉澱析出)
(先添加NH而不是CO:CO在NaCl中的溶解度很小,先通入NH使食鹽水顯鹼性(用無色酚酞溶液檢驗),能夠吸收大量CO氣體,產生高濃度的HCO ,才能析出NaHCO晶體。)
2NaHCO(加熱)=NaCO+HO+CO↑
發明特點
 侯德榜博士郵票
侯德榜博士郵票針對索爾維法生產純鹼時食鹽利用率低,制鹼成本高,廢液、廢渣污染環境和難以處理等不足,侯德榜先生經過上千次試驗,在1943年研究成功了聯合制鹼法。這個新工藝是把氨廠和鹼廠建在一起,聯合生產。由氨廠提供鹼廠需要的氨和二氧化碳。母液里的氯化銨用加入食鹽的辦法使它結晶出來,作為化工產品或化肥。食鹽溶液又可以循環使用。為了實現這一設計,在1941一1943年抗日戰爭的艱苦環境中,在侯德榜的嚴格指導下,經過了500多次循環試驗,分析了2000多個樣品後,才把具體工藝流程定下來,這個新工藝使食鹽利用率從70%一下子提高到96%,也使原來無用的氯化鈣轉化成化肥氯化銨,解決了氯化鈣占地毀田、污染環境的難題。這方法把世界制鹼技術水平推向了一個新高度,贏得了國際化工界的極高評價。1943年,中國化學工程師學會一致同意將這一新的聯合制鹼法命名為“侯氏聯合制鹼法”。所謂“聯合制鹼法”中的“聯合”,指該法將合成氨工業與制鹼工業組合在一起,利用了生產氨時的副產品CO,革除了用石灰石分解來生產,簡化了生產設備。此外,聯合制鹼法同時也避免了生產氨鹼法中用處不大的副產物氯化鈣,而用可作化肥的氯化銨來回收,提高了食鹽利用率,縮短了生產流程,減少了對環境的污染,降低了純鹼的成本。聯合制鹼法很快為世界所採用。
優缺點
優點:
保留了氨鹼法的優點,消除了它的缺點,使食鹽的利用率提高到 96 %; NHCl 可做氮肥(氮肥不可與鹼性物質混用,但可用草木灰檢驗其純度);可與合成氨廠聯合,使合成氨的原料氣 CO 轉化成 CO,革除了CaCO制 CO這一工序,減少可能造成的環境污染。
兩個循環:
一:2NaHCO=NaCO+HO+CO↑(CO循環使用)(以加熱作為反應條件)
二:向 母液中加入食鹽細粉,從而使 NHCl 單獨結晶析出供做氮肥。
第二個循環的具體操作:
①通入氨氣,冷卻後,加入NaCl,使得NHCl沉澱。過濾後,得到較純淨的NHCl晶體(產物),濾液為 飽和食鹽水(含有氨氣分子),經處理後方可回到第一步循環利用;
②不通氨氣,冷卻後,加入NaCl,使得NHCl沉澱。過濾後,得到NHCl晶體(產物),濾液為飽和食鹽 水,可直接回到第一步循環利用。
原理:低溫時,氯化銨的溶解度低於氯化鈉的溶解度,而由於之前加入氯化鈉(氨氣)使得氯離子(銨根 離子)濃度提高,所以再根據勒夏特列原理,氯化銨將最先析出。
不足之處:
侯氏聯合制鹼法也存在不足。較氨鹼法而言,它的用氨量較大,在有些情況下不適用。
發明歷史
什麼是純鹼
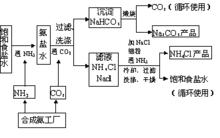 侯氏制鹼法流程圖
侯氏制鹼法流程圖純鹼(碳酸鈉)化學式為NaCO,俗名純鹼,又稱蘇打、鹼灰,是一種重要的化工基本原料,純鹼的用途很廣,一般都是利用它的鹼性。它可用於製造玻璃,如平板玻璃、瓶玻璃、光學玻璃和高級器皿;還可利用脂肪酸與純鹼的反應制肥皂;在硬水的軟化、石油和油類的精製、冶金工業中脫除硫和磷、選礦、以及銅、鉛、線、錫、鈾、紹等金屬的製備、化學工業中製取鈉鹽、金屬碳酸鹽、漂白劑、填料、洗漆劑、催化劑及染料等均要用到它,在陶瓷工業中製取耐火材料和釉也要用到純鹼。純鹼是重要的化工原料之一,用於制化學品、清洗劑、洗漆劑、也用於照相術和制醫藥品。絕大部分用於工業,一小部分為民用。在工業用純鹼中,主要是輕工、建材、化學工業,約占三分之二;其次是冶金、紡織、石油、國防、醫藥及其它工業。
純鹼生產歷史
純鹼是人類最早製取和使用的化學物質之一。7000多年以前,天然的碳酸鈉首先是從幼發拉底河邊生長的花的灰燼中提取的。大約5500年以前埃及人也開始用一種從湖水蒸發中提取的天然純鹼,生產裝飾玻璃和作為鉛酸矽砂聚和肥皂的一種成份。當人們從海藻類植物的灰中提取豐富的鈉鹼時,也從木材灰中得到了豐富的鉀鹼。用天然植物生產鉀鹼的方法一直延續到1870年,德國JP始采含鉀鹽礦才結束。
1790年獲得專利權的路布蘭制鹼法是人類歷史上第一個大規模化學制鹼法。用此方法建成的鹼廠曾遍布整個歐洲。路布蘭制鹼法一直延續到1930年,後來完全被索爾維制鹼法所取代。
1861年,E.索爾維在煤氣廠從事稀氨水的濃縮工作時,在用鹽水吸收氨和二氧化碳的試驗中得到碳酸氫鈉。同年,他獲得了用食鹽、氨和二氧化碳製取碳酸鈉的工業生產方法的專利。此種生產方法被稱為索爾維法,又稱氨鹼法。
日本旭稍子公司於1950年在牧山化工廠建立日產30噸的聯合制鹼廠,1959年3月在千葉化工廠開始建立了新的聯合制鹼廠,日產300噸純鹼和氯化銨,命名為A.C.法。19世紀70年代日本氯化銨的生產供過於求,除恢復部分氨鹼法生產外,旭稍子創建了新旭法,又稱N.A.法。
發展歷史
 侯德榜
侯德榜第一次世界大戰後,中國從歐洲進口純鹼的道路被阻斷,而當時壟斷中國純鹼市場的英國卜內門洋鹼公司卻囤積居奇,鹼價暴漲。看到這種情況,范旭東先生於1917年在實驗室成功制出了鹼。1920年成立“永利制鹼公司”,1922年請來侯德榜先生作為技術指導,他全身心的投入制鹼工藝和設備的改進上,終於摸索出了索爾維法的各項生產技術。1924年8月,塘沽鹼廠正式投產。1926年,中國生產的“紅三角”牌純鹼在美國費城的萬國博覽會上獲得金質獎章。產品不但暢銷國內,而且遠銷日本和東南亞。
1937年日本帝國主義發動了侵華戰爭,把工廠遷到四川,新建了永利川西化工廠。
制鹼的主要原料是食鹽,也就是氯化鈉,而四川的鹽都是井鹽,要用竹筒從很深很深的井底一桶桶吊出來。由於濃度稀,還要經過濃縮才能成為原料,這樣食鹽成本就高了。另外,索爾維制鹼法的致命缺點是食鹽利用率不高,也就是說有30%的食鹽要白白地浪費掉,這樣成本就更高了,所以侯德榜決定不用索爾維制鹼法,而另闢新路。
他首先分析了索爾維制鹼法的缺點,發現主要在於原料中各有一半的比分沒有利用上,只用了食鹽中的鈉和石灰中碳酸根,二者結合才生成了純鹼。食鹽中另一半的氯和石灰中的鈣結合生成了氯化鈣,這個產物都沒有利用上。那么怎祥才能使另一半成分變廢為寶呢?他想呀想,設計了好多方案,但是—一都被推翻了。後來他終於想到,能否把索爾維制鹼法和合成氨法結合起來,也就是說,制鹼用的氨和二氧化碳直接由氨廠提供,濾液中的氯化銨加入食鹽水,讓它沉澱出來。這氯化銨既可作為化工原料,又可以作為化肥,這樣可以大大地提高食鹽的利用率,還可以省去許多設備,例如石灰窯、化灰桶、蒸氨塔等。構想有了,能否成功還要靠實踐。於是他又帶領技術人員,做起了實驗。一直進行了500多次試驗,還分析了2000多個樣品,才把試驗搞成功,使構想成為了現實。
這個制鹼新方法被命名為“聯合制鹼法”,它使鹽的利用率從原來的70%一下子提高到96%。此外,污染環境的廢物氯化鈣成為對農作物有用的化肥——氯化銨,還可以減少1/3設備,所以它的優越性大大超過了索爾維制鹼法,從而開創了世界制鹼工業的新紀元。