基本信息
 deoxycholic acid
deoxycholic acid通用名:deoxycholicacid(脫氧膽酸注射液)
GenericName:deoxycholicacid
批准時間:2015年4月29日
DateofApproval:April29,2015
Company:KytheraBiopharmaceuticals,Inc.
Treatmentfor:SubmentalFullness
適應證和用途
伴隨豐滿頦下脂肪
KYBELLA™(去氧膽酸)注射液是適用為在成年中中度至嚴重凸起或伴隨豐滿頦下脂肪外觀的改善。
使用限制
尚未確定為頦下區外皮下脂肪治療KYBELLA的安全和有效使用和建議不使用。
劑量和給藥方法
1劑量
用面積調整劑量的2mg/cm2KYBELLA被注入至在頦下區中皮下脂肪組織。
●一個單次治療由直至最大50次注射組成,各0.2mL(直至總共10mL),間隔1-cm。
●在間隔小於1個月內可能給予直至6個單次治療。
注射前見對給藥的一般考慮和注射技術。
對給藥的一般考慮
應由衛生保健提供者給予KYBELLA。
篩選患者頦下凸起/豐滿其他潛在原因(如,甲狀腺腫大和淋巴結腫大)。
在過多的皮膚鬆弛,突出頸闊肌帶或可能導致頦下脂肪減少在美容上不希望的結果其他情況患者中仔細考慮KYBELLA的使用.
在曾有以前頦下區的手術或美學治療患者中慎用。解剖/標誌性變化或瘢痕組織的存在可能影響安全給予KYBELLA的能力或以獲得所需的美容效果。
KYBELLA是透明,無色和無顆粒物質。肉眼觀測KYBELLA小瓶顆粒物質和/或變色,而如溶液變色和/或含顆粒物質遺棄小瓶。
使用後,遺棄在小瓶中任何遺留溶液。
注射技術
KYBELLA的安全和有效使用依賴於使用正確數量和注射位置,適當針位置,和給藥技術。
衛生保健專業人員給予KYBELLA必須了解相關頦下解剖學和在牽連區域關聯的神經肌肉結構和由於以前手術或美容技術對解剖學的變化.
避免注射接近下頜緣神經的區域
放置針相對於下頜骨的位置是非常重要的因為它減少對損傷下頜緣神經的潛能,一個面神經運動分支。對神經損傷展示為不對稱的微笑由於唇降肌麻痹。
避免對下頜緣神經損傷:
●不要注入至下頜骨下緣以上。
●不要注入下緣1-1.5cm線以下確定的區域內(從下顎[manidible]至頦部[mentum]的角度)。
●僅注射KYBELLA在目標頦下脂肪治療區內。
●採用大口徑針,抽吸1mL的KYBELLA至一個無菌1mL注射器和排出注射器筒中任何空氣泡。
●讓患者緊張頸闊肌。捏住頦下脂肪和,用一個30號(或更小)0.5-英寸針,注入0.2mL的KYBELLA至前-頸闊肌脂肪通過針垂直於皮膚相鄰每個標記的注射部位進針。
●注射太淺(至真皮)可能導致皮膚潰瘍。注射過程中不要從皮下脂肪將針退出,因為這可能會增加皮內暴露和潛在的皮膚潰瘍的風險。
●通過注入KYBELLA至脂肪組織的深度到皮下脂肪層的大約在中途避免注射入後-頸闊肌脂肪(圖2)。
●如果在任何時間針插入遇到阻力時,這表明可能接觸到筋膜或非脂肪組織,針頭必須撤回到注射給藥之前適當的深度。
●避免注射至其他組織例如肌肉,唾液腺和淋巴結.
●在針回撤時,對每個注射部位可能需要加壓力因為需要減少出血;可套用粘合劑敷料。
劑型和規格
注射液:10mg/mL。KYBELLA注射液是一種透明,無色,無菌溶液在2mL小瓶中供應意向為單個患者使用。每毫升溶液含10mg去氧膽酸。
禁忌證
在注射部位存在感染禁忌KYBELLA。
警告和注意事項
1下頜緣神經損傷
臨床試驗期間報導下頜緣神經損傷的病例,或面部肌肉無力(麻痹)。避免對神經損傷潛能,KYBELLA不應被注入至或在靠近面部的下頜緣支神經。從試驗報導的所有下頜緣神經損傷自發地解決(範圍1-298天,中位數44天)。
2咽下困難
在臨床試驗中發生在給藥部位反應情況下吞咽困難(咽下困難),如,疼痛,腫脹,和頦下區的硬結。咽下困難的病例自發地解決(範圍1-81天,中位3天)。
有當前或咽下困難既往史受試者被排除臨床試驗。在當前或既往病史患者由於咽下困難可能導致病情惡化避免KYBELLA使用。
3注射部位血腫/瘀傷
在臨床試驗中,用KYBELLA治療受試者72%經受注射部位血腫/瘀傷。
有出血異常或當前正在用抗血小板或抗凝治療因為在治療區可能發生出血加重或瘀傷應慎用使用KYBELLA。
4接近注射易受傷害解剖結構風險
避免潛在的組織損傷,KYBELLA不應被注入或緊密鄰近(1-1.5cm)至唾液腺,淋巴結和肌肉。
不良反應
臨床試驗
因為臨床試驗是在廣泛不同情況下進行的,臨床試驗觀察到不良反應率不能與另一種藥臨床試驗發生率直接比較而且可能不反映實踐中觀察到的發生率。
在兩項雙盲,安慰劑-對照臨床試驗513例受試者用KYBELLA治療和506例受試者用安慰劑治療。人群是19-65歲,85%是女性,87%高加索人,8%非洲美國人。在基線時人群有均數BMI為29kg/m2,中度至嚴重頦下區凸起(在0至4級被分級為2或3)和沒有過多的皮膚鬆弛。受試者接受直至6個治療間隔至少1個月和在末次接受治療後被隨訪直至6個月。
反應情況
伴隨KYBELLA使用其他不良反應包括:注射部位出血,注射部位變色,預暈厥/暈厥,淋巴結腫大,注射部位蕁麻疹和頸痛。
不良反應持續長於30天和在多於10%受試者是注射部位麻木(42%),注射部位水腫/腫脹(20%),注射部位疼痛(16%),和注射部位硬結(13%)。
在特殊人群中使用
妊娠
風險總結
在妊娠婦女中沒有KYBELLA的適當和對照良好研究告知藥物關聯風險。不知道適應人群中主要出生缺陷和流產背景風險。但是,在美國一般人群主要出生缺陷背景風險是2-4%和流產是臨床可識別妊娠的15-20%。在動物生殖研究中,大鼠在器官形成期在劑量直至皮下給予去氧膽酸最大推薦人劑量(MRHD)100mg的5倍未觀察到胎鼠危害。
數據
動物數據
在大鼠和兔在器官形成期時給予皮下劑量去氧膽酸曾進行胚胎胎兒發育研究。對比較動物與人劑量的基礎,MRHD是1.7mg/kg(100mg/60kg)。在大鼠中直至最高測試劑量(50mg/kg)根據一個mg/m2比較它比KYBELLA的MRHD較高5-倍,未觀察到胎兒危害的證據。但是,在兔中在所有測試劑量水平包括最低劑量(10mg/kg)根據一個mg/m2比較它比KYBELLA的MRHD較高2-倍時注意到丟失中間肺葉。這些效應可能與母體毒性相關,在所有測試劑量水平也見到。
哺乳
風險總結
不能得到在乳汁人中合成去氧膽酸的存在,藥物對哺乳嬰兒影響或藥物對乳汁產生的影響信息。應一併考慮哺乳餵養發育和健康獲益與母親對KYBELLA臨床需求和哺乳餵養兒童來自母親所患情況任何潛在不良影響。
兒童使用
尚未確定在18歲以下患者中安全性和有效性和KYBELLA不意向為兒童或青少年使用。
老年人使用
KYBELLA的臨床試驗未包括充分數量年齡65和以上受試者不餓能確定他們的反應是否不同於較年輕受試者。其他報導的臨床經驗沒有鑑定老年人和較年輕患者間反應的差別。一般說來對一位老年患者劑量選擇應謹慎,通常在給藥劑量範圍低端開始,反映老年人肝,腎,或心臟功能減低和同時疾病或其他藥物治療的頻數更高。
藥物過量
KYBELLA的過大劑量/容積的注射可能增加不良反應的風險。
一般描述
KYBELLA(去氧膽酸[deoxycholicacid])注射液,10mg/mL是一種透明無色,無菌溶液為皮下使用。它含一種細胞溶解藥,去氧膽酸,作為活性成分。去氧膽酸化學名為3α,12α-dihydroxy-5β-cholan-24-oicacid,和其分子式為C24H40O4,及其分子量為392.57g/mol。去氧膽酸的化學結構為:
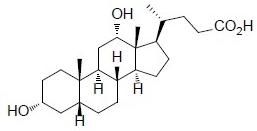 化學式
化學式臨床藥理學
作用機制
KYBELLA是一種細胞溶解藥,當注入組織物理學地破壞細胞膜引起溶解。
藥效動力學
心臟電生理學
在治療劑量,KYBELLA不延長QTc間期。
藥代動力學
在個體內和間內源性去氧膽酸血漿水平是高度變異;這個天然組分的大多數是隔離腸肝循環。
吸收和分布
皮下注射後來自KYBELLA的去氧膽酸被迅速吸收。用單次最大推薦劑量治療劑量KYBELLA(100mg)給藥後,觀察到注射後中位Tmax為18分鐘達到最高血漿濃度(均數Cmax)。均數(±SD)Cmax值為1024±304ng/mL和是較高於缺乏KYBELLA期間24-小時觀察到基線內源性期間平均Cmax值的3.2-倍。最大推薦單次治療劑量(100mg)後,均數(±SD)去氧膽酸暴露(AUC0-24)為7896±2269ng.hr/mL和是1.6-倍較高於內源性暴露。治療後在24小時內去氧膽酸血漿水平返回至內源性範圍。用建議的治療頻數預期無積蓄。
去氧膽酸被廣泛地結合至血漿中蛋白(98%)。
代謝和排泄
內源性去氧膽酸是膽固醇代謝的產物和在糞中被完整排泄。在正常條件下去氧膽酸不被代謝至任何顯著程度。
來自KYBELLA的去氧膽酸在肝腸循環中加入內源性膽汁酸池和與內源性去氧膽酸一起被排泄。
藥物相互作用的體外評估
來自體外研究的結果表明在臨床相關濃度去氧膽酸不抑制或誘導人細胞色素P450(CYP)酶。去氧膽酸不抑制以下轉運蛋白:P-gp,BCRP,MRP4,MRP2,OATP1B1,OATP2B1,OATP1B3,OCT1,OCT2,OAT1,OAT3,NTCP,和ASBT。
特殊人群
肝受損
尚未在有肝受損受試者中研究KYBELLA。考慮中間給藥頻度,小劑量給藥代表約3%的總膽酸池,而內源性去氧膽酸水平高度變異,KYBELLA注射後去氧膽酸的藥代動力學可能不受肝受損影響。
性別的藥代動力學影響
去氧膽酸的藥代動力學不受性別影響。
非臨床毒理學
癌發生,突變發生,生育力受損
未曾在動物中進行長期研究評價KYBELLA的致癌性潛能。
在一組體外試驗中(Ames試驗和人淋巴細胞染色體畸變試驗)和體內(大鼠紅細胞微核試驗)遺傳毒性試驗KYBELLA是陰性。
在雄性和雌性大鼠交配前和期間和在雌性大鼠至妊娠第7天給予去氧膽酸在皮下劑量至50mg/kg(根據mg/m2比較MRHD的5倍)每周1次未觀察到對生育力影響。
臨床研究
進行兩項相同設計的隨機化,多中心,雙盲,安慰劑-對照試驗評價KYBELLA為使用改善伴隨頦下脂肪凸起或豐滿的外觀。試驗納入健康成年(19至65歲,BMI≤40kg/m2)有中度或嚴重伴隨頦下脂肪凸起或豐滿(即,在5-點等級評分2級或3級,其中0=無和4=極等級),由臨床醫生和受試者兩方面評判分級。受試者接受直至6個治療用KYBELLA(N=514,複合試驗)或安慰劑(N=508,複合試驗)在不小於1個月間期。臨床試驗期間允許用冰/冷敷,局部和/或注射局部麻醉。注射容積是0.2mL沒注射部位,間隔1cm至頦下脂肪組織,它也用劑量每面積表示如2mg/cm2。對覆蓋整個治療區每個治療允許最大100mg(10mL)。在試者在第一次治療時給予平均6.4mL,而所有受試者6個治療,在第6個治療接受給予平均4.4mL。59%受試者接受全部6個治療。
在這些試驗中,均數年齡為49歲和均數BMI為29kg/m2。受試者的大多數是婦女(85%)和高加索人(87%)。在基線時,51%受試者有臨床醫生-分級頦下脂肪嚴重程度計分中等度和49%有嚴重頦下脂肪計分。
共-主要療效評估是根據最後治療後12周臨床醫生-報告和患者-報告的頦下脂肪頦下凸起或豐滿複合分級至少2-級和至少1-級改善。此外,在一個子組受試者(N=449,複合試驗)用核磁共振影像(MRI)評價頦下脂肪容積的變化。還使用6個問題的調查評價頦下脂肪視覺和情感的影響(快樂,煩惱,自我意識,尷尬,顯得衰老或超重),每個問題分級從0(一點沒有)至10(極度/非常)。
在KYBELLA組與安慰劑組比較當通過臨床醫生和患者複合分級觀察到頦下脂肪容積減小。
當用MRI評價時KYBELLA-治療受試者與安慰劑-治療受試者比較,有較大比例頦下脂肪容積減小至少10%(分別43%相比5%)。
KYBELLA組比安慰劑組總體患者-報告的滿意和自身-感知屬性顯示更大改善。
如何購買/貯存和處置
KYBELLA(去氧膽酸)注射液,10mg/mL是一種透明,無色,無菌溶液在2mL,單次患者使用小瓶供應在4小瓶,好醫友美國藥房提供專科藥物、處方藥物、非處方藥物、藥物配置、藥物注射以及各類非住院患者的藥物分發、諮詢、配送等各項服務。美國是醫藥分開的國家,藥房全部實行嚴格的處方藥與非處方藥分類管理。對處方藥的銷售,必須憑美國醫生(電子/紙質)處方。如今國內患者可以依託科技,實現遠程的病歷互動,由美國醫生根據患者病情開具電子處方,以正規渠道在美國藥房購買到處方藥。
貯存在20°C至25°C(68°F至77°F);外出允許15°C至30°C(59°F至86°F)[見USP控制室溫]。

