簡介
 電催化
電催化選用合適的電極材料,以加速電極反應的作用。所選用的電極材料在通電過程中具有催化劑的作用,從而改變電極反應速率或反應方向,而其本身並不發生質的變化。電極上施加的過電位也能影響反應速率,因此衡量電催化作用的大小,必需用平衡電位Ee時的電極反應速率,常稱為交換電流密度i0。電解池和原電池的電位分別為E1和E2。
原理
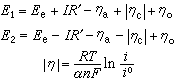
式中ηa和ηc分別為陽極和陰極的電活化過電位;I為電流;R′為電阻;n為電極反應的電子轉移數;R為氣體常數;T為熱力學溫度;F為法拉第常數;α為陰極反應的傳遞係數;ηc為其他過電位。顯然,交換電流密度愈大,則電活化過電位愈小,有利於反應的進行。
不同的金屬電極對釋氫反應的過電位有非常明顯的差異,在1Μ硫酸介質中,從鈀(i0=10安/米2)到汞(i0=10-8.3安/米2),這么大數量級的變動,就足以反映出電極材料對反應速率的影響。
 電催化
電催化電催化作用覆蓋著電極反應和催化作用兩個方面,因此電催化劑必需同時具有這兩種功能:①能導電和比較自由地傳遞電子;②能對底物進行有效的催化活化作用。能導電的材料並不都具有對底物的活化作用,反之亦然。因此,設計電催化劑的可行辦法是修飾電極。將活性組分以某種共價鍵或化學吸附的形式結合在能導電的基底電極上,可達到既能傳遞電子,又能活化底物的雙重目的。當然,除了考慮電極的巨觀傳質因素外,還有一個修飾分子和基底電極的相互作用問題,這種相互作用有待進一步研究。
